迷走神经是连接大脑与身体关键器官的重要通路。通过植入式电极刺激该神经,可有效抑制体内炎症反应,为自身免疫疾病的治疗提供全新策略。然而,传统植入式神经刺激器通常面临三大挑战:刚性平面电极与柔软曲面神经的几何形态难以匹配,术中缝合固定容易造成组织损伤,外源电刺激信号与天然生物电信号形式不同,难以实现自适应通讯。上述问题严重制约了植入式神经刺激器在体内的长期安全性和有效性。
近日,中国科学院深圳先进技术研究院医学成像科学与技术系统全国重点实验室、医工所智能医用材料与器械研究中心杜学敏研究员团队,在多功能铁电生物电子领域取得了重要研究进展,相关成果以“Multifunctional ferroelectric bioelectronic interfaces for long-term biosafe vagus nerve modulation”为题,发表在国际权威期刊Advanced Materials上。

文章链接:https://doi.org/10.1002/adma.73023
该研究提出的多功能铁电生物电子界面(FBI)通过材料与结构的协同创新,实现了对迷走神经的自适应贴合、免缝合固定,以及基于光控极化变化产生的仿生电信号刺激,在动物模型中展现出了长期安全、稳定且高效的抗炎疗效,为治疗难治性自身免疫疾病带来了新希望。
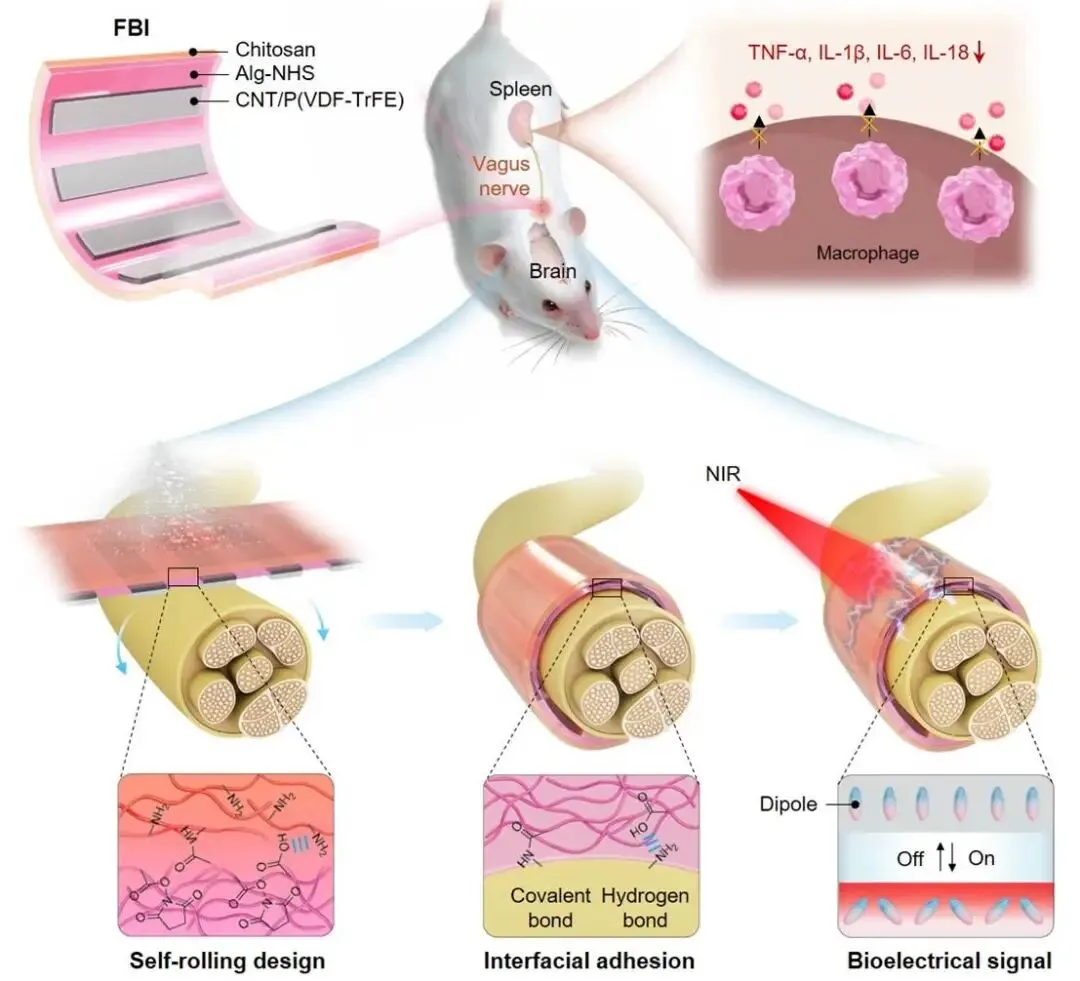
图1 集自卷曲、免缝合、仿生电信号多功能于一体的FBI设计
该FBI由三层功能材料协同整合而成,共同赋予其自卷曲、免缝合和仿生电信号输出的多重功能(图1)。其中,底层由具有优异生物相容性的壳聚糖和海藻酸钠天然多糖构建的双层水凝胶基底,在遇水后可自动卷曲成管,精准包裹直径仅约0.5毫米的细小神经,实现无缝贴合;与此同时,水凝胶表面的活性基团可与神经组织表面形成氢键和共价键,提供约50千帕的粘附强度,使器件无需缝合即可牢固固定于神经表面。位于器件上层的聚偏氟乙烯-三氟乙烯铁电高分子与碳纳米管复合条带(CNT/P(VDF-TrFE)),则可在近红外(NIR)光照射下发生偶极子取向偏转,从而产生与天然神经元极化变化所诱导动作电位相似的仿生电信号。基于此,该FBI能够通过NIR遥控,有效刺激神经细胞响应;与传统硅基光电材料相比,其诱发的细胞毒性活性氧水平降低了16倍。在活体实验中,FBI可自动卷曲包裹大鼠迷走神经并实现自粘合,通过激活胆碱能通路进而有效降低血清中促炎细胞因子水平。植入自由活动的大鼠体内长达60天后,FBI不仅未出现移位、神经压迫和局部炎症,而且仍能保持与植入初期一致的抗炎效果。值得强调的是,FBI通过多功能融合,有效解决了传统神经刺激器与神经组织长期存在的界面失配问题,不仅为迷走神经刺激治疗自身免疫疾病提供了更安全、持久的解决方案,其设计理念也有望推广至其他周围神经和中枢神经调控,以及脑机接口、组织工程等多个生物医学领域。
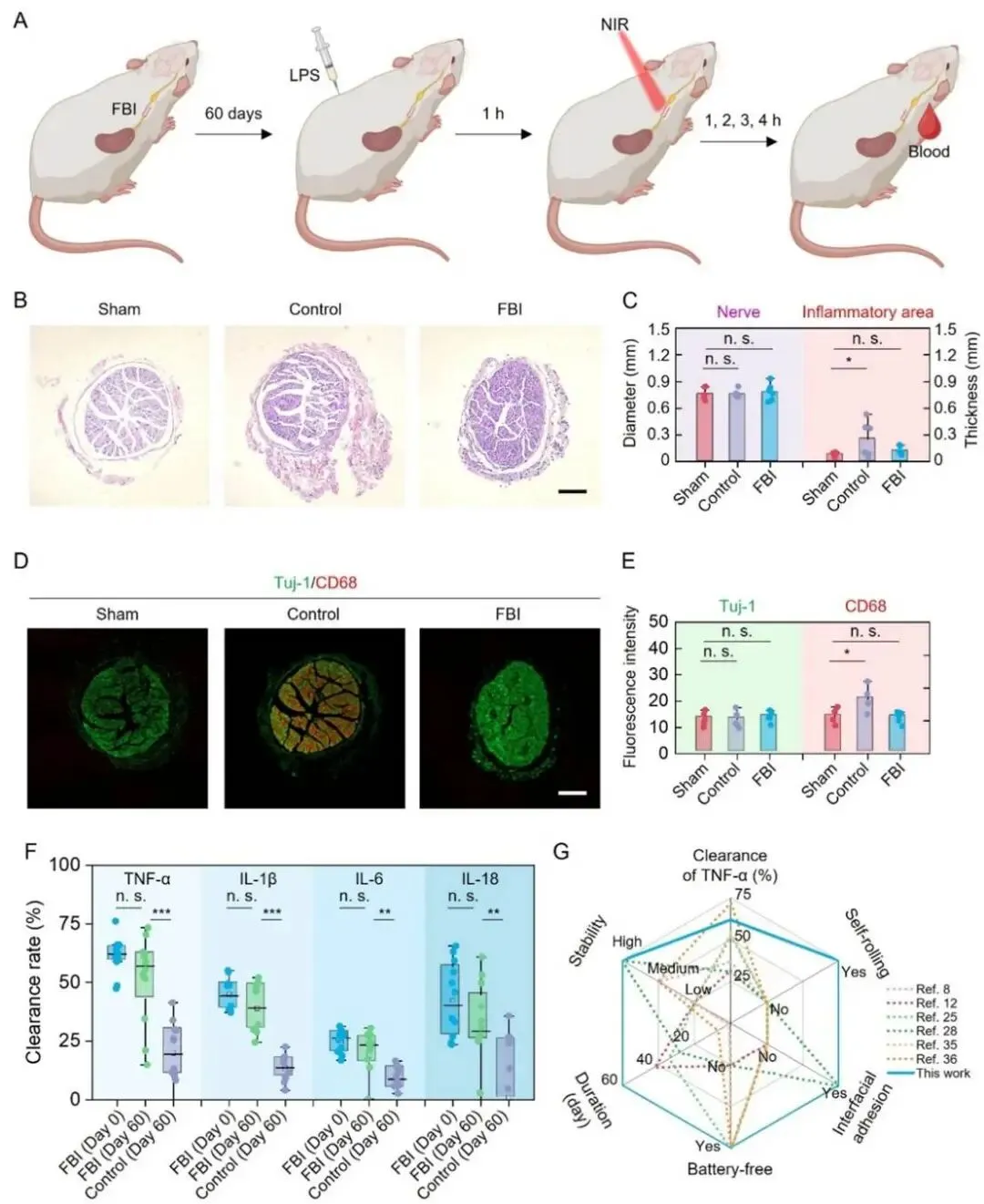
图2 FBI长期安全有效调控大鼠迷走神经抗炎
中国科学院深圳先进技术研究院医学成像全国重点实验室/智能医用材料与器械研究中心杜学敏研究员为该论文的通讯作者,硕士研究生祝栩乐、赵启龙副研究员为共同第一作者,北京大学基础医学院王韵教授为共同作者。该论文得到国家自然科学基金、国家重点研发计划、中国科学院青年创新促进会、深圳市医学研究专项、深圳市基础研究计划等科技项目支持。
团队长期招聘博士后,欢迎将简历发送至:xm.du@siat.ac.cn
网站:https://ibmd.siat.ac.cn/
纳米材料 定制合成
请联系
王老师
198 2262 5523