最新!中国科学院深圳先研院国家杰青JACS-合成生物学-光驱动CO₂和H₂O合成C4化合物:基于工程化光催化剂-微生物联合体
- 2026-05-24 14:51:19
一、中文标题
光驱动CO₂和H₂O合成C4化合物:基于工程化光催化剂-微生物联合体(Light-Driven C4 Biosynthesis from CO2 and H2O via Engineered Photocatalyst-Microbial Consortia)
二、发表单位及通讯作者
主要单位:中国科学院深圳先进技术研究院(合成生物学研究所、定量合成生物学重点实验室、深圳合成生物学创新研究院)、上海科技大学(物理科学与技术学院)
通讯作者:马贵军(Guijun Ma)、高翔(Xiang Gao)、王新宇(Xinyu Wang)、钟超(Chao Zhong)
三、科学问题
如何通过整合Z型光催化剂与工程化微生物联合体,构建一种无需牺牲剂、仅以CO₂和H₂O为原料、能够一步法光驱动合成多碳化合物(如丁二酸)的生物杂合系统?
四、发表时间
时间:2026年3月18日
链接:https://pubs.acs.org/doi/10.1021/jacs.5c16572
五、摘要
开发利用太阳能将CO₂转化为高值化学品的可持续技术仍是一项关键挑战。本研究构建了一种整合Z型光催化剂与工程化微生物联合体的生物杂合系统,无需牺牲剂即可实现光驱动的丁二酸合成。该系统由表达甲酸脱氢酶的大肠杆菌生物膜(将CO₂光还原为甲酸)和经适应性进化的需钠弧菌(将甲酸升级为丁二酸)组成。在6小时内,该系统产丁二酸0.068 mM,表观量子产率0.154%。生物膜与光催化剂保持共形接触,可循环使用4次;同时,光催化剂提供的甲酸使需钠弧菌的活力提高11%。同位素示踪表明约20%的碳来自CO₂。本研究为太阳能驱动多碳合成建立了可持续平台。
六、研究背景
大气CO₂浓度持续攀升,亟需开发将其转化为高值化学品的可持续技术。自然光合作用虽为太阳能驱动CO₂固定提供了蓝图,但其效率低(<1%)且产物谱有限,推动了人工替代方案的发展。其中,半导体-微生物生物杂合系统因其整合了半导体宽光谱吸收和微生物催化特异性的优势而备受关注。近期研究已实现光驱动CO₂还原为甲酸、甲烷、乙酸等C₁-C₂化合物,效率超越自然光合作用。
然而,现有系统面临两大关键瓶颈:(1)依赖牺牲剂(如半胱氨酸、甘油、三乙醇胺、抗坏血酸)作为空穴清除剂,增加了成本并复杂化了产物纯化;(2)由于非生物C-C偶联的动力学瓶颈和自养底盘遗传工具匮乏,难以高效合成多碳(C₃⁺)分子。现有解决方案(如电催化与微生物发酵串联)引入了操作复杂性和能量损失。迄今,仅以CO₂和H₂O为原料光驱动合成多碳化学品仍是巨大挑战。
相比之下,自然微生物联合体通过劳动分工实现高效的碳升级——这一策略启发了合成生物学中分布式生物合成的方法。尽管该范式在生物杂合系统中仍未被充分探索,但有望突破人工光合成的C₂上限。本研究报道了一种光催化剂-微生物联合体生物杂合系统,整合Z型光催化剂与工程化大肠杆菌生物膜和需钠弧菌,实现了以H₂O为唯一电子供体的光驱动CO₂固定合成丁二酸。
七、研究结果
结果1、光催化剂-生物膜生物杂合体的制备与表征
通过质粒系统改造大肠杆菌MG1655,使其表达CsgAHis(诱导生物膜形成)和甲酸脱氢酶(FDH)。TEM和刚果红染色确认生物膜形成,Western blot验证FDH表达。采用RuO₂-Mo:BiVO₄(模拟光系统II,氧化H₂O)和Ru@Cr₂O₃-Rh:SrTiO₃(模拟光系统I,还原CO₂)构建Z型光催化剂,ITO作为电子传递介质。将光催化剂滴铸于ITO玻璃,退火后于M63培养基中培养72小时,形成光催化剂-生物膜生物杂合片。SEM显示生物膜(3.04 μm)均匀共形包覆光催化剂(16.58 μm)。TEM和EDS证实光催化剂纳米颗粒锚定于生物膜基质。光辅助KPFM显示两种光催化剂间表面光电压差达230 mV,证明有效的电荷分离。
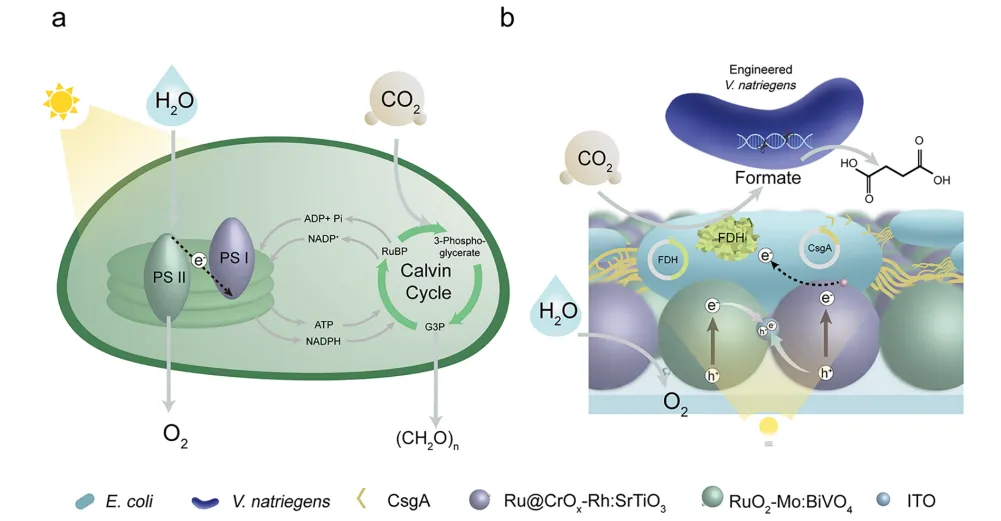
图1 光驱动微生物群落生物杂合系统
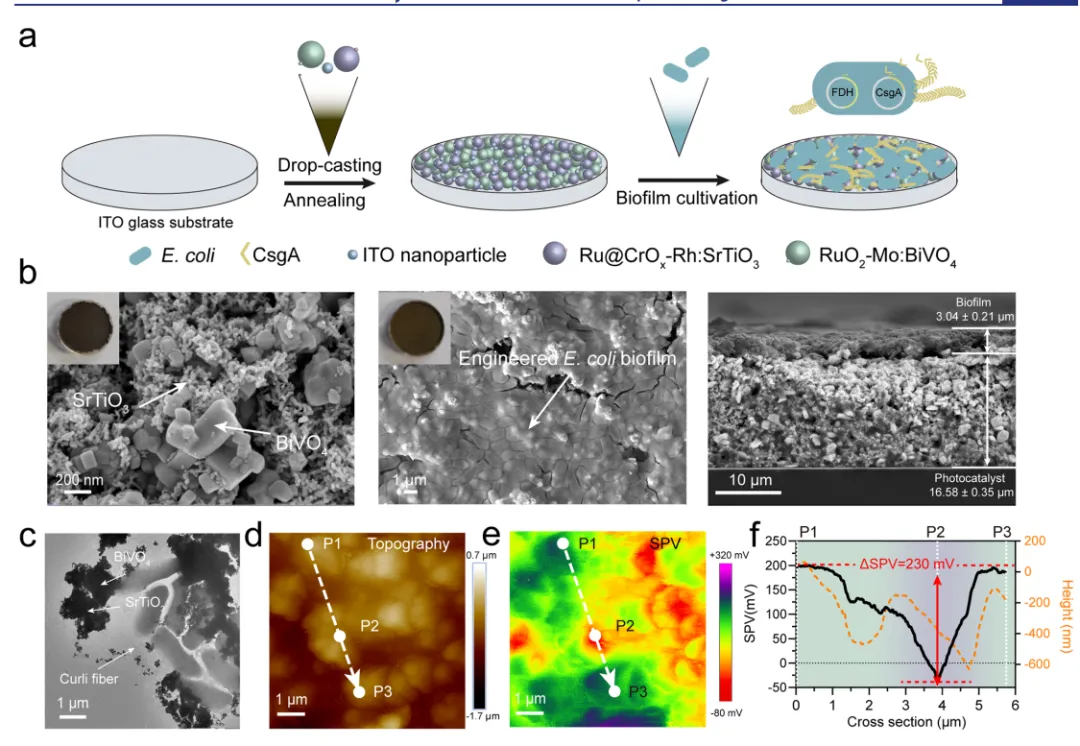
图2 特性表征
结果2、光催化CO₂还原产甲酸
在无有机碳源、含100 mM NaHCO₃的M9培养基中,光照射下系统产甲酸。瞬态光电流测试显示,生物杂合片的光电流约10 μA/cm²,且平均电子传输时间从光催化剂片的0.1358 s缩短至生物杂合片的0.1265 s,表明生物膜加速了电荷分离与转移。细胞内NADH/NAD⁺比值从0.173增至0.439,证明光催化剂增强了胞内还原力。6小时产甲酸0.68 mM,太阳能-甲酸转化效率约0.019%;450 nm单色光下AQY约0.148%。添加0.2%糖蜜副产物后,甲酸产量提高1.9倍。¹³C同位素示踪显示约20.6%的甲酸来自CO₂。生物杂合片可直接循环使用或经24小时再培养后循环使用,3次循环后仍保持产甲酸能力。Live/Dead染色显示反应6小时后细菌存活率仍达94.59%,生物膜保护了细菌免受光损伤。ICP-MS显示光催化剂中元素溶出极少。
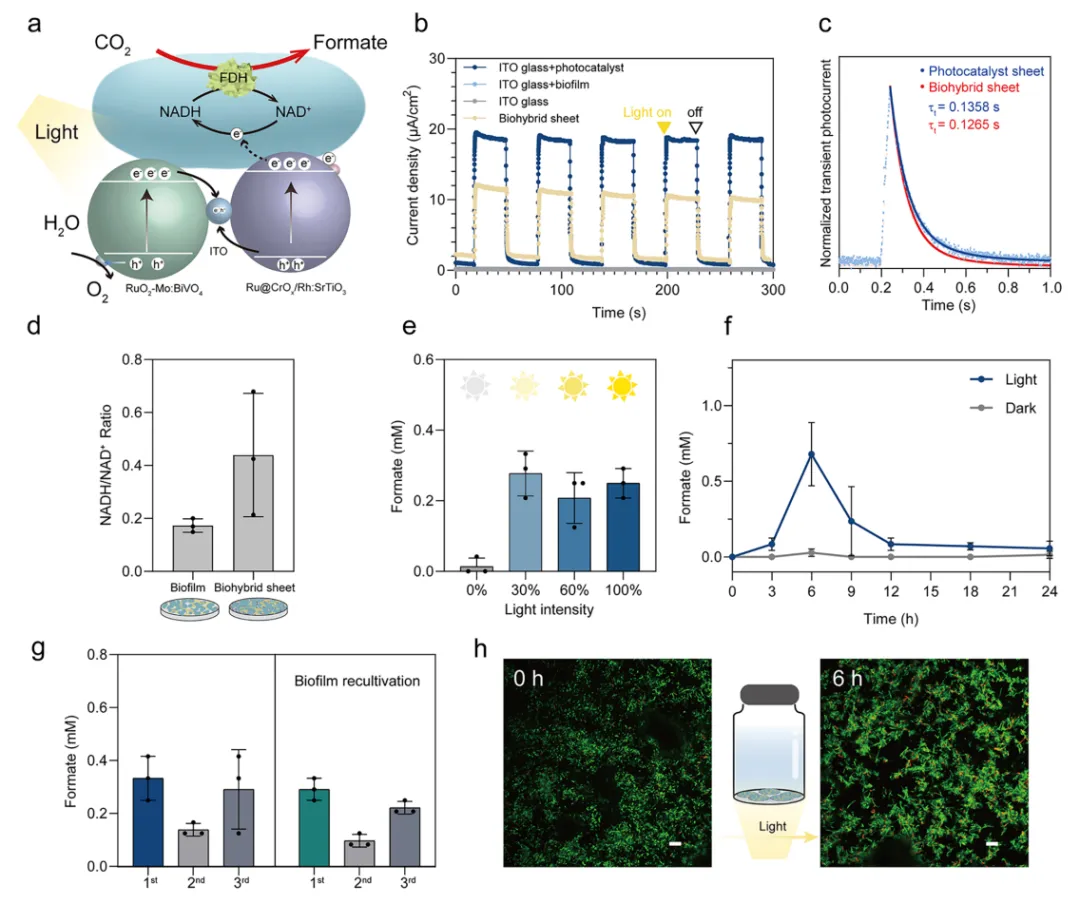
图3 光催化性能
结果3、光催化产丁二酸:光催化剂-微生物联合体
将光催化剂-生物膜片与适应性进化的需钠弧菌(ALE V. natriegens)共培养。该菌经适应性进化获得利用甲酸为碳源合成丁二酸的能力(在10 g/L甲酸中12小时产33 mg/L丁二酸)。在含100 mM NaHCO₃的无碳源M9培养基中,光照6小时,系统产丁二酸0.068 mM,太阳能-化学转化效率约0.0077%,同时溶液中检测不到甲酸(被V. natriegens消耗)。对照实验证实光、光催化剂、工程化大肠杆菌和ALE需钠弧菌均为必需。450 nm单色光下AQY约0.154%。¹³C同位素示踪显示丁二酸中约20%的碳来自CO₂。Live/Dead染色和流式细胞术显示,共培养体系中ALE需钠弧菌的存活率较单独培养提高11%(48.7% vs 37.7%),证明甲酸供应维持了其活性。反应溶液中总ROS约75.79 μM,但细胞内ROS仅3.72 μM,低于致死浓度。生物杂合片经再培养后可循环使用4次,仍保持初始活性的64.2%。
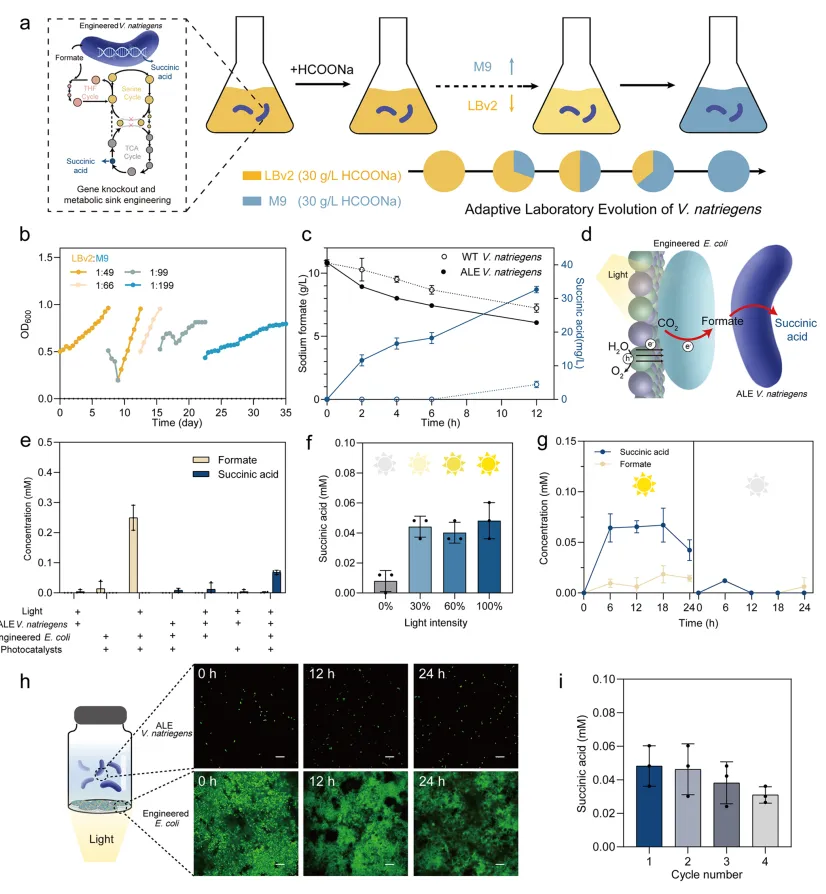
图4 微生物群落杂合系统生产琥珀酸
八、讨论
本研究通过理性整合Z型光催化剂与工程化微生物联合体,成功实现了以CO₂和H₂O为原料、无牺牲剂的光驱动丁二酸合成。系统通过劳动分工策略——大肠杆菌生物膜负责CO₂还原产甲酸,适应性进化需钠弧菌负责甲酸升级为丁二酸——突破了单一微生物难以同时完成光催化碳固定和多碳合成的限制。生物膜的共形包覆实现了高效界面电子传递和光催化剂-微生物的稳定连接,且生物膜保护细菌免受光损伤。然而,系统能量转化效率仍受限于异养代谢与光催化的竞争、FDH的催化效率瓶颈以及需钠弧菌的耗氧代谢。未来可通过引入合成碳固定途径(如还原性甘氨酸途径)降低对有机碳的依赖,通过酶工程改造FDH提高CO₂还原效率,并通过光电极分区设计缓解氧对丁二酸积累的影响。本研究为太阳能驱动的多碳化合物合成提供了模块化框架。
