深圳大学刘翼振等:基于比率型CRISPR策略实现单CpG位点甲基化的高分辨精准定量
- 2026-05-25 00:20:23
DNA甲基化作为一种关键的表观遗传修饰,在重大疾病的早期筛查与精准诊断中具有极高的标志物价值。然而,面对基因启动子区密集的CpG岛,如何排除相邻位点甲基化状态的干扰、实现单个CpG位点的高分辨精准定量,一直是临床分子诊断面临的重大挑战。传统的MS-HRM或qMSP技术往往只能评估扩增区域的平均甲基化水平,缺乏单点分辨率;而焦磷酸测序等金标准技术虽精度高,但流程繁复、耗时长且成本高昂。近年来,基于CRISPR-Cas的检测系统展现出了单碱基分辨的潜力,但常规CRISPR检测过度依赖绝对荧光信号强度,极易受到DNA起始输入量和扩增效率波动的干扰,在实际复杂样本的准确定量中受到了很大的限制。
基于此,深圳大学化学与环境工程学院刘翼振副教授团队开发了一种名为EPILIGHT的比率型CRISPR检测新策略,成功突破了高密度CpG区域精准定量的瓶颈,并展现出卓越的双重抗干扰能力(图1)。首先,在抗相邻位点干扰方面,作者通过将目标靶点“锚定”在crRNA间隔区中部的精准设计,成功规避了相邻位点未知甲基化状态对核心识别位点的空间与序列干扰,实现了实用意义上的单CpG位点独立解析。其次,在抗样本浓度与扩增波动干扰方面,EPILIGHT系统摒弃了传统的单一荧光绝对值依赖,而是通过双通道独立检测,计算“甲基化信号”占“总荧光信号(甲基化+非甲基化)”的比率(Proportional Signal, PS)来进行定量。研究表明,即使目标DNA的浓度在20 fM至200 fM之间发生剧烈波动,其比率信号PS值依然保持高度稳定,从根本上消除了由初始靶标浓度差异或等温扩增效率不一致所引发的定量偏差。
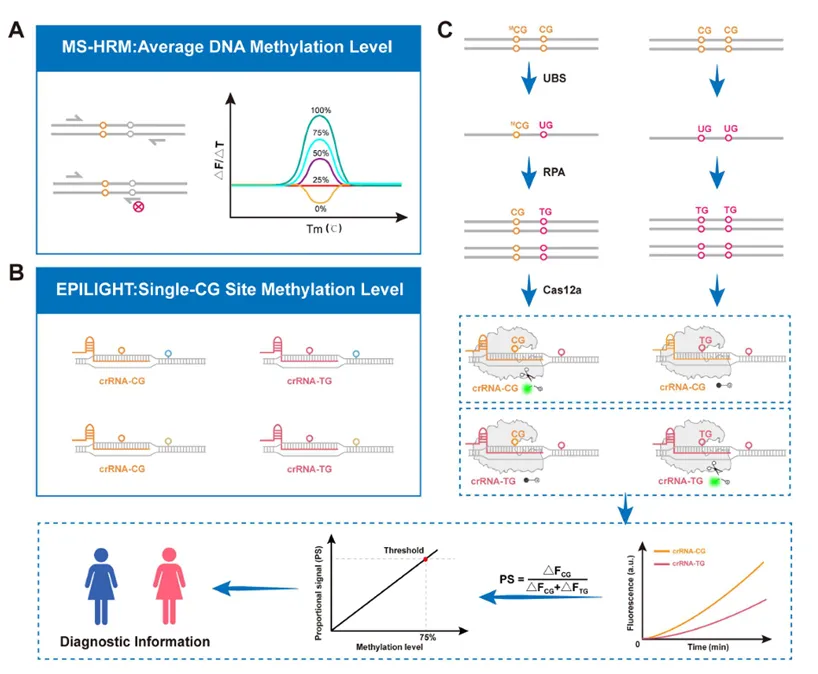 图1.EPILIGHT系统原理示意图
图1.EPILIGHT系统原理示意图得益于这种强大的抗干扰与精确定量能力,研究人员将该平台成功应用于系统性红斑狼疮(SLE)核心标志物——IFI44L基因启动子区域的临床检测中。如图2所示,在无需复杂测序的条件下,EPILIGHT全流程仅需70分钟即可出具结果。在涵盖真实SLE患者和健康对照的临床队列中,以75%(Site 1)和25%(Site 2)为诊断阈值,该系统表现出极高的临床诊断效能(灵敏度分别达96.2%和84.6%,特异性均为100%),且定量结果与耗时数天的金标准(焦磷酸测序)完全一致。总体而言,EPILIGHT是一种快速、低成本且极其可靠的表观遗传学分析工具,不仅为SLE的临床早筛提供了新方案,并有潜力广泛应用于其他依赖DNA甲基化标志物的重大疾病诊断中。
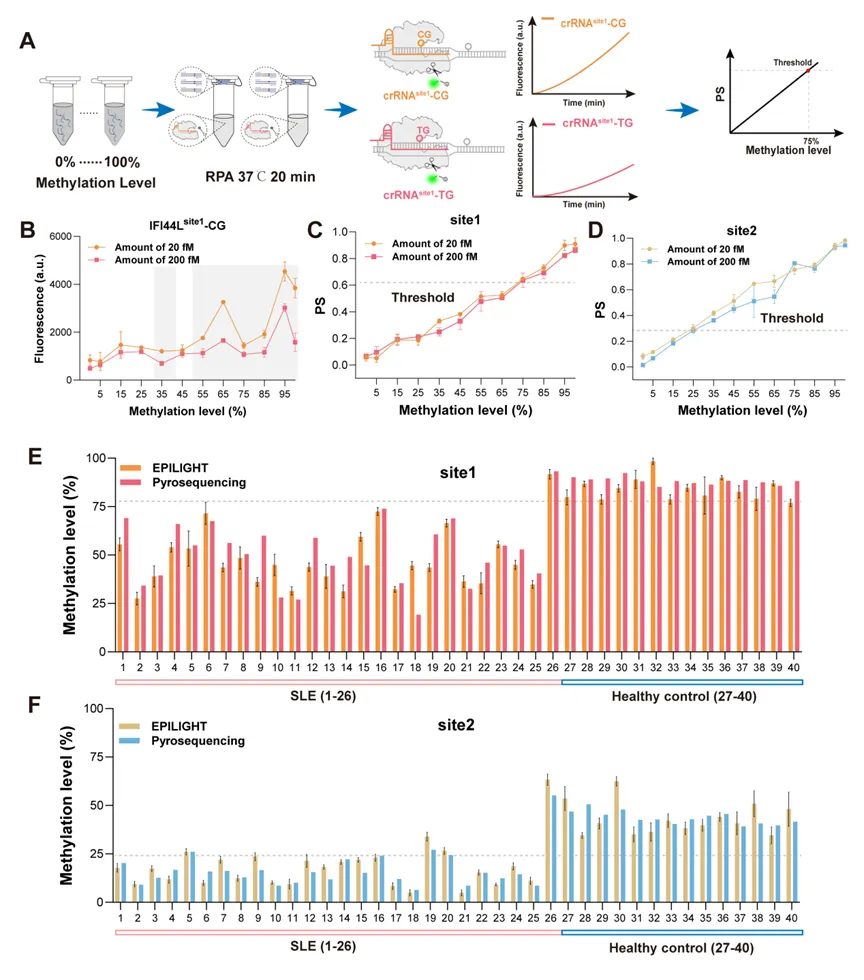 图2.EPILIGHT在SLE临床样本中的精准定量与诊断效能验证
图2.EPILIGHT在SLE临床样本中的精准定量与诊断效能验证该成果以“EPILIGHT: precise quantification of single-CpG methylation level with a ratiometric CRISPR strategy”为题,发表于Science China Chemistry上(https://doi.org/10.1007/s11426-025-3290-x)。论文第一作者为深圳大学化学与环境工程学院副研究员庄松宽、硕士研究生邓淦丰以及深圳市宝安区人民医院检验科徐羽中主任,通讯作者为深圳大学化学与环境工程学院刘翼振副教授。

刘翼振,深圳大学副教授、博士生导师,深圳市高层次专业人才。2014年毕业于武汉大学,获得理学博士学位。现任深圳大学发展规划部副处长(挂职)、化学与环境工程学院院长助理。主要围绕病原体、遗传、肿瘤等重大疾病的临床早期检测需求,从事新型CRISPR分子诊断技术与DNA等温扩增/信号放大检测新技术的研究。近年来以第一/通讯作者身份在Nat. Biomed. Eng.、Sci. China Chem.、Anal. Chem.、Biosens. Bioelectron.、Chem. Commun.等国际权威期刊上发表学术论文三十余篇,获授权国家发明专利6项。
扫描二维码或点击左下角“阅读原文”可查阅全文。

【扩展阅读】
喜讯!《中国科学: 化学》(中文刊)入选中国科技期刊卓越行动计划和中国科学院精品期刊
Science China Chemistry 2025年优秀论文评选结果发布!
Sci. China Chem.影响因子9.7 || 量质齐升创新发展
上海交通大学沈建磊团队综述:DNA分子探针实现细胞膜力学分析的研究进展
Science China Chemistry综述:人工智能在纳米医学中的应用
华东理工大学郭志前/中山医院沈亚星、冯明祥等:口服内质网靶向型近红外荧光探针实现术中胸导管无创、实时定位
西湖大学吴明轩课题组:依赖催化活性的Jumonji C赖氨酸去甲基化酶共价多肽探针开发

