深圳放大招!"细胞十条" 重磅落地,2028年冲刺200亿 CGT 产业规模
- 2026-05-13 02:52:49

2026年4月4日,深圳市发改委与市科技创新局联合印发《深圳市推动细胞与基因领域高质量发展工作方案》,推出十项核心举措(简称 "细胞十条"),明确提出到 2028 年的三大硬核目标:产业规模突破 200 亿元、IIT 项目累计完成50项、建成2个以上CRO/CDMO 公共服务平台并服务企业超 300 家,全面打造细胞与基因治疗 (CGT) 领域的全球创新高地深圳市发展和改革委员会
一、2028 年深圳 CGT 产业要达到什么水平?
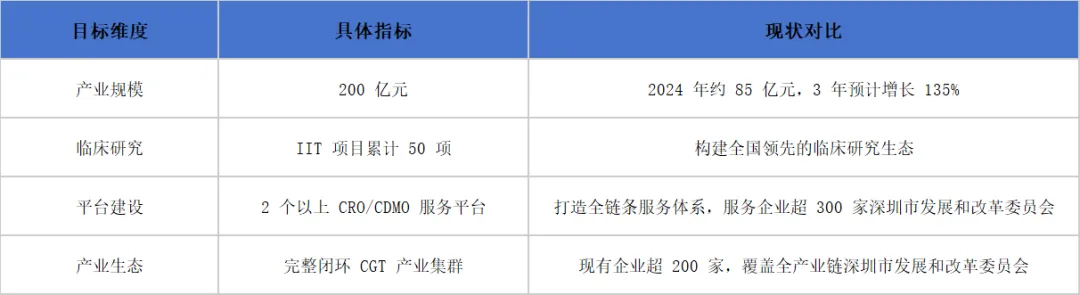
二、"细胞十条" 核心举措全解读
1️⃣ 强化招商引资,夯实产业根基
聚焦肿瘤、遗传病、自免疾病、罕见病四大临床急需领域,重点引进临床试验阶段药物管线与核心技术企业;依托前海优势,服务企业赴港上市、境外融资、外资项目落地,构建国际资本对接平台。
2️⃣ 突破关键核心技术,攻克 "卡脖子" 难题
围绕载体优化、新型递送系统、细胞快速扩增、AI数据挖掘四大方向,支持产学研联合攻关,重点突破基因编辑、质控标准、冷链存储等技术瓶颈,打造技术创新策源地。
3️⃣ 加速临床转化,提升IIT研究效率
支持三甲医院搭建专病临床研究平台,建立伦理审查联盟,缩短成果转化周期;推动粤港澳大湾区临床研究协同,加速创新产品从实验室到病床的转化速度。
4️⃣ 建设关键平台,完善产业服务生态
重点打造专业化CRO/CDMO 公共服务平台,提供从临床前到临床申报的一站式服务,构建 CAR-T、TCR-T、MSC、iPSC 等全品类细胞制剂制备能力;同步建设一流细胞制剂质量检测平台,为产品注册申报提供高标准质控保障深圳市发展和改革委员会。
5️⃣ 产业载体升级,打造 GMP 生产集群
鼓励企业建设符合 GMP 标准的规模化生产线,打造研发-中试-生产-仓储-检测的一体化 CGT 专业园区,推动技术从实验室走向规模化量产,降低生产成本。
6️⃣ 金融赋能创新,构建全生命周期支撑
发挥市级生物医药、细胞与基因等产业基金引导作用,撬动社会资本共同参与;建立市区联动的项目融资服务机制,积极开展重点项目并购投资和早期项目天使投资,构建覆盖企业全生命周期的金融支撑体系深圳市发展和改革委员会。
7️⃣ 支付创新破局,让患者用得起
推动商业保险将 CGT 产品纳入保障范围,开发按疗效付费、带病体专属保险,构建 "基本医保为主、商业保险补充" 的多元共付体系,降低患者支付门槛,促进创新产品市场准入与应用普及。
8️⃣ 深港跨境协同,打造国际合作高地
在前海蛇口自贸片区开展人体干细胞、基因诊断与治疗技术开发和应用扩大开放试点,争取试点范围拓展到河套深港科技创新合作区;建立特殊物品联合监管白名单,加速跨境研发物资流通。
9️⃣ 完善监管合规,筑牢安全防线
建立伦理审查快速通道和 "细胞治疗 + AI" 监管新模式,加强产品全生命周期追溯;试点干细胞合规收费改革,明确临床应用收费标准,促进产业规范化发展。
🔟 人才引育并举,夯实智力支撑
实施 "细胞与基因领域高端人才计划",引进全球顶尖科学家与创新团队;支持高校设立相关专业,建立 "产教融合" 人才培养机制,打造多层次人才梯队。
三、CGT 产业迎来最强政策东风
对企业:全方位赋能,降低创新门槛
研发端:核心技术攻关支持 + 公共平台共享,大幅降低研发成本,缩短研发周期
临床端:伦理审查加速 + IIT 项目支持,加速产品临床试验进程,提高成功率
产业化:GMP 园区建设 + CDMO 服务,解决中小微企业 "产能不足、质量不稳" 痛点
融资端:产业基金 + 深港资本对接,拓宽融资渠道,助力企业快速成长与上市
对患者:创新疗法触手可及
可及性提升:多元支付体系降低治疗费用,让更多患者用得起先进疗法
治疗选择增多:IIT 项目扩容至 50 项,加速创新疗法从实验室到临床应用
安全性保障:严格质控标准 + 全生命周期监管,确保治疗安全有效
对产业:打造全国 CGT 创新标杆
深圳已汇聚细胞与基因企业超 200 家,2024 年产业总营收超 85 亿元,随着 "细胞十条" 落地,到 2028 年将实现产业规模翻番(突破 200 亿元),IIT 项目数量全国领先,建成具有国际影响力的 CGT 产业集群,带动粤港澳大湾区生物医药产业整体升级。
四、从 "跟跑突破" 到 "领跑布局"
深圳正将细胞与基因治疗当成未来生物医药的核心王牌来打!"细胞十条" 不是简单的政策叠加,而是全链条、系统性、闭环式的产业扶持方案,精准击中 CGT 产业 "研发难、临床慢、生产贵、支付高" 四大痛点,为行业发展扫清关键障碍。
对于细胞与基因治疗企业而言,这是最好的时代,也是必须抓住的战略机遇。深圳正以开放的姿态、精准的政策、完善的生态,向全球发出邀请 —— 共同打造细胞与基因治疗产业的 "深圳高地",为人类健康事业贡献中国智慧与深圳力量深圳市发展和改革委员会!
818新政机遇及难点分析+CGT创新药开发及生物医学新技术临床转化路径全周期分析(包括临床过程,项目投入费用及开发周期等)交流会
2026年5月1日,818号令将正式施行,818 号令的出台,为生物医学新技术的转化应用搭建了全新路径,将有力推动行业高质量发展,而配套实施细则的落地,更是新技术项目具体落地实施的重要基础。
为精准把握细则核心要求,厘清临床研究备案与转化应用的具体流程、费用构成及未来发展方向,海南博鳌乐城医学公益基金会计划在成都组织“818新政机遇及实操难点分析+CGT创新药开发及生物医学新技术临床转化路径全周期分析(包括临床过程,项目投入费用及开发周期等)”交流会,特邀行业同仁参与本次研讨会,共同解读 818 号令细则条款、研判行业发展方向,明确新技术转化应用所需的技术储备与资金规划方案,明晰企业发展路径。
时间:4月11日
地址:成都市金牛区金泉路15号 四川新生命干细胞科技股份有限公司多功能厅

扫码报名
帮扶服务
离条例实施时间越来越近,由于生物医学新技术转化应用是一个长周期、多环节、高费用的过程,为了助力临床研究发起机构少走弯路,主编特意整合资源,助力大家实现转化,可在以下几个方面给大家提供帮助:
一、资料汇总
①818号令细则;
②818细则实施配套文件;
③生物医学新技术临床转化路径全周期分析(医院选择、临床试验所需费用及周期,未来发展规划等)电子版资料汇总;
④特殊区域的具体政策(海南博鳌、广东南沙、河北北戴河)
⑤海南博鳌乐城获批的干细胞临床转化应用汇总
⑥CDE已获批的IND项目汇总

二、一对一深入咨询对接
2026年5月1日,国务院第818号令将正式实施,万众期待的818号令细则也基本确定。从目前的征求意见稿来看,818号令虽然为生物医学新技术转化应用提供了一个出口,但是收费并没有那么简单,并不是所有企业都合适走生物医学新技术的路线。818号令实施后,企业该如何发展,该如何按照818号令进行项目落地,以及落地过程需要多久,需要准备多少资金,临床方案如何设计,合作医院如何选择,为了解决大家困扰,特邀请行业专家一对一帮扶指导,如果有需要咨询者,可以深入沟通。咨询内容包括不限于:
(1)根据企业本身情况,如何选择未来发展道路;
(2)如何根据新政策调整方向;
(3)818政策落地全流程帮扶(医院选择,项目合作,临床落地细节,样本合规获取,临床方案设计等);
(4)融资对接等。

三、非临床实验
动物水平安全性和有效性验证。
四、药物申报及818临床转化全流程赋能
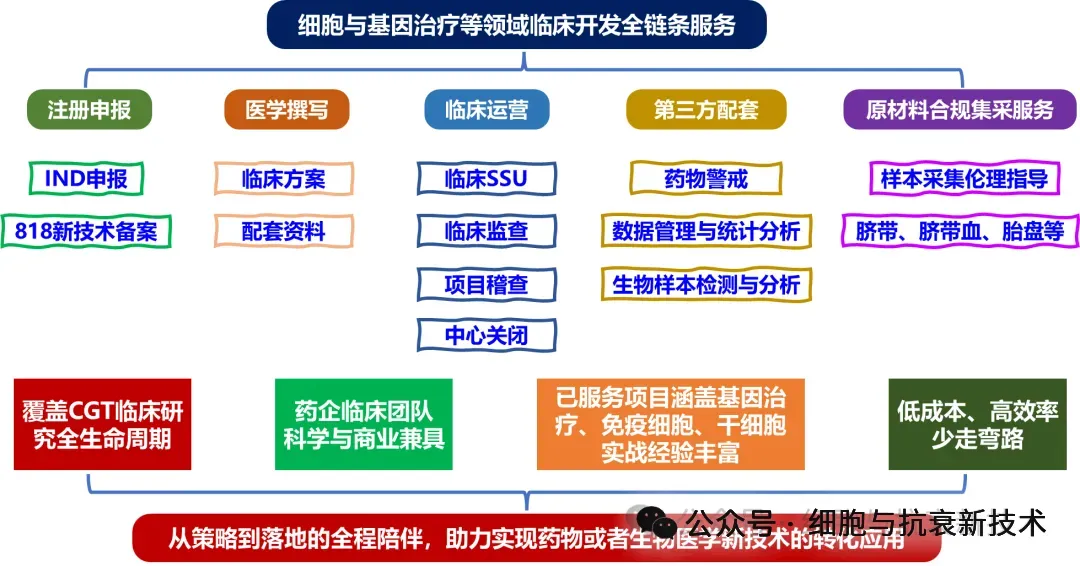
编辑│知风
愿生命如水螅一般永恒!


推荐阅读


