深圳先进院《Bioactive Materials》:利用双外泌体组合策略缓解骨关节炎
- 2026-05-10 12:46:17
骨关节炎(OA)是一种慢性退行性关节疾病,主要表现为疼痛、活动受限和关节畸形,甚至可能导致残疾,严重影响患者的生活质量。据统计,中国约有1.32亿患者,全球超过6.5亿人受OA影响。由于其病理多态性,OA在临床上难以治疗。据报道,OA的主要病理微环境包括慢性炎症、合成代谢抑制、软骨退化等。骨关节炎患病率与发病率持续上升,亟需高效治疗方案。然而,单一疗法难以应对OA复杂的病理机制,也难以实现全面的软骨保护功能。
来自中国科学院深圳先进技术研究院的阮长顺等团队通过RNA测序分析,发现骨髓间充质干细胞来源外泌体(BMSC-Exo)与软骨祖细胞来源外泌体(CPC-Exo)具有差异化的miRNA富集特征:前者主要调控巨噬细胞功能,后者侧重调节软骨细胞活性。本文开发了双外泌体组合策略,通过联合具有抗炎作用的BMSC-Exo和抗分解代谢的CPC-Exo,同步调控巨噬细胞极化和软骨细胞表型,从而缓解骨关节炎进展。当通过甲基丙烯酰化透明质酸微球递送至大鼠膝关节腔后,该双外泌体组合通过改善关节炎症与分解代谢环境,显著延缓了OA进展,并进一步揭示了关键干预通路(包括miR-708–5p/NRP-1、miR-431/BRCA-1/PLK-1及miR-7a-5p/NOTCH-3)。本研究通过定制化设计外泌体组合实现多靶点调控,为OA治疗提供了新的潜在策略。相关工作以题为“Harnessing bi-exosome combination alleviates osteoarthritis progression”的文章发表在2026年02月02日的期刊《Bioactive Materials》。

【miRNA的特征分析与比较】
本文分别从大鼠骨髓和关节软骨中分离出骨髓间充质干细胞(BMSCs)和软骨祖细胞(CPCs),其中CPCs与软骨细胞(CCs)通过纤连蛋白差异亲和法进行分离。在确认细胞纯度(CD29与CD90阳性率>98%,CD45与CD11b阳性率<1%)后,进行三系分化实验。BMSCs与CPCs均能向中胚层来源细胞(成骨细胞、软骨细胞、脂肪细胞)分化,但呈现明显差异化的分化倾向。茜素红染色与油红O染色的定量分析表明,BMSCs的成骨与成脂能力分别是CPCs的7.04倍和1.44倍;而阿尔新蓝染色显示其成软骨潜能较弱,仅为CPCs的0.69倍(图1B)。这些结果在一定程度上解释了本文在前期骨软骨缺损修复体内研究中观察到的差异。
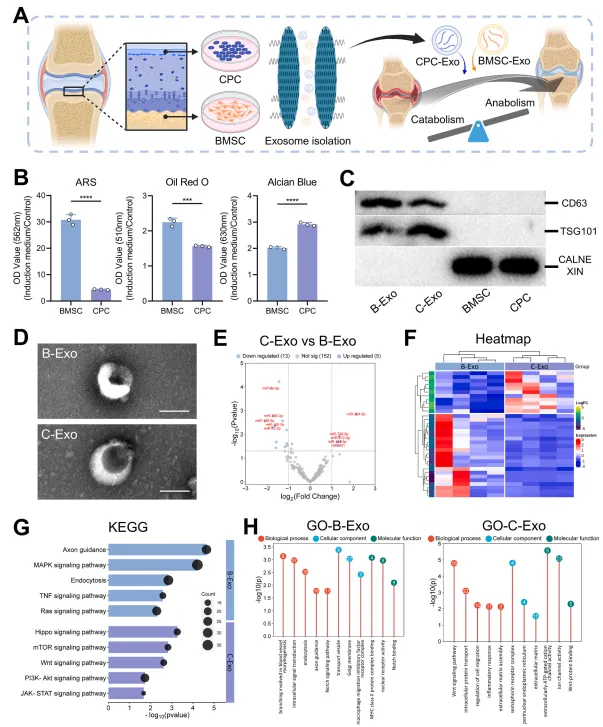
图1 B-Exo与C-Exo中miRNAs富集情况对比
【B-Exo与C-Exo对体外培养软骨细胞及骨髓源性巨噬细胞作用的比较研究】
测序结果支持了本文的假设:外泌体可能是揭示骨髓间充质干细胞与软骨祖细胞在组织修复潜能差异的另一关键指标。具体而言,B-Exo在调控炎症反应和巨噬细胞行为方面表现更优,而C-Exo主要影响细胞合成代谢与凋亡过程。为验证其功能,本文选取了关节损伤与修复过程中的两类关键细胞——软骨细胞和巨噬细胞进行研究(图2A)。首先,通过IL-1β刺激软骨细胞建立体外骨关节炎模型,并分别用B-Exo或C-Exo进行处理。结果显示,两种外泌体均能显著改善IL-1β诱导的软骨细胞迁移与增殖能力(图2B、C)。在外泌体刺激2天后,C-Exo组表现出比B-Exo更显著的促增殖效果(图2C)。炎症环境会破坏软骨细胞合成-分解代谢平衡,导致软骨细胞外基质合成减少(表现为Sox-9和Col-II基因表达下调),而两种外泌体均能缓解这一趋势。与B-Exo组相比,C-Exo处理的软骨细胞中Sox-9和Col-II转录水平分别提高33.31%和22.21%(图2D)。通过流式细胞术检测外泌体对IL-1β诱导软骨细胞凋亡的影响,发现IL-1β刺激使细胞凋亡率从2.97±0.38%升至8.53±0.54%,而C-Exo组凋亡率(4.47±0.60%)显著低于B-Exo组(7.09±0.12%)(图2E)。综合来看,C-Exo在促进软骨细胞增殖、增强细胞外基质合成及抑制凋亡方面均优于B-Exo。
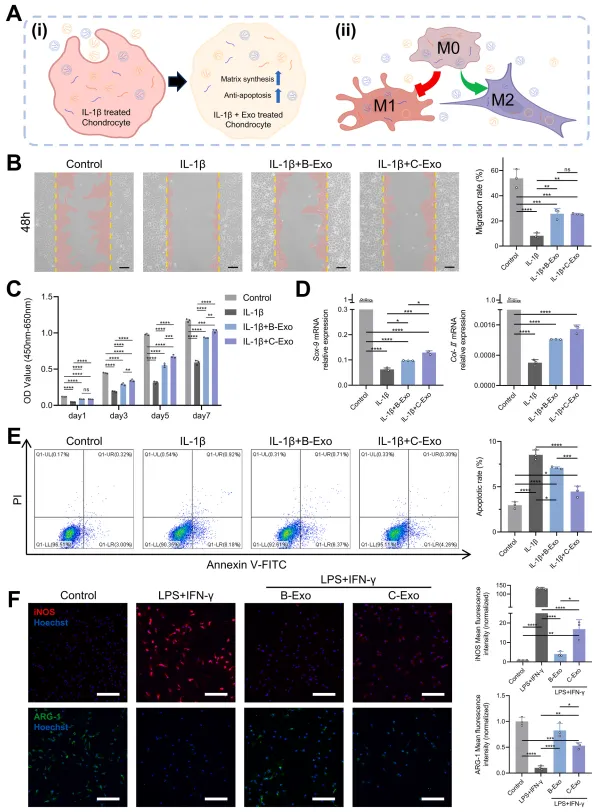
图2 B-Exo与C-Exo对体外软骨细胞及骨髓源性巨噬细胞的作用分析
【利用外泌体组合策略在体外保护软骨细胞免受炎症微环境影响并调控骨髓源性巨噬细胞极化】
基于B-Exo与C-Exo的功能差异,本研究提出联合使用两种外泌体治疗骨关节炎的策略(图3A)。首先通过DiI和DiO分别标记B-Exo与C-Exo,细胞摄取实验证实两类外泌体均可被软骨细胞和骨髓源性巨噬细胞内化(图3B),这是其发挥生物学效应的先决条件。随后评估BC-Exo联合治疗方案对软骨细胞合成与分解代谢的影响:通过蛋白免疫印迹检测软骨形成特异性转录因子SOX-9发现,IL-1β组表达量最低,而IL-1β+B-Exo、IL-1β+BC-Exo及IL-1β+C-Exo组呈现递进式升高。其中IL-1β+C-Exo与IL-1β+BC-Exo组的SOX-9水平分别达到IL-1β+B-Exo组的1.77倍和1.43倍(图3C)。qRT-PCR结果显示,BC-Exo组的蛋白聚糖(Acan)基因表达量较B-Exo组提升1.31倍,较C-Exo组提升1.29倍(图3F)。作为软骨细胞外基质的主要结构成分,Acan基因表达上调提示BC-Exo在IL-1β存在环境下可能具有更强的促软骨修复作用。
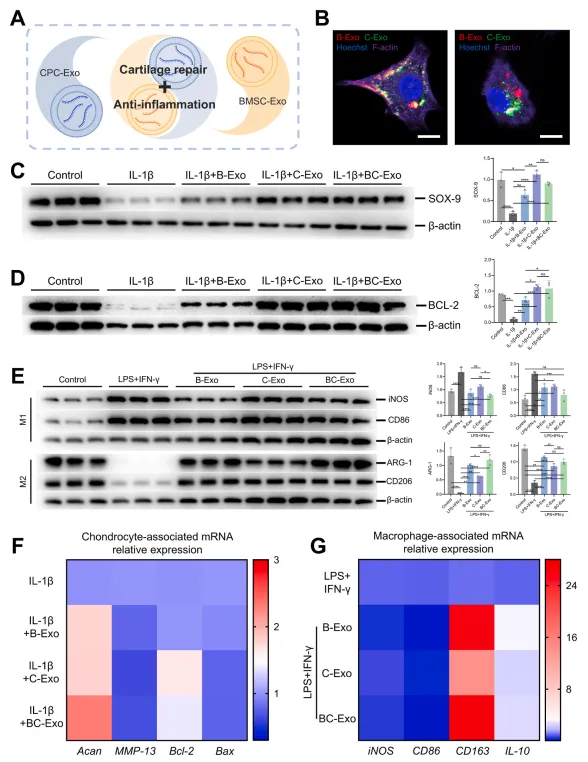
图3 外泌体在体外保护软骨细胞及调控巨噬细胞极化的功能研究
【外泌体组合递送微球的制备与表征研究】
将外泌体负载于生物材料中,可实现其在关节腔内的持续稳定释放,从而延长治疗效果。本研究开发了可注射水凝胶微球作为外泌体的递送载体。如图4A(i)所示,通过微流控技术将外泌体封装至HAMA中形成微球。负载外泌体的HAMA水凝胶经流变学分析表明,HAMA-Exo与纯HAMA在紫外光交联后储能模量均从0.01 Pa急剧上升至约45 kPa,说明外泌体的掺入未损害HAMA水凝胶的光交联能力。在测试温度范围(10–40°C)内,外泌体的加入未显著改变HAMA水凝胶的热敏特性。随后采用微流控系统制备了三种负载外泌体的HAMA微球:B-Exo-MS、C-Exo-MS及BC-Exo-MS。显微观察显示,水凝胶微球在油相与水相中均保持优异的形态完整性(图4B),平均直径为111 ± 35 μm(图4D)。荧光标记实验进一步证实,B-Exo与C-Exo在微球内负载水平相近且分布均匀(图4C),这一特性有利于实现平稳的持续释放。
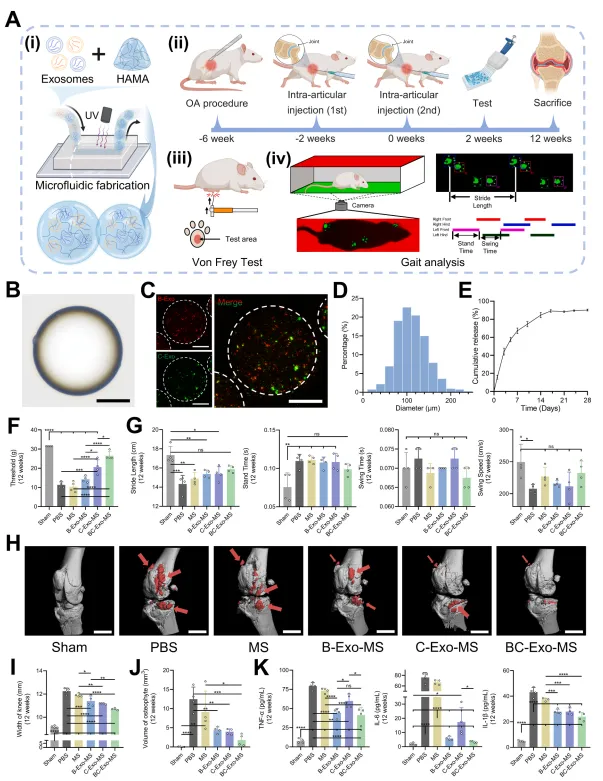
图4 外泌体体内抗骨关节炎效应的动态演变
【外泌体组合在体内展现出抗骨关节炎效应】
滑膜组织的H&E染色显示,PBS组和MS组均出现滑膜衬里细胞显著增多、细胞密度明显升高及血管翳形成等病理改变,而B-Exo-MS与BC-Exo-MS治疗能有效缓解这些病变(图5B)。滑膜炎评分证实,B-Exo-MS与BC-Exo-MS在减轻滑膜炎症方面疗效相当(P=0.9539),且均显著优于C-Exo-MS(P值分别为0.0055和0.0324)。同样,滑膜免疫荧光染色显示,B-Exo-MS组和BC-Exo-MS组的CD86+细胞比例显著低于PBS组和MS组;而CD206+细胞比例则显著高于PBS组和MS组。C-Exo-MS组的CD86+与CD206+细胞比例在五组中处于中间水平(图5F、G)。这表明B-Exo与BC-Exo均能通过诱导巨噬细胞向M2型极化,缓解病理性的炎症微环境。
本研究进一步通过组织学与免疫组化染色评估关节软骨内细胞外基质(ECM)和软骨细胞(CCs)表型的变化。假手术组关节软骨表面光滑、结构排列有序、番红O/固绿染色深染;而PBS组和MS组则出现软骨结构严重破坏、细胞分布不均、番红O/固绿染色减弱。相比之下,BC-Exo-MS组和C-Exo-MS组虽存在软骨损伤,但仍保持结构完整性且无软骨下骨暴露,OARSI评分较低(图5A-C)。免疫组化分析显示,在COL-II染色切片中,BC-Exo-MS组和C-Exo-MS组的软骨染色更为深染,而B-Exo-MS组仅显示有限染色区域(图5D)。半定量分析表明,BC-Exo-MS组的COL-II染色强度最高(与C-Exo-MS组相比P=0.012,与B-Exo-MS组相比P<0.0001)。
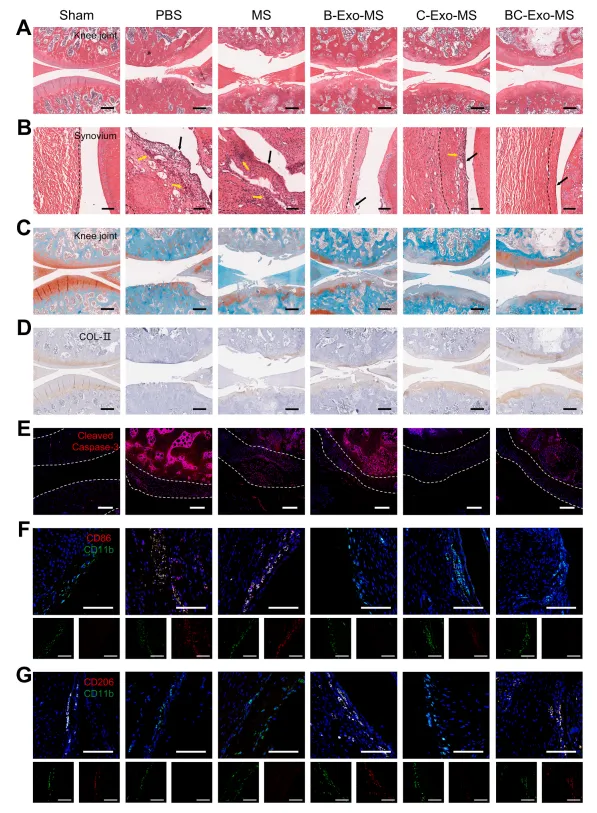
图5 关节腔内注射外泌体后的组织学变化
【体内转录组揭示外泌体组合缓解骨关节炎进展的潜在机制】
本文后续的研究聚焦于解析BC-Exo调控炎症、促进细胞外基质合成及推动软骨再生的潜在机制。通过对BC-Exo-MS组与MS组大鼠膝关节软骨区域组织进行治疗后2周的转录组分析(图6A),差异表达基因热图显示组间基因表达谱存在显著差异。差异基因火山图进一步凸显了BC-Exo对炎症调控与软骨修复的影响,共鉴定出272个上调基因与237个下调基因(BC-Exo-MS组 vs MS组),其中标记出五个代表性相关基因(图6B)。通过GO富集分析与KEGG通路分析,进一步明确了这些差异基因的功能意义。在BC-Exo对基质再生与软骨修复的作用方面,GO分析显示相较于MS组,BC-Exo-MS组的上调基因(如Col-IIa1与Cytl1)主要参与细胞外基质合成、含胶原细胞外基质生成及软骨稳态调控(图6B、C)。同时,下调基因表明BC-Exo处理抑制了金属肽酶的表达(图6C)。包括MMP-3与MMP-13在内的多种基质金属蛋白酶是软骨基质降解的关键介质。
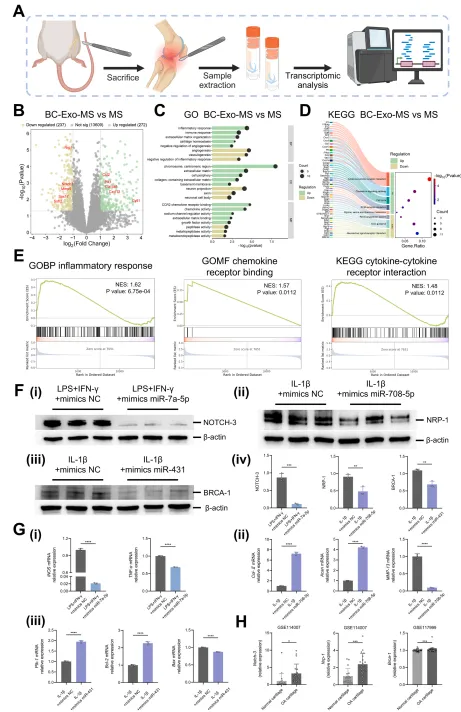
图6 BC-Exo生物效能调控机制的探索
【总结与展望】
综上所述,本研究揭示了B-Exo与C-Exo独特的功能意义,以及双外泌体组合的抗骨关节炎功效。除骨关节炎外,纳米级外泌体目前在多种疾病领域也受到广泛关注。事实上,开发外泌体或其他分泌组作为细胞疗法的替代方案具有内在优势:植入的外源性细胞易受宿主病理微环境(如缺氧、炎症和氧化应激)影响,导致异常死亡(如铁死亡)并损害分泌组功能;而通过GMP标准培养细胞获取的外泌体不仅继承了母细胞的生物功能,还能抵抗宿主应激压力。此外,通过在细胞培养过程中进行可控刺激,可进一步增强其功能。作为系列研究的一部分,本研究通过简化B-Exo与C-Exo联合给药剂量验证了该概念的可行性,并观察到有趣的现象。后续研究将着力解决遗留问题:例如通过脂质体等合适纳米载体评估miR-7a-5p/miR-708–5p/miR-431混合物的功能,可直接揭示其疗效;需优化微球系统以实现更持久的药物释放,避免多次关节腔内注射。此外,骨关节炎的恶化或缓解依赖于多细胞相互作用,解析其互作机制对理解骨关节炎干预策略至关重要。这些方面将是本研究团队未来研究的重点优化方向。
参考资料:
https://doi.org/10.1016/j.bioactmat.2025.11.050

联系我们