深圳大学刘心元/顾强帅JACS丨铜催化立体汇聚C-S交叉偶联!
- 2026-04-07 23:46:59

烯基化合物广泛存在于天然产物和功能分子中,过渡金属催化的交叉偶联是构建烯基结构的重要方法。传统的双电子氧化加成机制通常保持烯烃几何构型,因此需要使用高E/Z纯度的烯基卤化物原料。
然而,几何纯烯基卤化物的合成和分离往往具有挑战性,这限制了相关方法的应用范围。相比之下,自由基活化策略可通过弯曲σ型烯基自由基的快速立体异构化或近似线性π型烯基自由基的形成来消除起始烯烃的立体化学信息,理论上可实现立体汇聚反应。
但烯基自由基具有极高的反应活性,且烯基C-X键解离能较高,使得其不对称催化控制面临重大挑战。亚砜亚胺作为亚砜的氮杂类似物,在生物活性分子和手性配体中具有重要应用,但催化不对称合成S-手性烯基亚砜亚胺的方法仍十分匮乏。
近日,南方科技大学大学刘心元、顾强帅、Li-Wen Fan团队在Journal of the American Chemical Society发表了题为"Cu-Catalyzed Stereoconvergent and Enantioselective C−S Cross-Coupling of Alkenyl Halides with Sulfenamides via Alkenyl Radicals"的研究论文。该研究针对烯基卤化物交叉偶联中立体化学控制的难题,发展了基于烯基自由基的立体汇聚不对称催化新策略。

• 首次实现铜催化烯基卤化物的立体汇聚不对称C-S交叉偶联反应 • 通过烯基自由基中间体消除初始烯烃几何信息,实现E/Z混合原料的单一立体选择性转化 • 建立可见光驱动Cu/光氧化还原与芳基自由基介导XAT双反应体系 • 高效构建含三取代和四取代硫键烯基的手性亚砜亚胺 • 产物可多样化转化为多种S-手性硫(VI)骨架,包括亚砜亚胺、磺基二亚胺等
📄 全文速览
过渡金属催化的交叉偶联是安装烯基的核心策略。烯基卤化物的常规双电子氧化加成通常是立体保持的,因此通常需要几何高度富集的(E)-或(Z)-烯基卤化物,这使得(E/Z)-混合原料的立体汇聚不对称交叉偶联具有挑战性。
该研究报告了一种立体汇聚和对映选择性的铜催化烯基碘和溴与硫代酰胺的C-S交叉偶联反应,通过消除初始烯烃几何信息的烯基自由基中间体提供S-手性烯基亚砜亚胺。
该反应在可见光驱动的Cu/光氧化还原条件或铜催化的芳基自由基介导的卤素原子转移(XAT)条件下进行,以广泛的底物范围提供具有高烯烃立体选择性和对映选择性的富对映体产物。
该方法具有可扩展性,所得手性烯基亚砜亚胺可容易地多样化为一系列S-手性硫(VI)骨架,为难以获得的富对映体硫立体烯基骨架提供模块化途径。
📊 图文解读
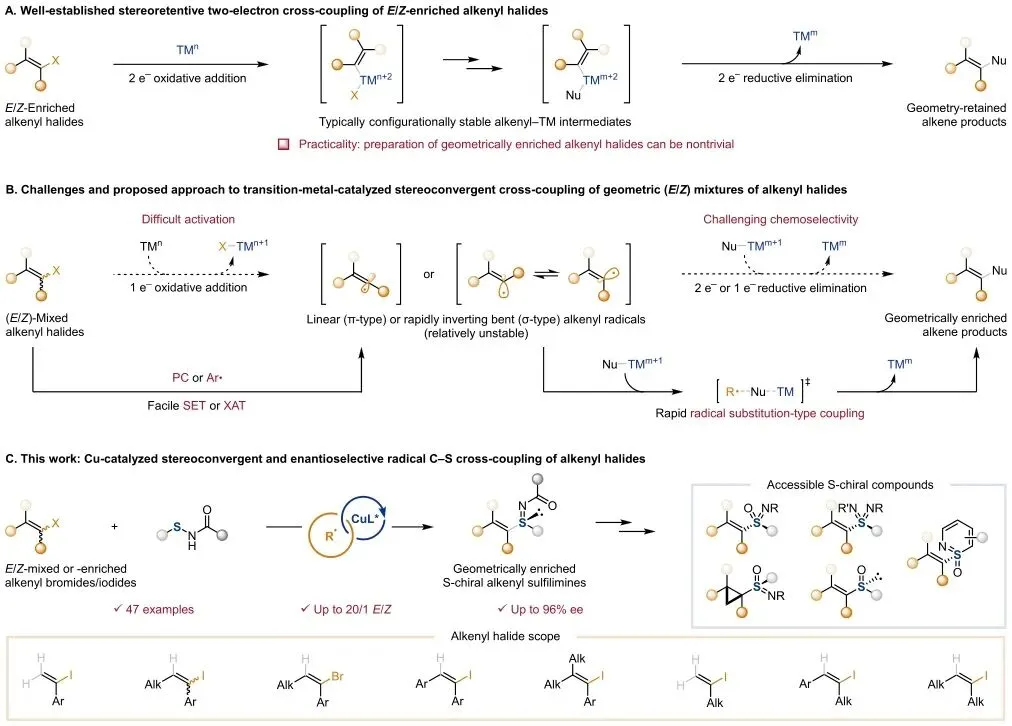
图1 | 铜催化立体汇聚和对映选择性烯基卤化物自由基C-S交叉偶联的动机与发展。TM,过渡金属;Nu,亲核试剂;PC,光催化剂;Ar,芳基;SET,单电子转移;XAT,卤素原子转移。
该图阐述了反应的设计理念和机制演变。传统双电子氧化加成途径保持烯烃几何构型,需要高纯度E/Z原料;而自由基途径通过σ型或π型烯基自由基中间体消除立体化学信息,实现立体汇聚。
研究采用可见光驱动SET或芳基自由基介导XAT策略活化烯基卤化物,经铜/手性配体催化实现不对称C-S键形成,构建S-手性亚砜亚胺。
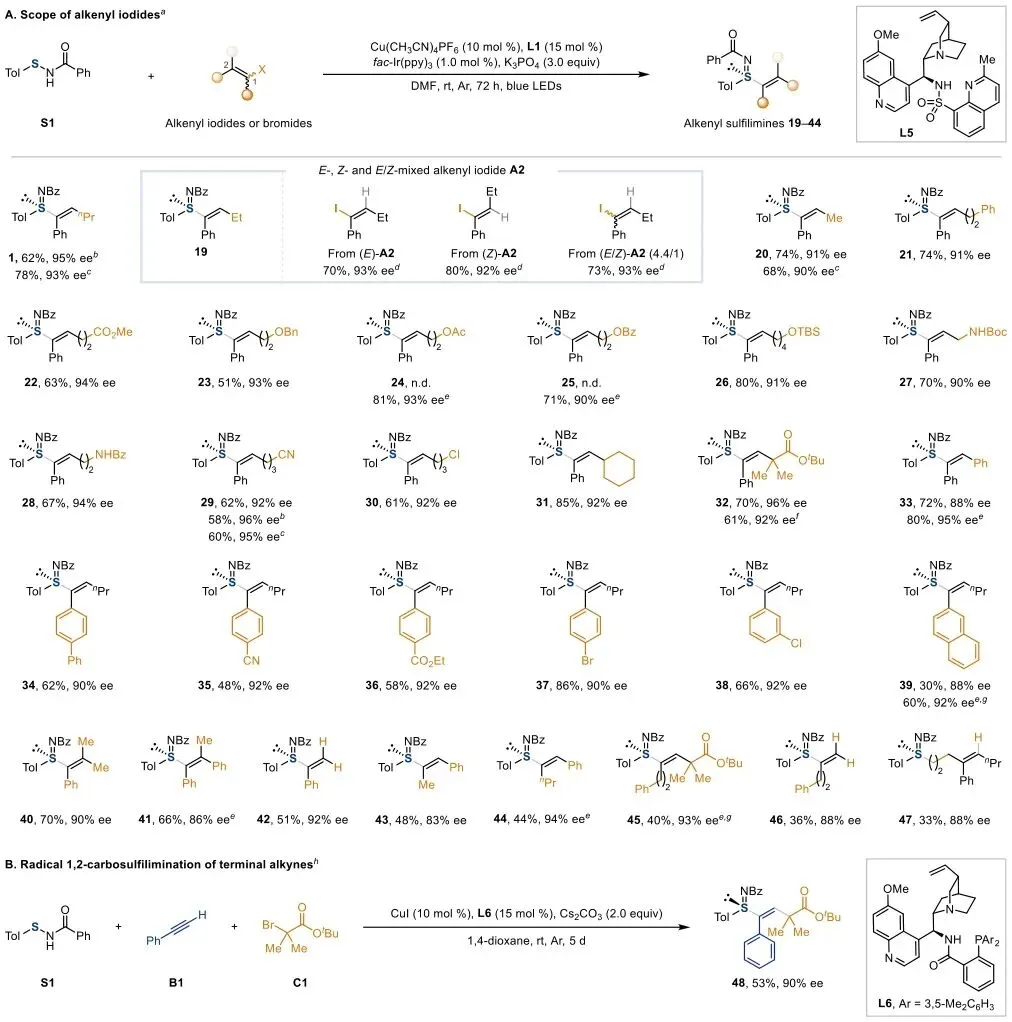
图2 | 烯基碘的底物范围及炔烃自由基1,2-碳亚砜亚胺化反应的拓展。a标准反应条件:硫代酰胺S1(0.20 mmol),烯基碘A(1.5当量),Cu(CH₃CN)₄PF₆(10 mol%),L1(15 mol%),fac-Ir(ppy)₃(1.0 mol%),K₃PO₄(3.0当量),DMF(2.0 mL),室温,氩气,蓝光LED照射72 h。b使用(Z)-烯基碘(Z)-A1或(Z)-A12。c使用(E/Z)-混合烯基碘((E/Z)-A1: 6.5/1; (E/Z)-A3: 2.8/1; (E/Z)-A12: 1/1.3)。d粗反应混合物的¹H NMR分析测定19的E/Z比(>20:1)。e硫代酰胺S(0.20 mmol),烯基碘A(1.5当量),CuI(10 mol%),L1(15 mol%),MesN₂BF₄(2.0当量),K₃PO₄(3.0当量),MTBE(4.0 mL),室温,氩气,4天。f使用A5-Br代替A15-I。g使用L5(15 mol%)代替L1。h硫代酰胺S1(0.10 mmol),炔烃B1(2.0当量),叔丁基α-溴代异丁酸酯C1(3.0当量),CuI(10 mol%),L6(15 mol%),Cs₂CO₃(2.0当量),1,4-二氧六环(1.0 mL),室温,氩气,5天。产率为分离产率,ee值由手性HPLC分析测定。Tol,对甲苯基;N.d.,未检测到。
该图系统展示了反应的底物普适性。烯基碘部分涵盖三取代、四取代、1,1-二取代等多种取代模式,包括含酯基、醚、酰胺、氰基等官能团的底物,均获得良好收率与优异对映选择性。
关键实验表明,E-富集、Z-富集或E/Z混合原料均给出相同结果,证实立体汇聚特性。研究还将方法拓展至炔烃的自由基1,2-碳亚砜亚胺化,实现三组分不对称双官能团化。
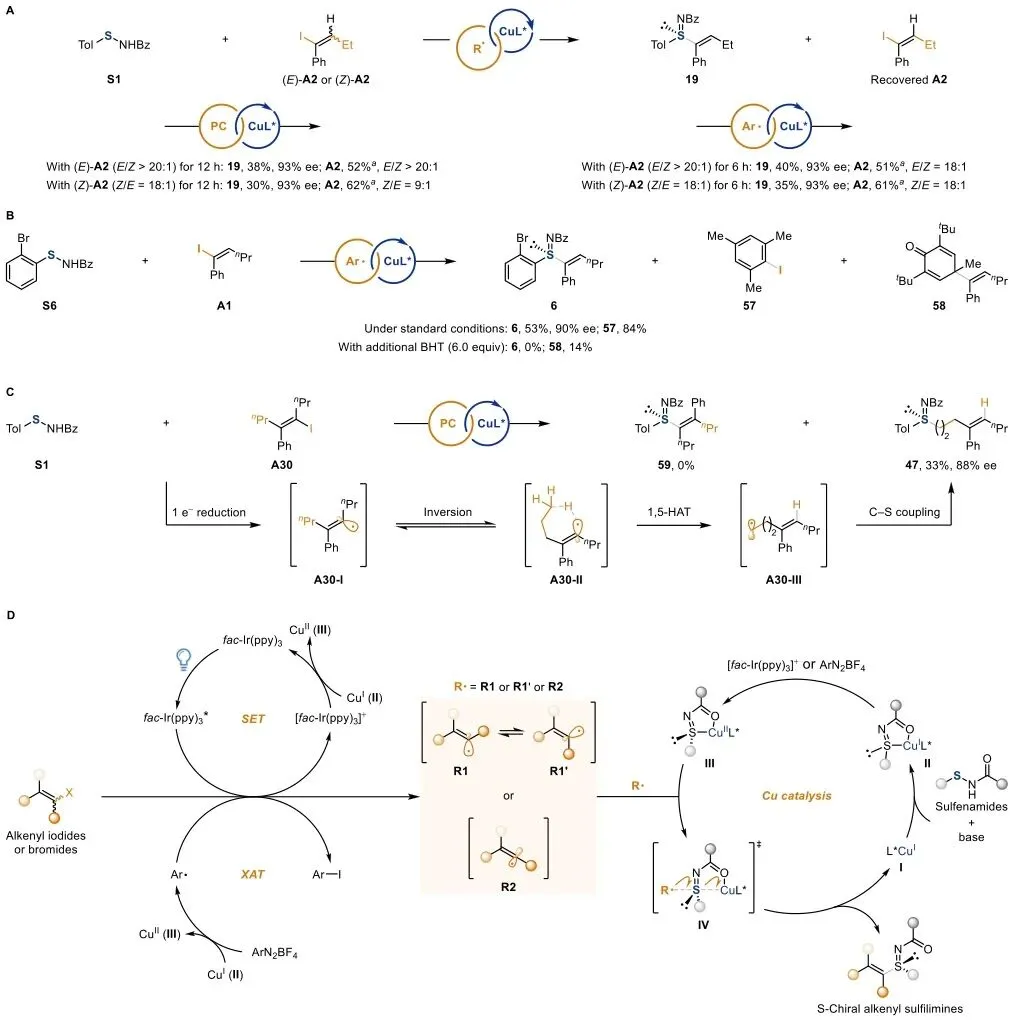
图3 | 机理研究和提出的催化循环。a回收产率基于A2的初始量计算。
该图通过控制实验验证反应机理。时间进程实验表明,无论起始原料为E-或Z-构型,反应过程中回收的烯基碘均保持高几何纯度,排除了直接E/Z互变异构路径,支持烯基自由基中间体的立体汇聚机制。
研究还观察到1,5-氢原子转移副产物,进一步佐证自由基中间体的存在。基于这些证据,提出了光氧化还原或XAT生成烯基自由基,经铜/手性配体捕获实现不对称C-S键形成的催化循环。
📝 总结
该研究成功发展了首例铜催化的烯基卤化物立体汇聚不对称C-S交叉偶联反应,通过烯基自由基中间体策略解决了传统方法对高纯度E/Z原料的依赖问题。双反应体系(可见光驱动Cu/光氧化还原和芳基自由基介导XAT)的建立为不同结构底物提供了灵活选择。
反应具有优异的底物普适性和官能团耐受性,可高效构建含三取代和四取代烯基的手性亚砜亚胺。克级规模实验和多样化衍生化证明了方法的实用价值,产物可转化为亚砜亚胺、磺基二亚胺等多种S-手性硫(VI)骨架,为相关生物活性分子的合成提供了新途径。该工作为烯基自由基的不对称催化控制提供了重要范例。
Cu-Catalyzed Stereoconvergent and Enantioselective C−S Cross-Coupling of Alkenyl Halides with Sulfenamides via Alkenyl Radicals, Journal of the American Chemical Society, 2026, DOI: 10.1021/jacs.6c02132
#深圳大学#刘心元#顾强帅#JACS#铜催化#烯基自由基#不对称催化

