深圳“细胞十条”出台 —— 细胞与基因治疗产业地方制度创新的监管逻辑、路径差异与全流程合规体系构建(含实务建议)
- 2026-05-14 01:44:04

前言
2026年4月4日,深圳市发布《关于支持细胞与基因产业高质量发展的若干措施》(业内称“细胞十条”),围绕肿瘤、遗传病、罕见病等临床急需领域,明确管线引进、企业招引、全产业链扶持等核心措施,依托前海政策推动产业集聚与国际化布局。同期,海南博鳌乐城国际医疗旅游先行区(下称“乐城先行区”)持续通过制度组合拳推进细胞治疗监管突破,构建了“特许准入+真实世界数据+闭环监管”的先行先试体系。
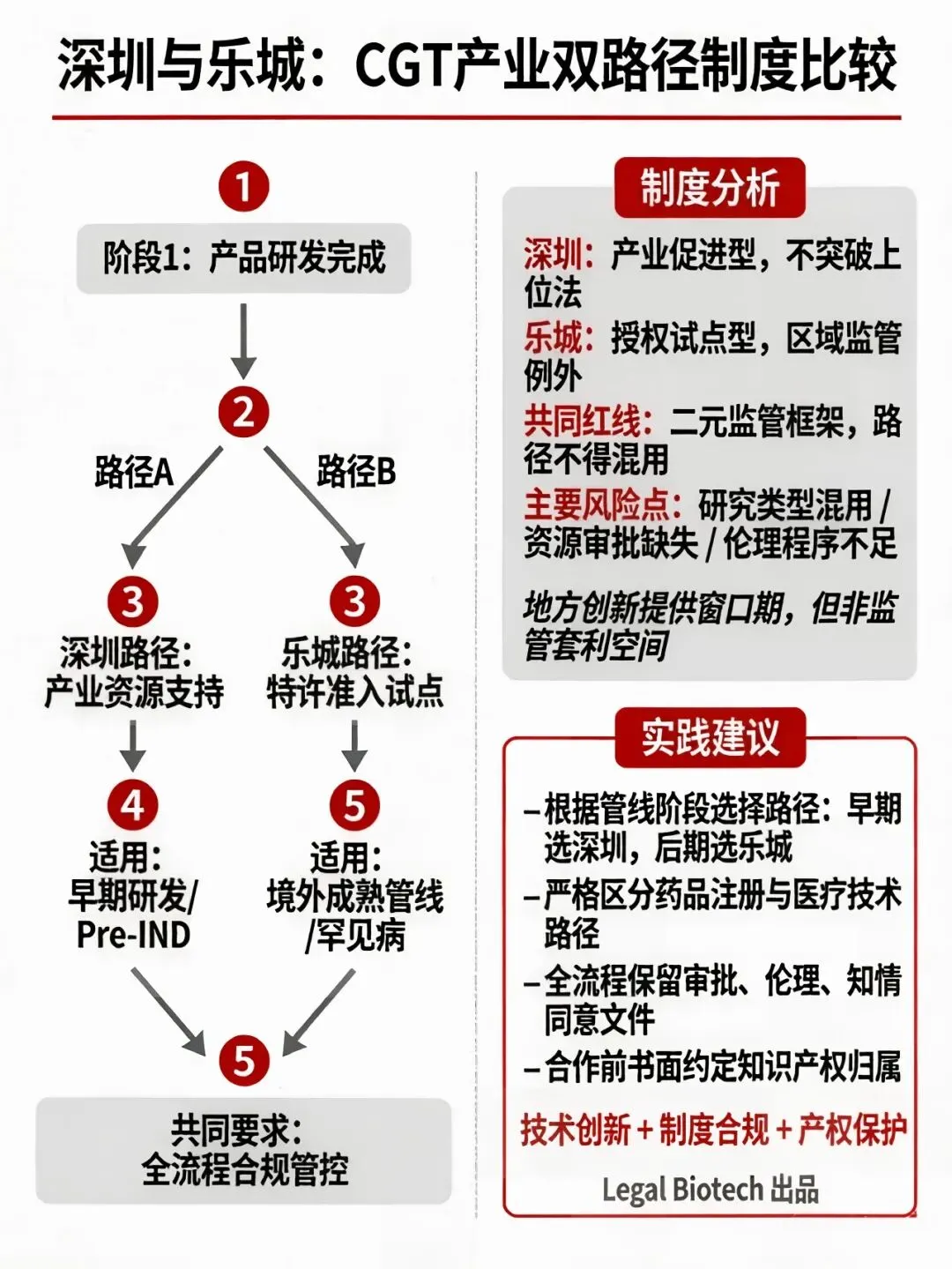
这两类实践,代表了我国细胞与基因治疗(CGT)领域两大核心发展方向:一类是以产业集聚与研发赋能为核心的要素驱动路径(深圳),一类是以临床转化与监管突破为核心的特许试点路径(乐城先行区)。在国家层面CGT监管框架持续完善但细分规则仍待细化的背景下,地方制度创新已成为影响企业研发路径、临床转化与商业化进程的核心变量。本文将从政策拆解、制度对比、法律风险、实务指引等多个维度,梳理CGT产业的合规逻辑与路径选择。
一、深圳“细胞十条”:制度定位、核心规则与法律边界
(一)核心定位:国家监管框架内的全产业链产业赋能
深圳“细胞十条”的核心逻辑,是在不突破药品、医疗技术、人类遗传资源上位法框架的前提下,通过产业要素优化配置,降低企业研发转化成本,推动创新资源集聚,本质是监管框架内的产业促进工具,而非监管突破。其核心政策重点集中在三个维度:
靶向支持产业集聚。聚焦临床急需领域,重点引进临床阶段CGT管线与拥有核心技术的创新企业,通过研发资助、场地支持、投融资扶持降低企业早期成本,同时推动关键原材料、核心设备、质控检测平台本地化布局,构建全产业链生态。 打通临床转化链路。支持本地医疗机构建设CGT临床研究中心,优化伦理审查机制,提升临床试验承载能力,推动研究者发起的临床研究(IIT)与注册临床试验(IND)协同衔接,加快创新技术的临床验证。 前海开放政策协同。依托前海合作区在跨境资金流动、国际科研合作、数据跨境合规流动等方面的制度优势,支持企业引进国际创新管线、开展跨境临床试验合作、引入海外高端人才,提升产业国际化水平。
(二)法律边界与适用场景
从法律效力来看,深圳“细胞十条”是地方政府出台的产业激励与服务保障措施,不具备突破上位法监管规则的效力,核心法律边界清晰明确:不改变CGT产品由国家药监局(NMPA)统一注册审批的权限与流程,不突破医疗技术临床应用的监管规则,不豁免人类遗传资源、数据合规、伦理审查的法定强制要求。
对市场主体而言,其核心价值在于研发资源优化与产业协同,最适配处于早期研发、Pre-IND阶段的创新型企业,以及企业总部、研发中心、生产基地的落地布局,能够有效缩短研发准备周期,降低早期投入成本,但无法为企业提供监管豁免或审批捷径。
二、乐城先行区:特许试点下的监管创新与法律边界
(一)核心定位:国务院授权下的区域监管例外与先行先试
乐城先行区的制度创新,核心依据是国务院批复的先行区建设方案、《海南自由贸易港博鳌乐城国际医疗旅游先行区条例》等上位法授权,属于法定范围内的区域监管例外机制,具备突破部分现行监管规则的法律效力,核心目标是推动前沿医疗技术的临床可及性提升与监管规则探索。其核心制度创新集中在四个维度:
特许医疗准入机制。允许先行区内具备资质的医疗机构,针对国内无有效治疗手段的临床急需疾病,引进使用已在境外获批上市、或处于关键临床试验阶段的CGT产品,无需先行完成国内上市注册,大幅缩短前沿疗法的国内临床可及周期。 真实世界数据(RWD)应用试点。作为国内首个国家级真实世界数据应用试点,先行区内特许使用CGT产品积累的真实世界数据,可依法用于支持产品的国内注册申报,为企业缩短上市周期、降低临床试验成本提供了全新路径。 全流程闭环监管体系。针对细胞治疗的高风险特征,出台专项管理规定、操作流程、伦理审查指南等制度文件,构建“机构准入-项目审批-伦理审查-临床应用-风险管控”的全流程闭环监管体系,实现先行先试与风险可控的平衡。 跨境要素流动便利化。依托海南自贸港政策优势,在CGT相关的跨境医疗合作、境外医师执业、药品器械进口、跨境资金流动等方面设置便利化措施,支持国际前沿CGT技术的引进与临床应用。
(二)法律边界与适用场景
乐城先行区的监管突破是法定授权下的有限例外,并非无边界的监管豁免,核心法律边界清晰:适用范围仅限乐城先行区范围内具备相应资质的医疗机构,特许使用的CGT产品仅限在区内用于符合条件的患者,不得带出区域外使用,也不得面向全国开展商业化推广;特许准入不替代法定的上市注册程序,产品若要全国上市销售,仍需完成完整的NDA审批流程;区内开展相关业务的机构需承担更高的合规义务与风险管控责任,违规将面临更为严格的处罚。
对市场主体而言,其核心价值在于前沿管线的国内早期临床布局、监管规则探索、真实世界数据积累,最适配三类场景:境外已进入临床后期或获批上市的成熟管线、个体化基因编辑等监管规则尚不明确的前沿技术、罕见病等难以开展大样本随机对照临床试验的产品。
三、CGT领域现行监管框架与核心合规风险
(一)二元监管框架的核心法律区分
我国当前针对CGT技术,形成了药品注册路径与医疗技术临床应用路径并行的二元监管框架,二者的监管主体、合规要求、法律后果存在本质差异,是企业开展研发与转化必须厘清的底层逻辑。
药品注册路径(IND-NDA路径)。由NMPA统一监管,以《药品管理法》《药品注册管理办法》为核心上位法,适用于按治疗用生物制品管理的体细胞治疗、基因治疗、溶瘤病毒等产品。企业作为上市许可持有人(MAH),需完成IND申请、临床试验审批、Ⅰ-Ⅲ期临床试验、NDA注册审批全流程,取得药品注册证书后,方可在全国范围内开展商业化生产与销售,是CGT产品实现全国商业化的唯一法定路径。 医疗技术临床应用路径。由国家卫健委统一监管,以《医疗技术临床应用管理办法》为核心,将体细胞治疗纳入限制类医疗技术管理,仅限具备相应资质的医疗机构在本机构内开展临床研究与应用,不得产业化生产、不得向其他机构推广、不得商业化销售,仅适用于医疗机构内的个体化临床应用,无法实现全国商业化上市。
(二)全流程核心合规风险点
IIT与IND路径混用风险。这是行业内最高发的合规风险。IIT由医疗机构/研究者主导,核心目的是探索性科学研究,无需NMPA审批,研究数据不得直接作为药品注册申报的核心证据,严禁向患者收取治疗费用或变相商业化;IND注册临床试验由企业主导,核心目的是药品注册申报,需取得NMPA临床试验默示许可,严格遵循GCP规范,试验数据是注册审批的核心法定依据。常见违规情形包括:以IIT替代注册临床试验、在IIT中向患者收取治疗费用、将IIT数据直接用于注册申报,上述行为将面临行政处罚,情节严重的可能构成刑事犯罪。 人类遗传资源合规风险。CGT研发与临床研究全程涉及我国人类遗传资源的采集、保藏、利用与对外提供,是《人类遗传资源管理条例》的重点监管领域。核心风险包括:开展国际合作临床试验未取得科技部审批、未经审批向境外机构提供人类遗传资源信息、采集保藏人类遗传资源未履行备案程序、中外合作研发成果归属未保障中方合法权益,违规将面临责令停止违法行为、高额罚款、禁止开展相关活动等处罚。 伦理审查与知情同意风险。CGT属于高风险生命科学研究,对伦理审查与知情同意的要求远高于常规医疗技术。核心风险包括:未通过伦理委员会审查即开展研究、研究方案重大变更未重新履行伦理审查程序、知情同意未充分告知技术的高风险性与潜在远期风险、违规开展可遗传的人类生殖细胞基因编辑研究,违规将面临行政处罚,造成患者损害的需承担民事赔偿责任,情节严重的将依法追究刑事责任。 数据合规与隐私保护风险。CGT研发涉及的患者基因信息属于敏感个人信息,核心风险包括:数据采集未取得个人单独明确的知情同意、超范围超目的使用个人信息、数据安全保护措施不到位导致泄露、敏感个人信息处理未履行《个人信息保护法》规定的特殊保护义务,违规将面临网信部门的高额罚款、责令暂停相关业务等行政处罚。
四、CGT领域知识产权归属与商业化路径合规安排
(一)核心知识产权合规要点
CGT产业的创新高度依赖产学研协同,知识产权归属与权益分配是行业合作纠纷的高发领域,核心合规要点集中在三个场景:
产学研合作中的知识产权归属。合作各方应在合作开展前签订书面合同,明确约定知识产权的申请权与所有权归属、专利申请义务与费用承担、实施许可与收益分配方式、后续改进成果的归属与使用规则;针对利用我国人类遗传资源完成的合作研发,需严格遵循相关法规要求,保障中方合作单位对成果的共同所有权,不得通过合同约定将知识产权独家归属境外机构。 IIT临床研究中的数据与知识产权分配。企业与医疗机构应在合作协议中明确约定,临床研究原始数据的所有权归属医疗机构,企业享有符合法律法规要求的、用于技术研发与专利申请的使用权;针对基于临床研究数据产生的新技术成果,明确约定知识产权归属与商业化收益分配方式,同时明确数据使用的范围、保密义务与出境限制。 跨境技术引进的知识产权合规。技术引进前需开展全面的知识产权尽职调查,核实许可方的专利权属、有效性与保护范围,排查专利侵权风险;在许可协议中明确约定许可类型、地域范围、使用场景、后续改进成果归属、侵权责任承担方式;涉及人类遗传资源合作研发的,严格履行法定的审批备案程序。
(二)商业化路径的合规安排
药品注册上市路径。这是CGT产品实现全国商业化的唯一法定路径。企业需围绕核心技术构建完善的专利保护体系,严格遵循GCP规范开展临床试验,提前搭建符合GMP要求的生产质量管理体系,上市后履行MAH全生命周期管理义务,推进医保准入与市场推广。 医疗技术临床应用路径。仅限具备资质的医疗机构在本机构内开展个体化体细胞治疗应用,需完成技术备案与伦理审查,建立完善的医疗质量控制体系,不得产业化、商业化推广;若需实现产业化上市,必须完整履行药品注册审批程序。 乐城特许应用到注册上市的转化路径。企业需严格遵循乐城先行区特许准入规定开展区内临床应用,提前制定符合监管要求的真实世界数据研究方案,同步推进全国范围内的IND申请与临床试验,以真实世界数据作为补充证据加快上市审批,最终通过NDA注册实现全国商业化。
五、企业路径选择的核心合规考量
两大路径并非非此即彼的互斥关系,企业可根据自身发展阶段、管线特征、战略布局进行组合适配,路径选择的核心合规考量集中在四个维度:
管线研发阶段与技术特征。处于早期研发、Pre-IND阶段的通用型CGT产品,优先选择深圳路径完成研发、中试与临床试验准备;临床后期、境外已获批的成熟管线,或监管规则尚不明确的前沿技术,适配乐城先行区路径开展早期临床布局。 合规能力与风险承受力。乐城先行区路径在提升临床转化效率的同时,对企业的全流程合规管控、风险处置能力提出了更高要求,更适合具备完善合规体系的成熟企业;初创企业、早期研发阶段的企业,优先选择深圳路径,在合规框架内完成研发能力与合规体系建设。 注册申报的证据策略。计划以大样本随机对照临床试验作为注册申报核心证据的,优先选择深圳等临床资源丰富的区域开展试验;针对罕见病、难治性疾病等难以开展大样本试验的产品,可选择乐城先行区路径,提前布局真实世界数据积累。 国际化布局需求。计划引进境外前沿管线、开展跨境合作的企业,可结合深圳前海的跨境要素流动政策与乐城先行区的特许准入政策,形成“前海跨境合作+乐城临床应用”的协同布局,加快境外管线的国内转化。
结语
深圳与乐城代表的两类地方实践,形成了“产业筑基+试点探路”的互补格局,共同推动我国CGT产业的创新发展与监管体系完善。对行业主体而言,地方制度创新的核心价值,绝非监管套利的空间,而是合规框架内加快研发转化、优化管线布局的窗口期。
CGT作为生命科学领域的战略赛道,其核心竞争力从来不止于技术层面的突破,更在于全流程的合规体系建设、知识产权布局与风险管控能力。企业唯有厘清不同路径的法律边界,构建“技术创新+合规管控+知识产权”三位一体的发展体系,才能在产业快速发展的浪潮中,实现创新与合规的平衡,在不确定的监管环境中,建立确定性的发展逻辑。
END

免责声明:本文及其内容仅用作交流,不代表本文作者出具的法律意见或决策。本文或可能引用或参考过其它第三方文章,如有侵权,请联系作者修改或删除。未经允许,禁止转载。
往期推荐
