香港中文大学唐本忠、深圳大学韩婷、河南大学王杰菲、师冰洋Science Advances!!超大斯托克斯位移引领脑部疾病治疗新范式
- 2026-03-31 20:13:46
医学研究前沿——聚焦医学前沿研究进展。100多万医学领域硕博医生们订阅的微信公众号。点击标题下蓝字“医学研究前沿”关注,我们将为您提供最有价值、最前沿的医学前沿资讯。

胶质母细胞瘤作为一种高度侵袭性的中枢神经系统肿瘤,其治疗面临严峻挑战,主要源于肿瘤边界识别困难导致的切除不彻底和复发率高。当前,手术切除是临床主要手段,但缺乏高灵敏度、实时的术中成像技术限制了治疗效果。近红外二区荧光成像技术因其卓越的组织穿透能力、低自发荧光干扰和最小光毒性,成为精准手术导航和深部肿瘤光疗的理想工具。然而,现有近红外二区探针普遍存在斯托克斯位移小、聚集态发光性能差及合成复杂等问题,难以满足临床需求。香港中文大学唐本忠团队联合多家机构,在《Science Advances》上发表研究,通过创新分子设计开发出新型近红外探针TNQ2,该探针具备超大斯托克斯位移和高效聚集诱导发光特性,为胶质瘤的精准诊疗提供了新思路。本研究不仅解决了传统探针的荧光猝灭难题,还通过纳米工程策略实现了探针的自组装优化,显著提升了成像灵敏度和治疗效率,为脑部疾病的光学诊疗奠定了技术基础。
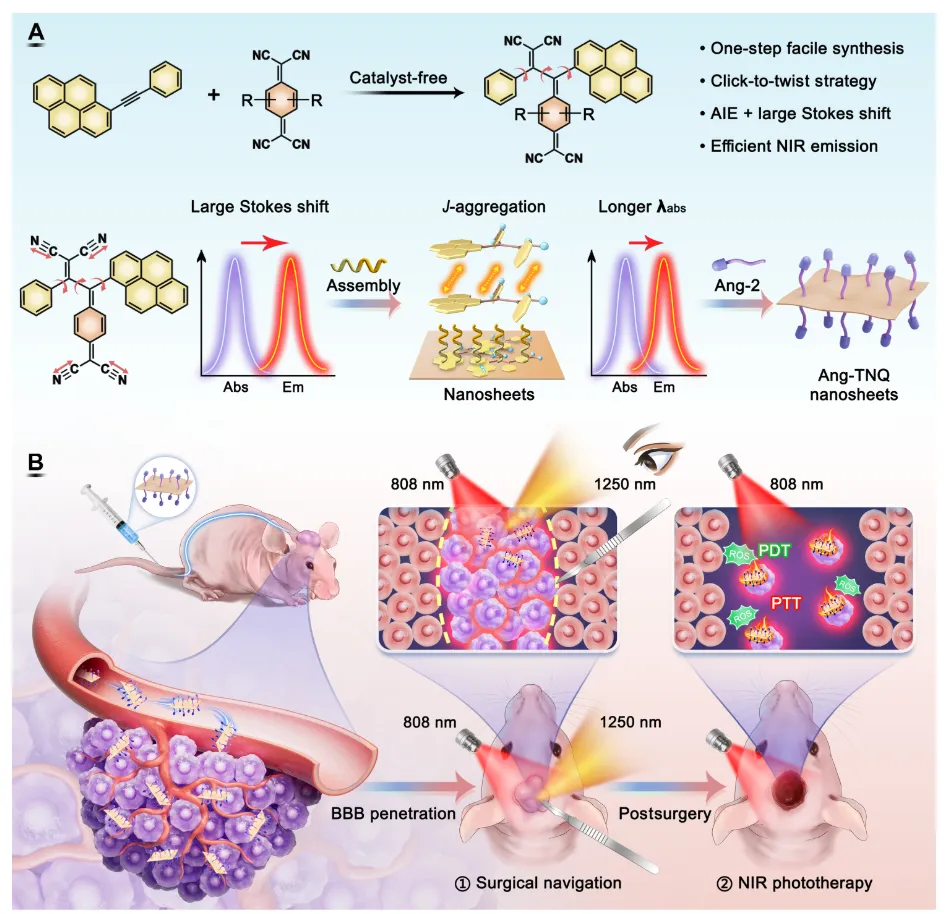
研究团队采用简便的一步点击反应合成了一种基于四氰基喹啉并二甲烷衍生的近红外探针TNQ2,该设计通过炔烃与缺电子试剂的环加成-逆电环化反应,将平面分子转化为高度扭曲结构,从而突破基于TCNQ发色团的非荧光性限制。TNQ2表现出前所未有的445纳米斯托克斯位移,覆盖可见光至近红外二区波段,并具备优异的抗荧光猝灭能力。通过可控自组装过程,TNQ2进一步形成尺寸约160纳米的二维矩形纳米片,在组装体中构建J-聚集体结构,使其吸收峰红移至725纳米,发射波长延伸至1000纳米附近,实现了聚集增强发光效应。这种纳米结构不仅提升了光子吸收和利用效率,还平衡了荧光成像、光热治疗和光动力治疗功能。经Angiopep-2肽修饰后,探针展现出良好的血脑屏障穿透性和肿瘤靶向能力,支持高灵敏度成像引导的手术切除。在808纳米激光照射下,探针可同步产生荧光信号、热量和活性氧,通过光热与光动力协同作用清除残留肿瘤细胞,为术后治疗提供保障。
在动物模型实验中,TNQ2基纳米诊疗系统实现了近红外二区荧光成像引导的胶质瘤精准切除,并有效执行术后光疗,显著延长了原位胶质瘤模型小鼠的生存期。研究结果表明,该探针的辐射与非辐射过程调控优化了诊疗效果,其超大斯托克斯位移减少了激发与发射串扰,而二维纳米片结构增强了组织穿透性和治疗精度。这一集成策略将分子设计与纳米工程相结合,克服了传统二维材料制备中的尺寸大、穿透性差等局限,为脑部疾病诊疗提供了可定制平台。该工作不仅证实了近红外二区探针在胶质瘤治疗中的实用性,还建立了一种变革性范式,有望推广至其他中枢神经系统疾病的研究。未来,基于此类探针的进一步优化可促进临床转化,推动精准医学发展。



说明:
🔹本文仅作科研人员学术交流。
🔹本文内容若存在版权问题,请联系我们及时处理。
🔹欢迎广大读者对本文进行转发宣传。
🔹《医学研究前沿》会不断提升自身水平,为读者分享更加优质的材料研究成果解读,欢迎关注我们。
欢迎广大科研工作者投稿最新研究成果。
