广州妇女儿童医疗中心 | 融合血小板 - 中性粒细胞膜的智能纳米粒,破解急性肺损伤治疗难题
- 2026-03-12 18:37:10

导读
针对急性肺损伤(ALI)缺乏特效治疗、现有药物靶向性差且生物利用度低的问题,设计了负载表没食子儿茶素没食子酸酯(EGCG)的巯基酮(TK)功能化介孔硅纳米粒(MSN),并包裹血小板 - 中性粒细胞混合膜(PNM)构建 PNM-EGCG@MSN-TK 纳米颗粒;该颗粒借助混合膜实现炎症部位靶向与免疫逃逸,通过 TK 键响应高活性氧(ROS)释放 EGCG,既清除过量 ROS 缓解氧化应激,又激活 MAPK/BNIP3 通路增强肺上皮细胞自噬,同时降低促炎细胞因子水平,最终在体内外实验中有效改善 ALI,为 ALI 治疗提供了兼具靶向性、抗氧化和抗炎功效的新型策略。
研究亮点
本研究构建的 PNM-EGCG@MSN-TK 纳米颗粒具有双重炎症靶向与免疫逃逸能力,创新采用血小板 - 中性粒细胞混合膜包裹,强化炎症部位靶向性;TK 键修饰实现 ROS 响应型药物释放,提升 EGCG 生物利用度;同步发挥 ROS 清除、抗炎作用,通过激活 MAPK/BNIP3 通路增强自噬,多机制协同改善 ALI;体内外实验证实其生物相容性良好、治疗效果显著,为 ALI 治疗提供了新型高效的纳米治疗平台。
全文归纳总结


研究方法
纳米颗粒制备与表征:通过梯度离心分离血小板和中性粒细胞,制备混合膜(PNM);采用溶胶 - 凝胶法合成 MSN,经胺功能化后负载 EGCG,结合 TK 键修饰得到 EGCG@MSN-TK,再与 PNM 混合经超声、挤压制备 PNM-EGCG@MSN-TK;利用 TEM、HAADF-STEM、DLS、UV-vis 等表征形貌、粒径、元素分布及药物负载效率,通过 Western blot 验证膜蛋白标记。
生物相容性评估:采用 CCK8 法检测 MLE12 细胞活力,流式细胞术检测细胞凋亡;对小鼠尾静脉注射纳米颗粒,监测体重变化,进行血常规分析,通过 H&E 染色观察心、肝、脾、肺、肾组织损伤情况。
靶向性与 ROS 清除实验:体外以 H₂O₂诱导 MLE12 细胞,体内以 LPS 诱导 ALI 小鼠模型,采用荧光标记观察纳米颗粒细胞摄取与体内靶向分布;DCFH 探针检测细胞内 ROS 水平,RT-qPCR 检测促炎细胞因子(TNF-α、IL-1β、IL-6)mRNA 表达。
自噬与机制探究:TEM 观察自噬体数量,免疫荧光与 Western blot 检测自噬相关蛋白(LC3、Beclin-1、P62)及凋亡相关蛋白(Bax、Bcl-2)表达;检测 BNIP3 及 MAPK 通路蛋白(p-P38、P38)表达,明确作用机制。
体内治疗效果验证:LPS 诱导小鼠 ALI 模型,尾静脉注射纳米颗粒,通过 H&E 染色评估肺组织病理损伤,TUNEL assay 检测细胞凋亡,免疫荧光与 Western blot 验证自噬相关机制,RT-qPCR 与免疫组化检测炎症因子水平。
研究结果
成功制备 PNM-EGCG@MSN-TK 纳米颗粒,平均粒径约 122 nm,EGCG 负载效率 24.2%,表面存在血小板和中性粒细胞特征膜蛋白,具有 H₂O₂依赖的药物释放特性。
该纳米颗粒生物相容性良好,对 MLE12 细胞无明显细胞毒性,不诱导凋亡;小鼠注射后体重、血常规无异常,主要脏器无病理损伤。
靶向性显著,体外对 H₂O₂诱导的 MLE12 细胞摄取率高于单一细胞膜包裹纳米颗粒,体内在 ALI 小鼠肺部荧光信号最强;ROS 清除能力优异,可显著降低细胞内 ROS 水平,下调 TNF-α、IL-1β、IL-6 表达。
能显著增强 H₂O₂诱导的 MLE12 细胞自噬,增加自噬体数量及 LC3、Beclin-1 表达,降低 P62 水平,抑制细胞凋亡;通过上调 BNIP3 表达及激活 P38 MAPK 通路调控自噬。
体内实验中,该纳米颗粒可显著缓解 LPS 诱导的小鼠肺组织病理损伤,减少细胞凋亡,增强肺组织自噬,降低炎症因子水平,治疗效果优于 EGCG@MSN-TK。
研究结论
本研究成功构建了炎症响应型仿生纳米颗粒 PNM-EGCG@MSN-TK,其通过血小板 - 中性粒细胞混合膜实现炎症部位精准靶向与免疫逃逸,TK 键修饰赋予 ROS 响应型 EGCG 释放功能,有效提升药物生物利用度。该纳米颗粒不仅能高效清除细胞内过量 ROS、抑制炎症因子释放,还可通过激活 MAPK/BNIP3 通路增强肺上皮细胞自噬,抑制细胞凋亡,多机制协同维持细胞稳态、减轻肺组织损伤。体内外实验均证实其生物相容性良好、治疗效果显著,为急性肺损伤提供了一种兼具靶向性、智能释放和多效协同治疗的新型策略,具有重要的临床应用潜力。
局限性:研究聚焦 ROS 调控与自噬诱导,纳米颗粒与炎症反应中其他分子通路的相互作用机制尚未明确。展望:未来需进一步探究该纳米颗粒与其他细胞通路的交叉作用,完善作用机制;优化纳米颗粒的制备工艺与药物负载效率,开展长期毒性研究,为其临床转化提供更全面的实验依据。
结果图解


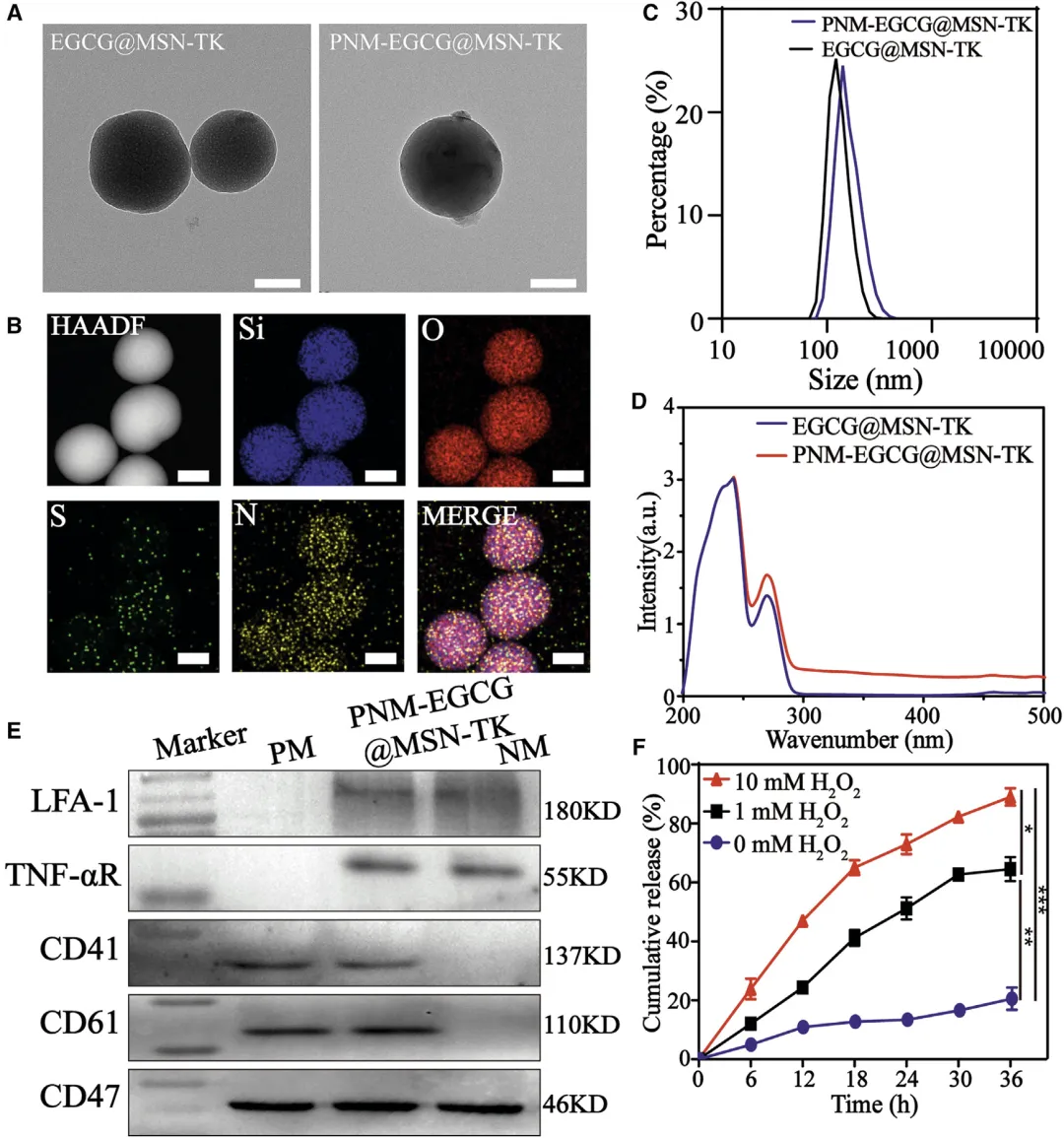 Figure 1:PNM-EGCG@MSN-TK 纳米颗粒的制备与核心特性验证
Figure 1:PNM-EGCG@MSN-TK 纳米颗粒的制备与核心特性验证
该图通过多种表征手段证实了 PNM-EGCG@MSN-TK 纳米颗粒的成功制备及关键功能特性。TEM 观察显示血小板 - 中性粒细胞混合膜(PNM)已成功包裹在 EGCG@MSN-TK 表面,形成了预期的核壳结构;元素 mapping 结果检测到 Si、O、N、S 等特征元素的均匀分布,印证了 EGCG 和 mPEG-TK 在纳米颗粒中的有效负载。DLS 测试表明该纳米颗粒平均粒径约为 122 nm,符合纳米药物递送系统的尺寸要求;UV-vis 光谱证实 EGCG 成功载入介孔硅(MSN),负载效率达 24.2%。Western blot 检测到血小板和中性粒细胞的特征膜蛋白(如 LFA-1、CD41、CD61 等)在纳米颗粒表面表达,进一步验证了混合膜的成功包覆;药物释放实验则显示,该纳米颗粒的 EGCG 释放具有显著的 H₂O₂浓度依赖性,高 H₂O₂环境下(模拟炎症部位氧化应激状态)释放效率显著提升,这一特性为其在炎症部位的智能药物释放提供了支撑。
Figure 2:PNM-EGCG@MSN-TK 纳米颗粒的生物相容性评估
该图通过体内外实验系统验证了 PNM-EGCG@MSN-TK 纳米颗粒的生物安全性。体外细胞实验中,CCK8 法检测显示经该纳米颗粒处理的 MLE12 细胞活力与正常细胞无显著差异,流式细胞术也未检测到明显的细胞凋亡现象,表明其无明显细胞毒性。体内实验中,对小鼠尾静脉注射纳米颗粒后,7 天内实验组与对照组小鼠的体重变化无显著差异;血常规分析显示红细胞、白细胞、中性粒细胞等指标均未出现异常波动;H&E 染色结果显示小鼠的心、肝、脾、肺、肾等主要脏器均未出现明显病理损伤。这些结果共同表明,PNM-EGCG@MSN-TK 纳米颗粒具有良好的生物相容性,为其后续的体内治疗应用奠定了安全基础。
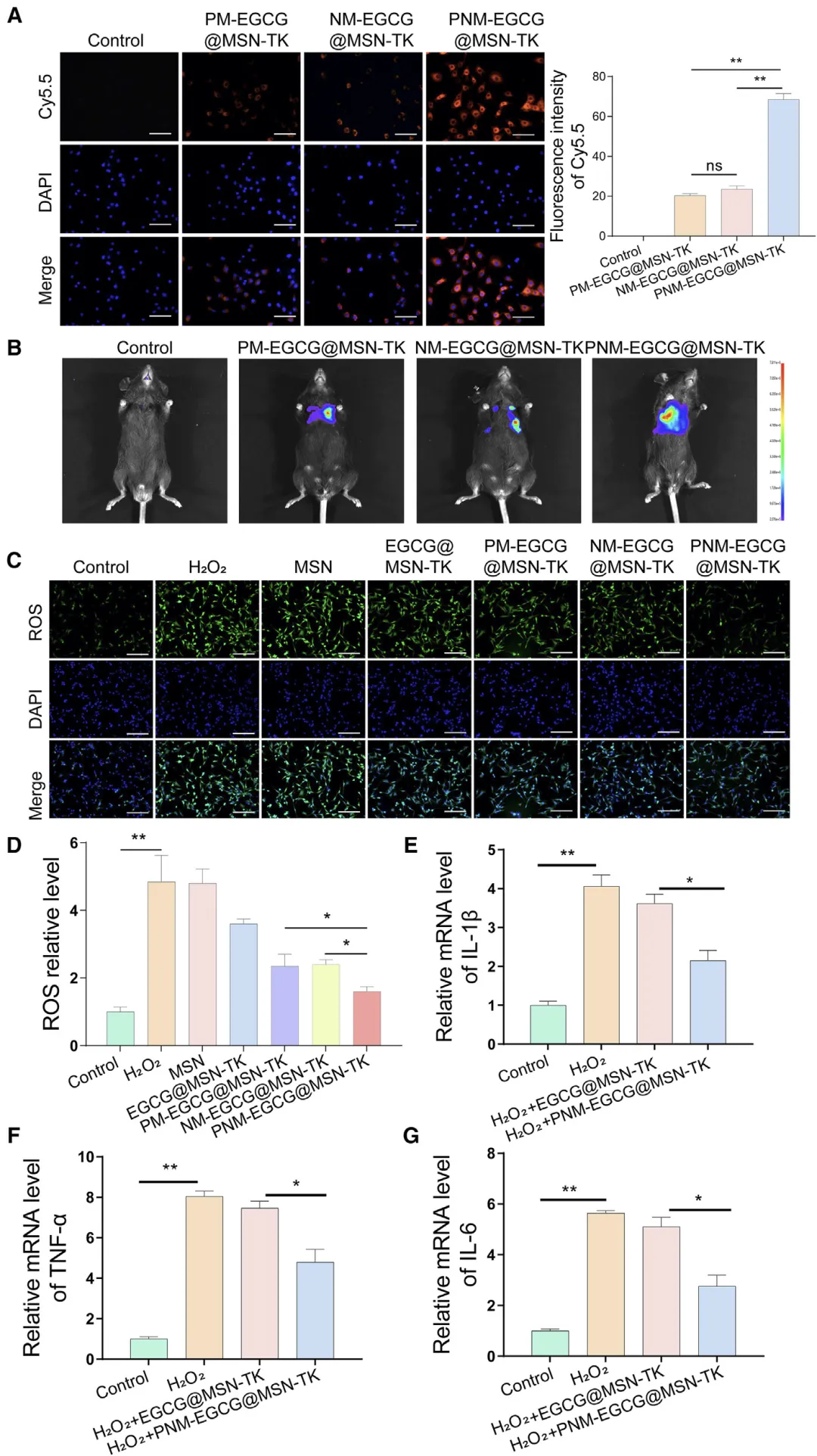
Figure 3:PNM-EGCG@MSN-TK 纳米颗粒的靶向性与 ROS 清除及抗炎能力验证
该图聚焦于纳米颗粒的核心治疗相关功能,证实了其优异的炎症部位靶向性、ROS 清除能力及抗炎效果。靶向性实验中,体外对 H₂O₂诱导的 MLE12 细胞(模拟炎症状态肺上皮细胞)的摄取实验显示,PNM 包裹的纳米颗粒荧光强度显著高于单一细胞膜包裹的纳米颗粒,表明混合膜增强了细胞靶向结合能力;体内活体成像显示,注射 PNM-EGCG@MSN-TK 的小鼠肺部荧光信号最强,证实其在 ALI 模型小鼠体内具有良好的肺组织靶向性。ROS 清除实验中,DCFH 探针检测显示,与单纯 MSN 相比,EGCG@MSN-TK、PM-EGCG@MSN-TK、NM-EGCG@MSN-TK 及 PNM-EGCG@MSN-TK 均具有 ROS 清除能力,其中 PNM-EGCG@MSN-TK 的清除效果最为显著,可有效缓解细胞内氧化应激。此外,RT-qPCR 检测显示该纳米颗粒能显著降低 H₂O₂诱导的 MLE12 细胞中 TNF-α、IL-1β、IL-6 等促炎细胞因子的 mRNA 表达水平,证实其具有明确的抗炎作用。
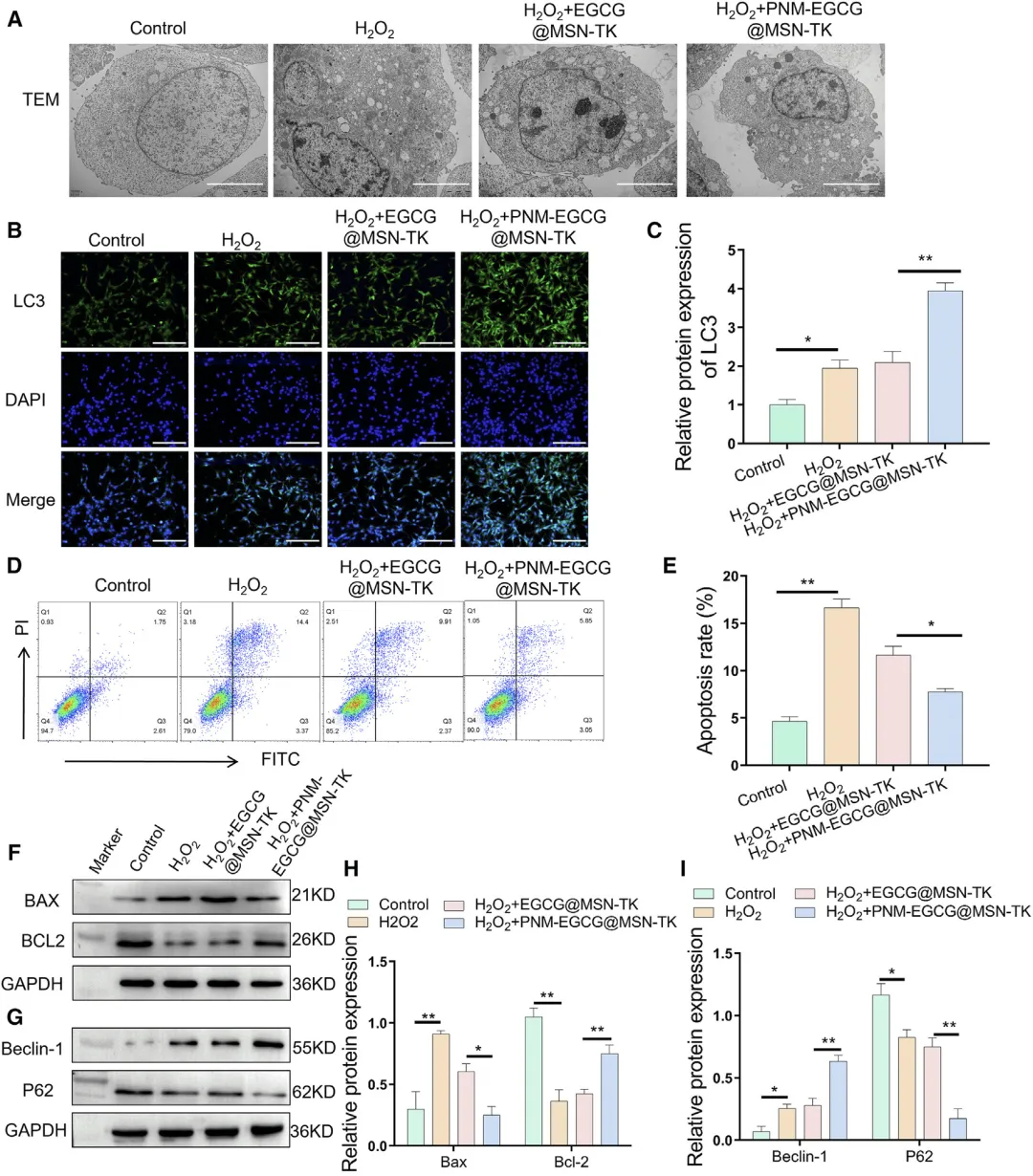
Figure 4:PNM-EGCG@MSN-TK 纳米颗粒对 H₂O₂诱导的 MLE12 细胞自噬增强与凋亡抑制作用
该图通过一系列细胞实验揭示了 PNM-EGCG@MSN-TK 纳米颗粒通过增强自噬、抑制凋亡保护肺上皮细胞的机制。TEM 观察显示,经该纳米颗粒处理的 H₂O₂损伤 MLE12 细胞中,自噬体数量显著多于 EGCG@MSN-TK 处理组及对照组;免疫荧光和 Western blot 检测进一步证实,自噬相关蛋白 LC3 和 Beclin-1 的表达水平显著升高,而自噬底物蛋白 P62 的表达水平显著降低,表明该纳米颗粒能有效增强损伤肺上皮细胞的自噬活性。同时,流式细胞术检测显示,PNM-EGCG@MSN-TK 处理可显著降低 H₂O₂诱导的 MLE12 细胞凋亡率;Western blot 检测显示凋亡相关蛋白 Bax 的表达被显著抑制,而抗凋亡蛋白 Bcl-2 的表达显著上调。这些结果表明,PNM-EGCG@MSN-TK 纳米颗粒可通过增强自噬、抑制凋亡两种途径,维持氧化应激损伤肺上皮细胞的稳态,减轻细胞损伤。
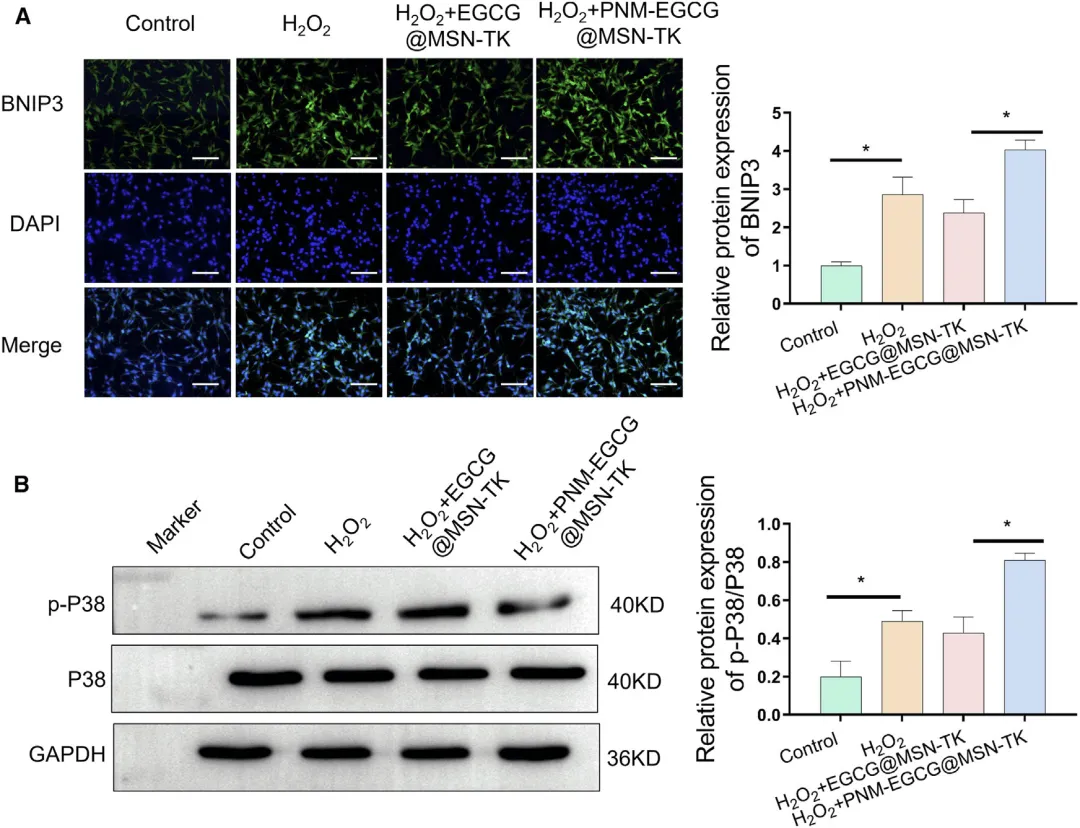
Figure 5:PNM-EGCG@MSN-TK 纳米颗粒通过 MAPK/BNIP3 通路调控自噬的机制验证
该图深入探究了 PNM-EGCG@MSN-TK 纳米颗粒增强细胞自噬的分子机制,证实其通过激活 MAPK/BNIP3 通路发挥作用。免疫荧光检测显示,该纳米颗粒处理后,H₂O₂损伤的 MLE12 细胞中 BNIP3 蛋白的表达水平显著升高,而 BNIP3 作为 Bcl-2 家族成员,可通过竞争性结合 Bcl-2 释放 Beclin-1,进而启动自噬过程。Western blot 检测进一步显示,与对照组和单纯 H₂O₂处理组相比,PNM-EGCG@MSN-TK 处理组中 p-P38 蛋白的磷酸化水平显著上调,而总 P38 蛋白表达无明显变化,表明 MAPK 通路中的 P38 亚型被激活。结合此前自噬相关指标的变化,这些结果共同证实,PNM-EGCG@MSN-TK 纳米颗粒通过激活 P38 MAPK 通路,上调 BNIP3 的表达,进而促进 Beclin-1 介导的自噬激活,最终实现对肺上皮细胞的保护作用。
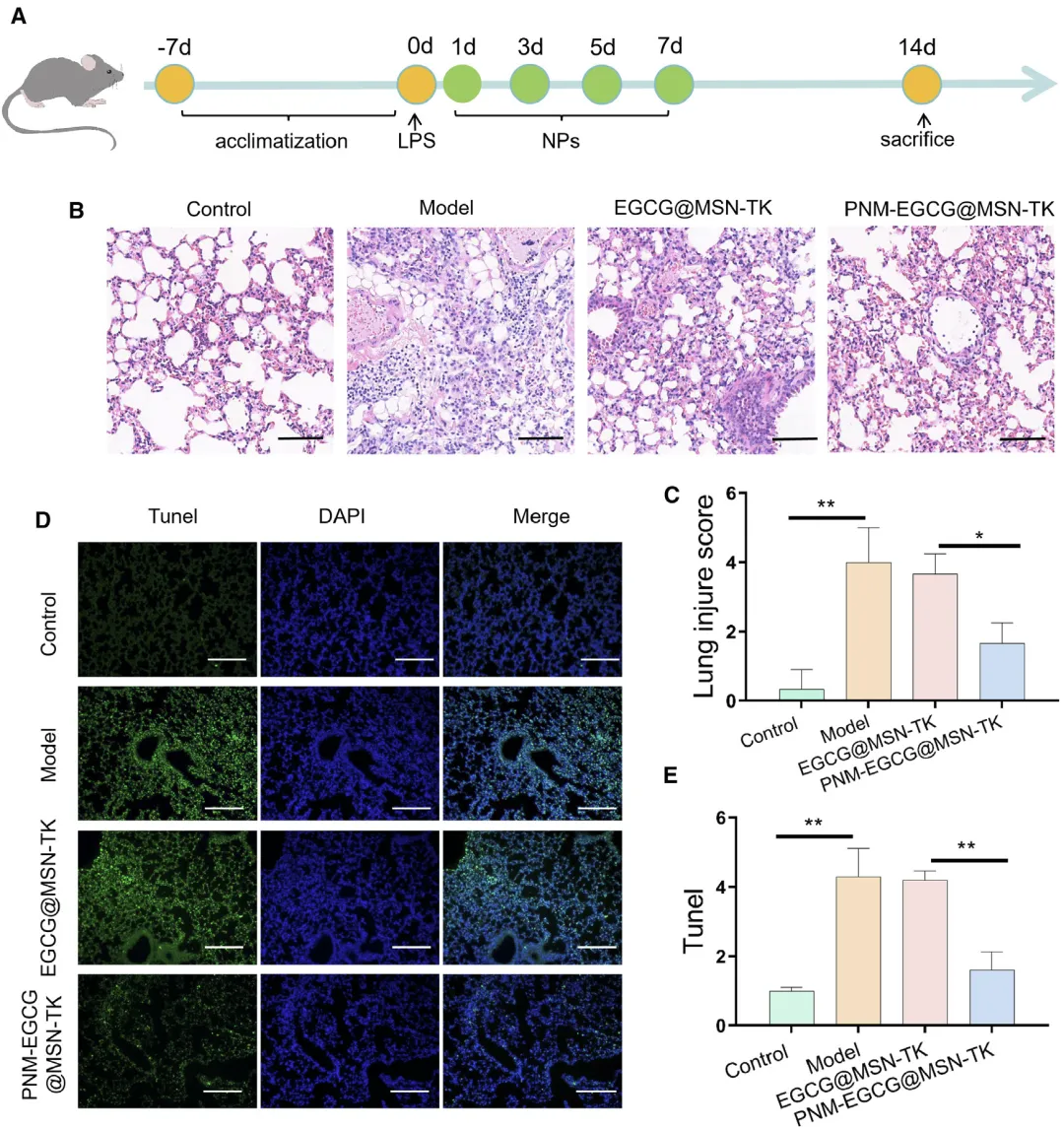
Figure 6:PNM-EGCG@MSN-TK 纳米颗粒在体内缓解 ALI 的治疗效果验证
该图通过 LPS 诱导的 ALI 小鼠模型,验证了 PNM-EGCG@MSN-TK 纳米颗粒的体内治疗效果。实验设计中,小鼠经鼻滴 LPS 建立 ALI 模型后,尾静脉注射纳米颗粒进行治疗,14 天后评估肺组织损伤情况。H&E 染色结果显示,模型组小鼠肺组织出现明显的肺间质增厚、肺泡结构破坏、炎症细胞浸润及出血等典型 ALI 病理特征;而 PNM-EGCG@MSN-TK 处理组的肺组织病理损伤显著减轻,肺泡结构相对完整,炎症浸润明显减少,且治疗效果优于 EGCG@MSN-TK 组。TUNEL 染色结果显示,PNM-EGCG@MSN-TK 处理可显著降低肺组织细胞的凋亡率,与模型组和 EGCG@MSN-TK 组相比,凋亡细胞数量明显减少。这些体内实验结果直接证实,PNM-EGCG@MSN-TK 纳米颗粒能够有效减轻 LPS 诱导的小鼠肺组织损伤,抑制肺细胞凋亡,具有显著的 ALI 治疗效果。
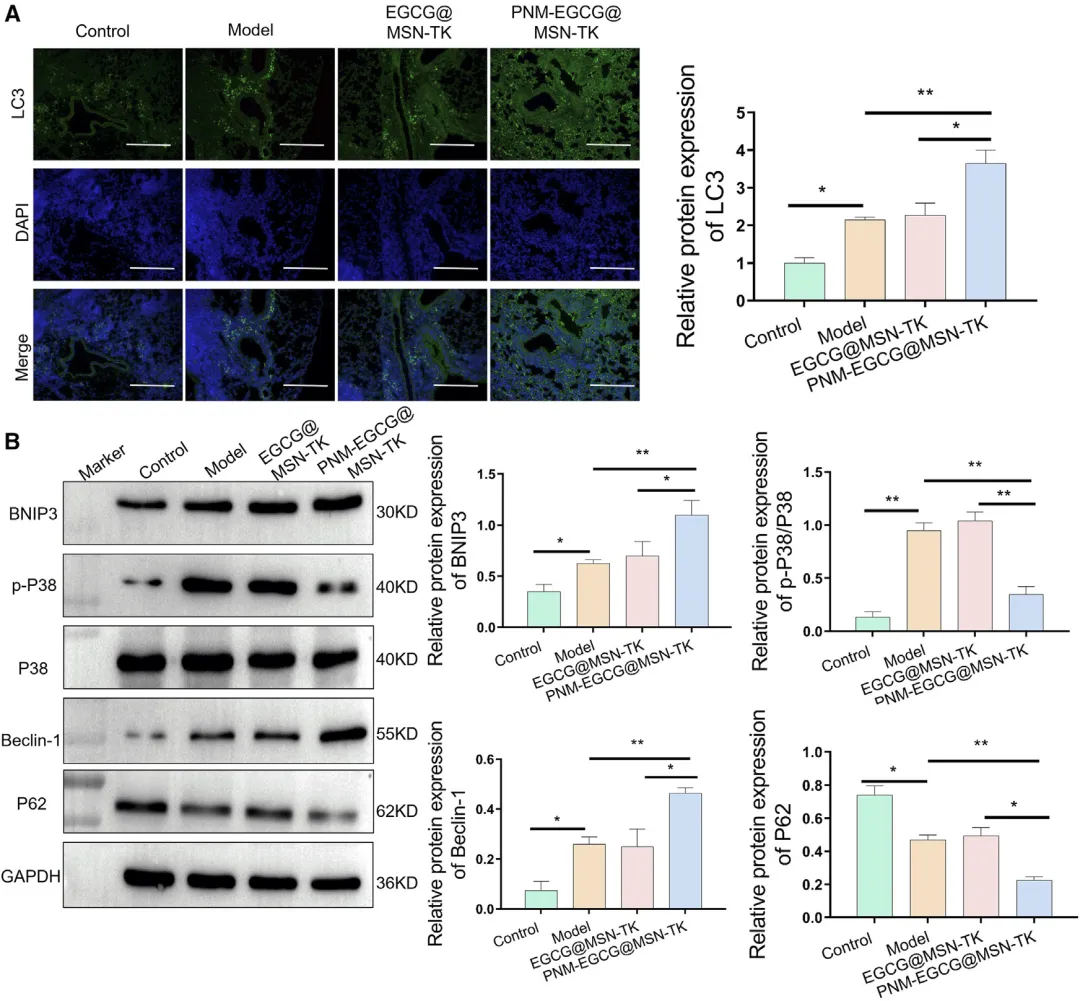
Figure 7:PNM-EGCG@MSN-TK 纳米颗粒在体内通过 MAPK/BNIP3 通路增强自噬的机制验证
该图在体内层面进一步验证了 PNM-EGCG@MSN-TK 纳米颗粒通过激活 MAPK/BNIP3 通路增强自噬,进而发挥 ALI 治疗作用的分子机制。免疫荧光检测显示,与模型组和 EGCG@MSN-TK 组相比,PNM-EGCG@MSN-TK 处理组小鼠肺组织中自噬相关蛋白 LC3 的表达水平显著升高,表明该纳米颗粒在体内可有效增强肺组织的自噬活性。Western blot 检测进一步证实,PNM-EGCG@MSN-TK 处理后,小鼠肺组织中 BNIP3 蛋白表达显著上调,p-P38 蛋白的磷酸化水平明显升高,同时自噬标志蛋白 Beclin-1 表达增加、P62 表达减少,与体外细胞实验结果一致。这些体内机制数据表明,PNM-EGCG@MSN-TK 纳米颗粒在 ALI 小鼠模型中,同样通过激活 P38 MAPK/BNIP3 通路,增强肺组织细胞自噬,从而减轻肺损伤,进一步印证了其治疗机制的一致性。
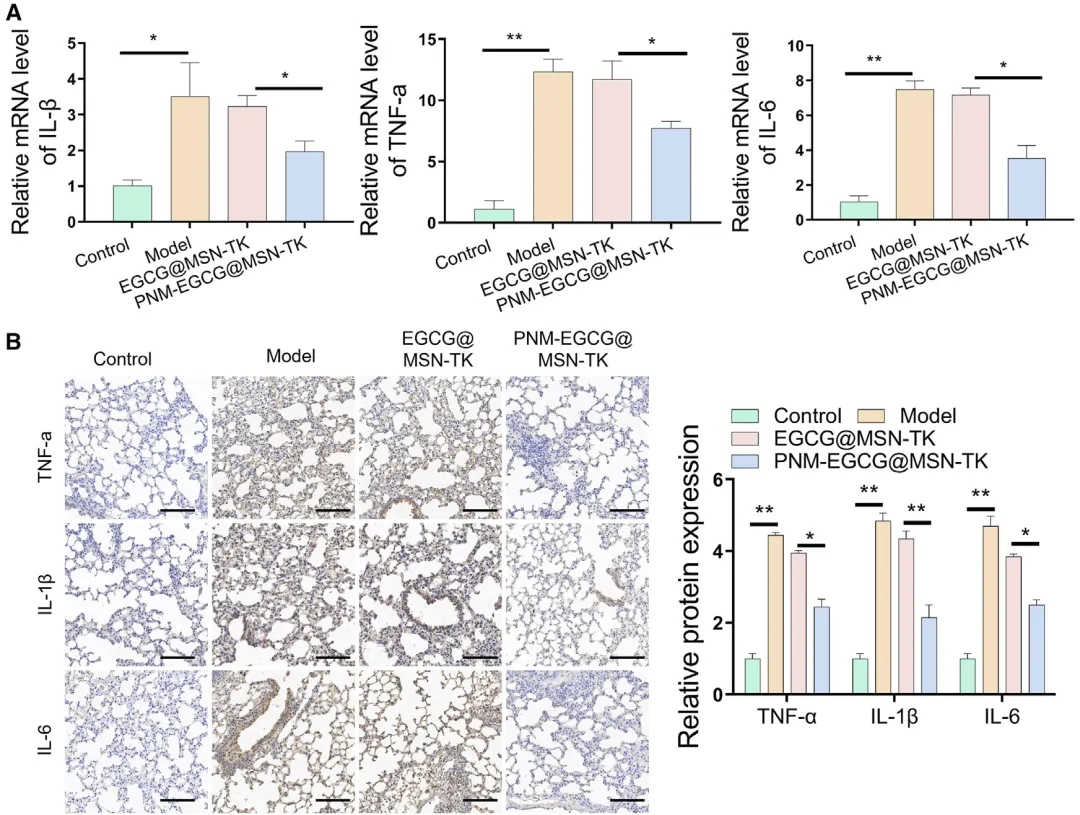
Figure 8:PNM-EGCG@MSN-TK 纳米颗粒在体内降低 ALI 小鼠炎症水平的效果验证
该图专门评估了 PNM-EGCG@MSN-TK 纳米颗粒对 ALI 小鼠体内炎症反应的抑制作用。RT-qPCR 检测显示,与模型组相比,PNM-EGCG@MSN-TK 处理组小鼠肺组织中 TNF-α、IL-1β、IL-6 等促炎细胞因子的 mRNA 表达水平显著降低;免疫组化分析进一步从蛋白水平证实,这些促炎细胞因子在肺组织中的表达量明显减少,且其抗炎效果优于 EGCG@MSN-TK 组。炎症反应过度激活是 ALI 发生发展的核心病理环节,这些结果表明 PNM-EGCG@MSN-TK 纳米颗粒能够有效抑制 ALI 小鼠体内的炎症应答,减少促炎因子释放,这也是其缓解肺组织损伤、发挥治疗作用的重要机制之一。
#急性肺损伤#仿生纳米颗粒#药物递送系统#ROS清除#自噬#MAPK#BNIP3通路#EGCG#炎症靶向

国家杰青一对一答疑视频
医学省自然申请答疑,立项的关键条件是哪一些?从哪些方向可以杀出重围
临床型博士如何准备国青标书?没有预实验怎么办?专家一对一解答规划
