深圳合成生物学创新研究院 | 肺癌脑转移基因组演化重大突破!535 例配对样本揭秘关键规律
- 2026-04-18 21:38:47

1.研究背景
转移是非小细胞肺癌致死主因,约 50% 患者会发生脑转移,血脑屏障使其治疗受限、预后极差。转移是肿瘤进化过程,癌细胞脱离原发灶后在不同器官微环境选择下形成器官亲嗜性转移,但既往研究多采用非配对样本,难以区分转移驱动突变与治疗干扰,且缺乏不同转移部位的平行对比,TRACERx 等大型研究也以淋巴结转移为主,对脑转移的基因组驱动因素、克隆播种模式及演化时间的认知仍不完整。因此亟需大样本配对原发 - 转移队列,系统解析不同部位转移的基因组特征、克隆性与播种时机,明确器官亲嗜性转移的核心决定因素,为临床预警、干预提供理论基础。
2.研究设计
整合公共数据库与自建队列,纳入 223 例 NSCLC 患者 535 对原发 - 转移样本,含脑转移 94 例、颅外远处转移 39 例、淋巴结转移 179 例,设 125 例早期无转移原发灶为对照;采用 TRACERx 统一流程处理全外显子测序数据,鉴定体细胞单核苷酸变异、插入缺失与拷贝数变异,计算肿瘤突变负荷与基因组受影响比例;通过癌症细胞分数区分克隆与亚克隆突变,分析驱动基因突变富集特征;用 Jaccard 相似指数判定单 / 多克隆播种,逆向模型估算转移播种时间;结合进化树与 Dollo 定律分析 LOH 介导的驱动突变丢失,联合转录组数据关联克隆性与基因表达。
3.结果解读
脑转移灶体细胞突变与驱动基因负荷显著高于其他转移部位,原发灶与转移灶驱动突变一致性高;脑转移相关原发灶中PTPRD、FAT1突变显著富集,颅外转移原发灶 TP53 突变富集,提示原发灶突变决定转移器官倾向;吸烟相关突变特征 SBS4 在肿瘤演进中持续衰减,亚克隆与转移阶段贡献降低;脑转移单克隆播种率达 89%,远高于淋巴结转移 41%、颅外转移 49%,且播种时间显著晚于淋巴结转移;首次发现脑、骨转移灶可通过 LOH 丢失原发灶早期克隆驱动突变,涉及 KMT2A、ARID1B 等基因;细胞黏附、迁移相关基因表达差异分别影响多克隆播种与早期转移。
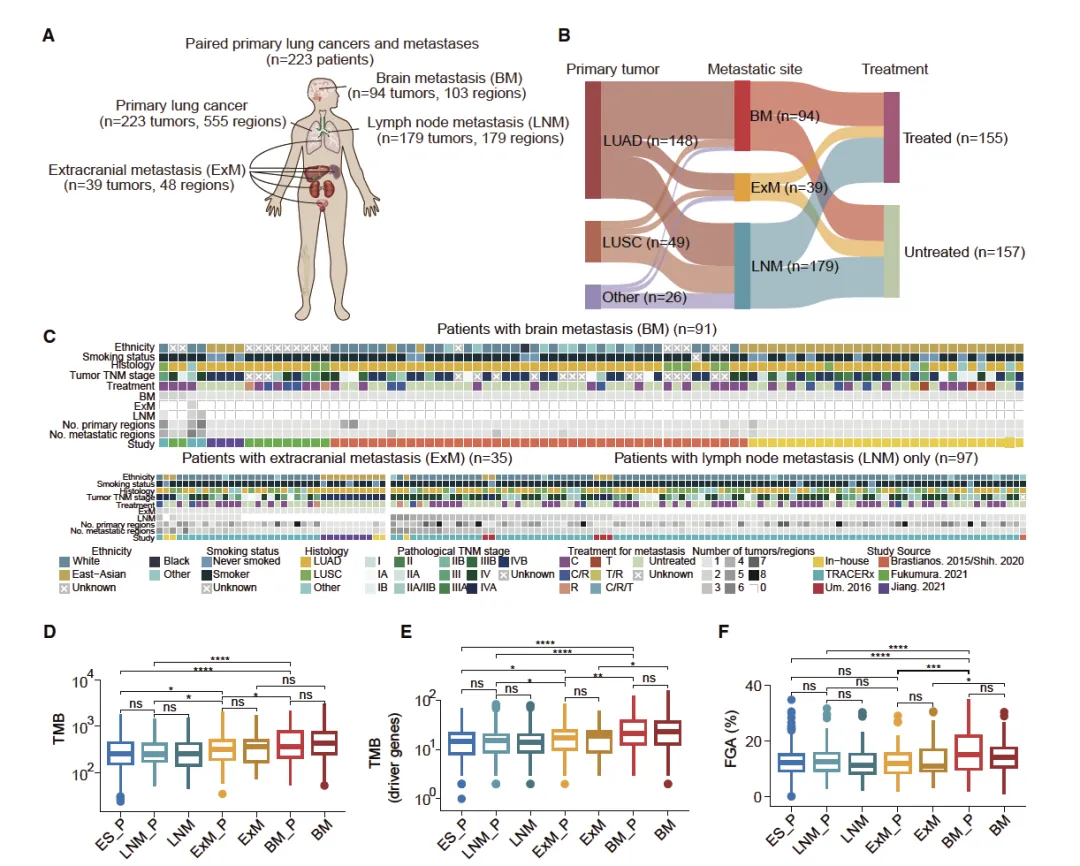
Figure 1 配对 NSCLC 原发 - 转移队列的整体概况与组间突变水平比较
这张图全面展示了本研究构建的非小细胞肺癌原发肿瘤与转移灶配对样本队列的基本情况、患者临床特征,以及不同组别间肿瘤突变负荷、驱动基因突变负荷和基因组拷贝数改变比例的核心差异,首先明确研究纳入 223 例患者、共 535 例肿瘤样本,按转移部位分为脑转移、颅外远处转移、淋巴结转移三个组别,并设置早期无转移原发灶作为对照,同时标注了样本的病理类型、治疗状态、人种、吸烟史等临床信息,随后通过统计检验直观呈现出脑转移相关的原发灶与转移灶,在总体突变数量、驱动基因突变量以及基因组拷贝数变异程度上,都显著高于淋巴结转移、颅外转移组及早期无转移组,而配对的原发灶与转移灶之间整体突变水平保持较高一致性,为后续针对不同部位转移的基因组特征对比分析奠定了可靠的队列基础与初步表型依据。
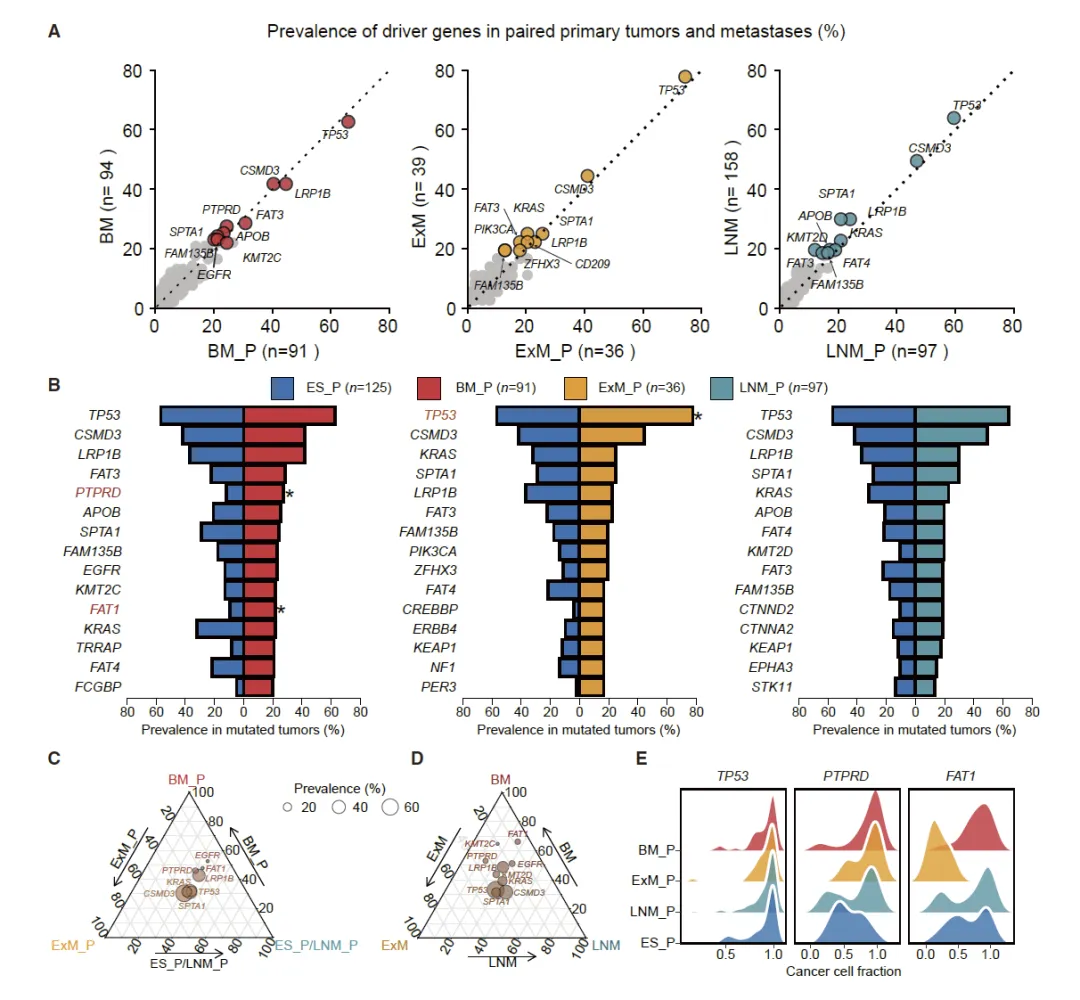
Figure 2 NSCLC 配对原发 - 转移样本的转移驱动基因突变图谱与富集特征
这张图系统解析了非小细胞肺癌原发灶与对应转移灶之间驱动基因突变的分布、频率差异及器官亲嗜性相关的突变富集规律,首先展示了脑转移、颅外转移、淋巴结转移三组配对样本中,高频突变驱动基因在原发灶与转移灶中的突变比例,发现大部分克隆驱动突变在配对样本间高度共享,而脑转移灶拥有更高比例的亚克隆特异性驱动突变,接着通过与早期无转移原发灶对比,筛选出在脑转移原发灶中显著富集的 PTPRD、FAT1 基因,以及颅外转移原发灶中富集的 TP53 基因,进一步通过三元图验证这些基因在不同转移倾向原发灶和转移灶中的特异性分布,同时分析这些器官倾向性驱动突变的癌症细胞分数,发现其在转移相关原发灶中具备更高克隆性,说明这些突变在肿瘤转移起始阶段受到强选择,是推动器官特异性转移的关键原发驱动因素。
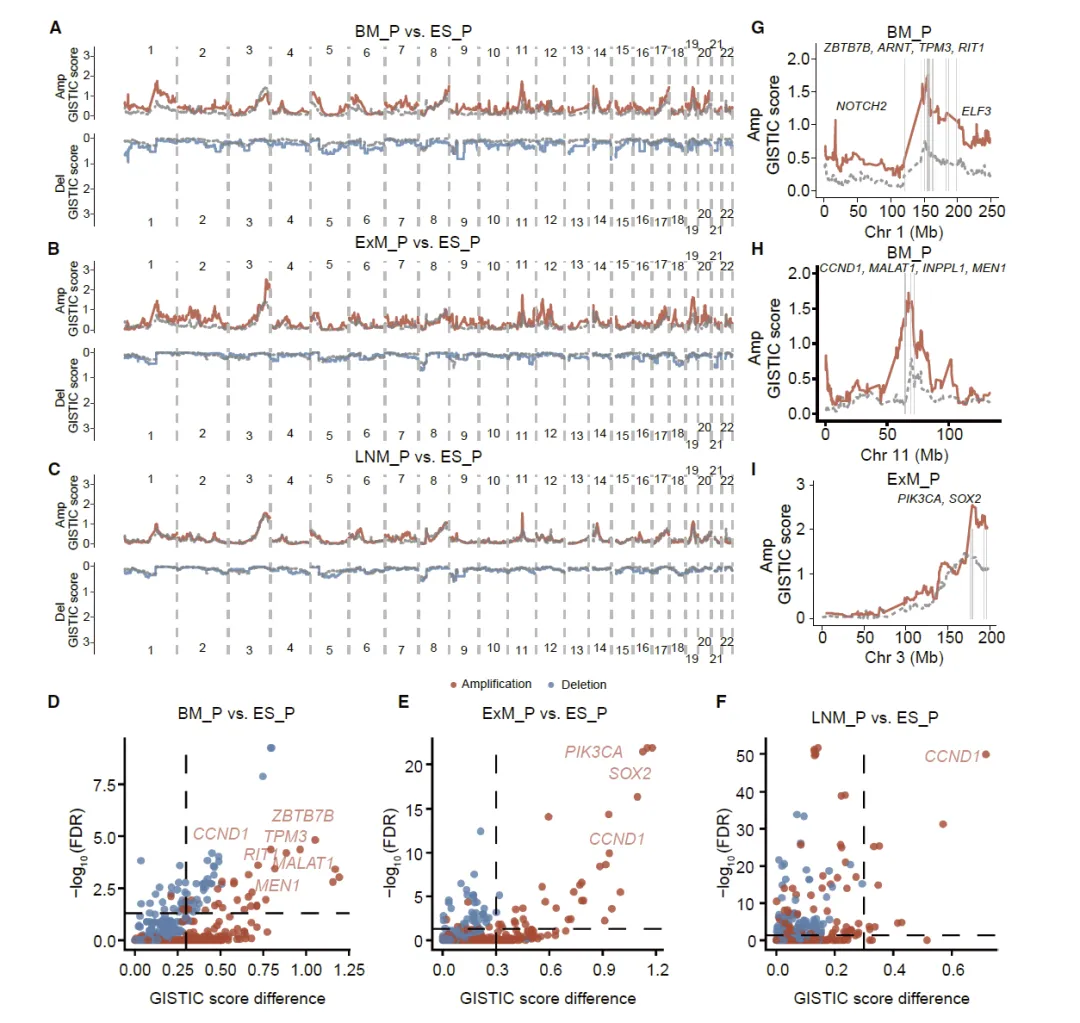
Figure 3 脑及颅外转移相关的体细胞拷贝数变异筛选与定位
这张图聚焦于体细胞拷贝数变异在肺癌器官特异性转移中的作用,通过 GISTIC 分析全面扫描并对比脑转移原发灶、颅外转移原发灶、淋巴结转移原发灶与早期无转移原发灶之间的基因组扩增与缺失区域,结果显示脑转移和颅外转移相关原发灶的拷贝数变异事件远多于淋巴结转移组,其中脑转移原发灶在 1 号染色体和 11 号染色体上存在多个显著扩增区域,包含 ZBTB7B、ARNT、CCND1、MALAT1 等多个驱动基因,颅外转移原发灶则在 3 号染色体上出现 PIK3CA、SOX2 所在区域的特征性扩增,同时通过统计检验明确这些差异拷贝数变异位点的显著性,证明原发肿瘤在进展过程中,特定染色体区段的拷贝数改变会形成器官转移的易感特征,为转移灶在特定器官的定植提供了拷贝数层面的选择优势。
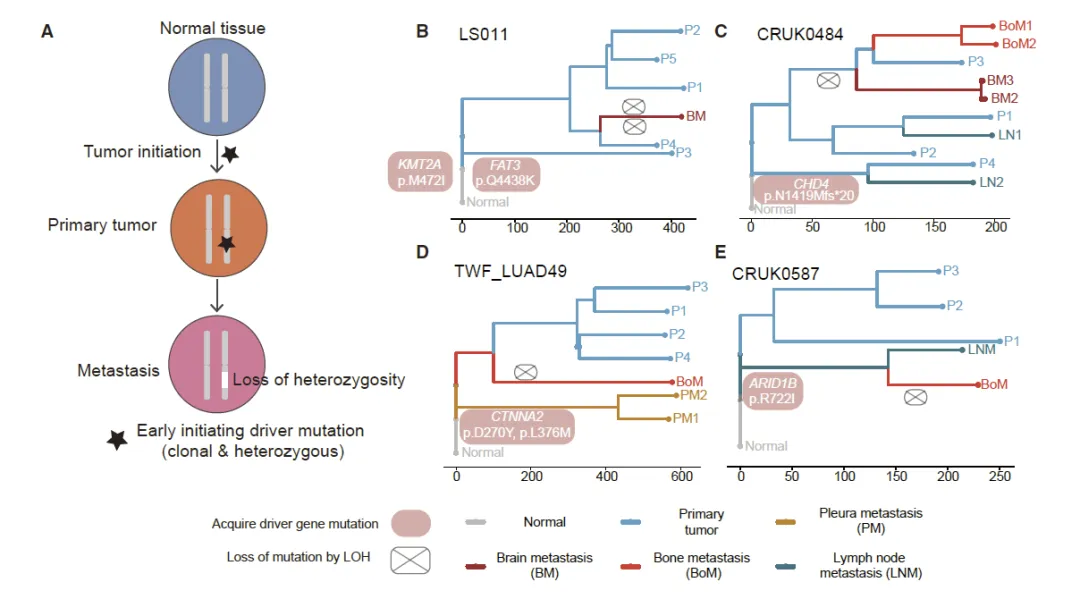
Figure 4 转移灶中由杂合性缺失介导的早期驱动突变丢失现象
这张图揭示了肺癌转移进化中一种全新的关键事件,即原发肿瘤的早期克隆驱动突变,会在转移灶中通过杂合性缺失(LOH)机制发生特异性丢失,首先以模式图清晰呈现该过程:肿瘤起始阶段产生的早期杂合驱动突变,在转移定植过程中因 LOH 导致突变等位基因丢失,进而使该驱动突变在转移灶中消失,随后通过 4 例患者的肿瘤多区域进化树,直观展示 KMT2A、FAT3、CHD4、ARID1B、CTNNA2 等驱动突变,在肿瘤共同祖先中获得,却在脑转移、骨转移等远端转移灶中经 LOH 丢失的进化轨迹,这一现象说明原发灶中有利的驱动突变,在脑、骨等截然不同的转移微环境中可能变为不利因素,进而在净化选择作用下被清除,反映出转移器官微环境对肿瘤基因组进化的强烈重塑作用。
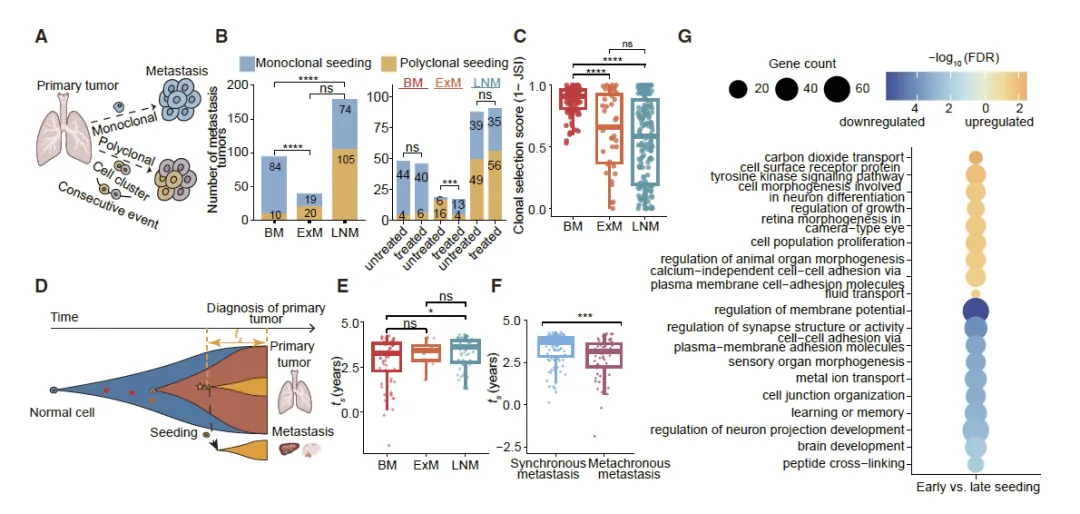
Figure 5 肺癌不同部位转移的克隆播种模式与时间特征
这张图核心阐明了非小细胞肺癌脑转移、颅外转移、淋巴结转移在克隆播种方式和播种时间上的显著差异,首先通过定义单克隆与多克隆播种的判断标准,发现脑转移以 89% 的极高比例呈现单克隆播种模式,远高于颅外转移的 49% 和淋巴结转移的 41%,且治疗仅影响颅外转移的克隆性,对脑转移无明显作用,同时结合转录组数据发现细胞黏附相关基因高表达与多克隆播种相关,细胞连接相关基因低表达与早期转移相关,随后通过逆向模型估算转移播种时间,证实脑转移的播种时间显著晚于淋巴结转移,异时性转移的播种时间也晚于同步性转移,完整揭示了脑转移因血脑屏障限制,呈现单克隆瓶颈、晚期播种的独特进化规律,而淋巴结转移多为多克隆、早期播种,从克隆结构和时间维度明确了不同部位转移的差异化进化模式。
4.研究总结
非小细胞肺癌器官亲嗜性转移由原发肿瘤驱动基因突变决定,而非转移后获得性突变;脑转移具有独特基因组演化轨迹,表现为高体细胞变异负荷、高比例单克隆播种、相对晚播散的特征;PTPRD、FAT1可作为肺癌脑转移风险的潜在预测标志物;转移灶可通过 LOH 丢失原发灶早期驱动突变,反映转移器官微环境的独特选择压力;该研究系统刻画肺癌转移进化规律,为脑转移早期预警、精准分型与靶向治疗策略开发提供关键基因组学依据。
局限:脑转移亚组分层不足,LOH 机制样本量小,存在研究间异质性。展望:扩大多区域测序队列,实验验证候选驱动基因,结合线粒体示踪与单细胞测序深入解析转移播种机制。
文献来源:Xie D, Tang WF, Jiang T, Duan H, Mo S, Zhang H, Zhai X, Tian Q, Li Z, Liang Y, Huang WZ, Jiang HM, On Lee LT, Zhang C, Zhai W, Mou Y, Zhong WZ, Hu Z. Deciphering genomic evolution of metastatic organotropism with 535 paired primary lung cancers and metastases. Cell Rep. 2025 Oct 28;44(10):116449. doi: 10.1016/j.celrep.2025.116449. Epub 2025 Oct 15. PMID: 41100253.
#肺癌#脑转移#基因组演化#器官亲嗜性#单克隆播种#PTPRD#FAT1#LOH

国家杰青一对一答疑视频
医学省自然申请答疑,立项的关键条件是哪一些?从哪些方向可以杀出重围
临床型博士如何准备国青标书?没有预实验怎么办?专家一对一解答规划
中医药科研研究