【纳米】深圳大学王东团队JACS:“肺捕获”新策略,精准治疗耐药菌肺炎与败血症
- 2026-05-26 11:42:12

注:文末有研究团队简介及本文科研思路分析
抗生素耐药已成为全球健康的主要威胁之一,每年导致数百万人死亡。其中,MRSA是引起肺炎、败血症等高死亡率感染的主要元凶。传统抗生素疗法依赖于不断识别并攻击细菌的特定靶点,犹如一场无休止的“军备竞赛”,且易破坏宿主正常菌群。抗菌肽和光动力疗法等替代策略虽各有优势,但前者往往缺乏精准靶向,后者则难以应对全身性扩散的感染。因此,亟需一种能够时空精准、高效低毒的创新治疗策略。能否转换思路,在体内关键部位设下“天罗地网”,主动拦截并清除循环中的耐药细菌?
近日,一项发表于Journal of the American Chemical Society的研究提出了革命性的“肺捕获”治疗诊断新策略。该研究由深圳大学王东团队主导,不同于传统的纳米颗粒肺部递送或滞留策略,也不同于直接在血管中捕获细菌,该策略利用一种物理捕获系统,将循环中的细菌聚集并截留于肺部微血管网络中,从而通过局部光疗实现清除,并将肺部转化为一个主动防御屏障。基于这一理念,构建了一种近红外二区聚集诱导发光(AIE)-多肽生物偶联体系BTFR。BTFR由三个功能模块组成:第一,配体肽RLYLRIGRR,可选择性识别并结合革兰氏阳性菌(如MRSA)细胞壁上的脂磷壁酸(LTA);第二,自组装抗菌肽基序FIIIKKK,使BTFR在初始状态下形成纳米颗粒结构,并在与LTA结合后发生结构转变形成纳米纤维;第三,近红外二区AIE分子BTPA-COOH,用于实现实时荧光成像和光动力治疗。
经静脉注射后,BTFR纳米颗粒能够在肺部微血管网络中快速富集并长时间滞留,从而在肺部形成一种“捕获陷阱”。当侵袭性细菌存在于肺部或血液循环中时,BTFR纳米颗粒能够通过特异性的受体–配体相互作用迅速识别细菌,并发生纳米纤维化结构转变,从而有效捕获细菌,抑制其侵袭能力并降低致病性。BTFR体系的近红外二区荧光发射使其在体内的分布情况能够实现实时监测。此外,被截留在肺部的系统性传播细菌还可以通过局部光照进行有效清除。
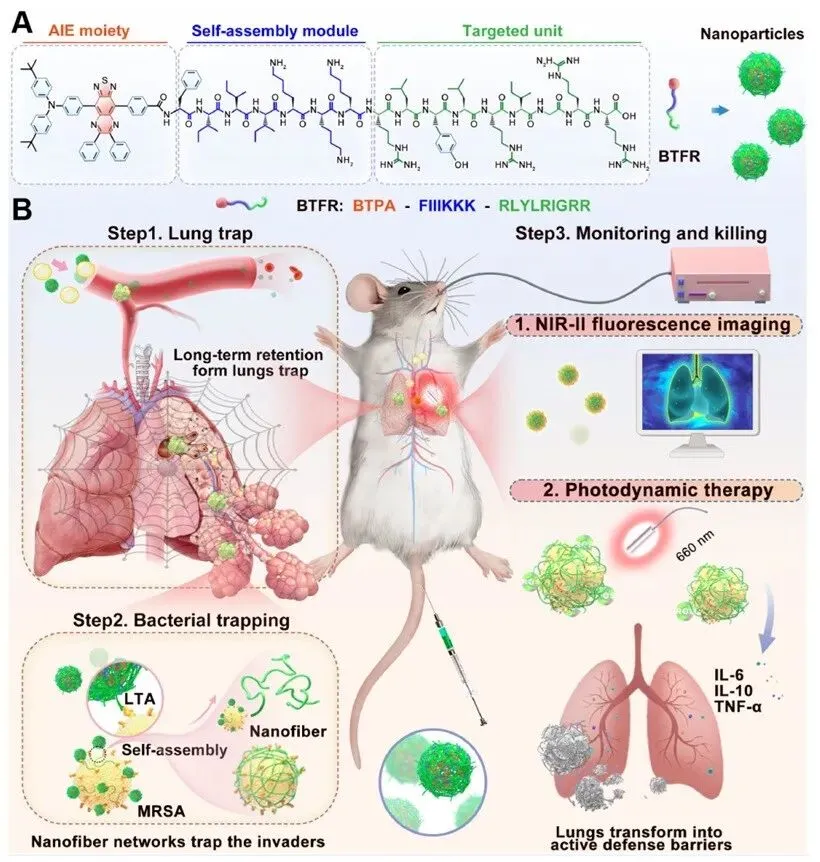
图1. BTFR通过“肺部陷阱”策略治疗MRSA诱发肺炎和菌血症的示意图。
BTFR的设计充分利用了人体肺部独特的毛细血管网络结构。静脉注射后,BTFR分子通过与血液成分相互作用,形成适当大小的聚集体,被肺部毛细血管机械性截留,从而在肺部形成一道“防线”。为确保治疗安全,团队在设计中前瞻性地避免了潜在栓塞风险。BTFR在肺部并非永久“堵截”,而是设计了一个动态的“捕获-解离-再捕获”循环。在血流剪切力作用下,部分聚集体可分解并重新进入循环,最终通过肝脏被逐步代谢清除。这种可逆机制既保证了药物在肺部的长期驻留和均匀分布,又确保了最终的安全清除,展现了卓越的临床转化潜力。
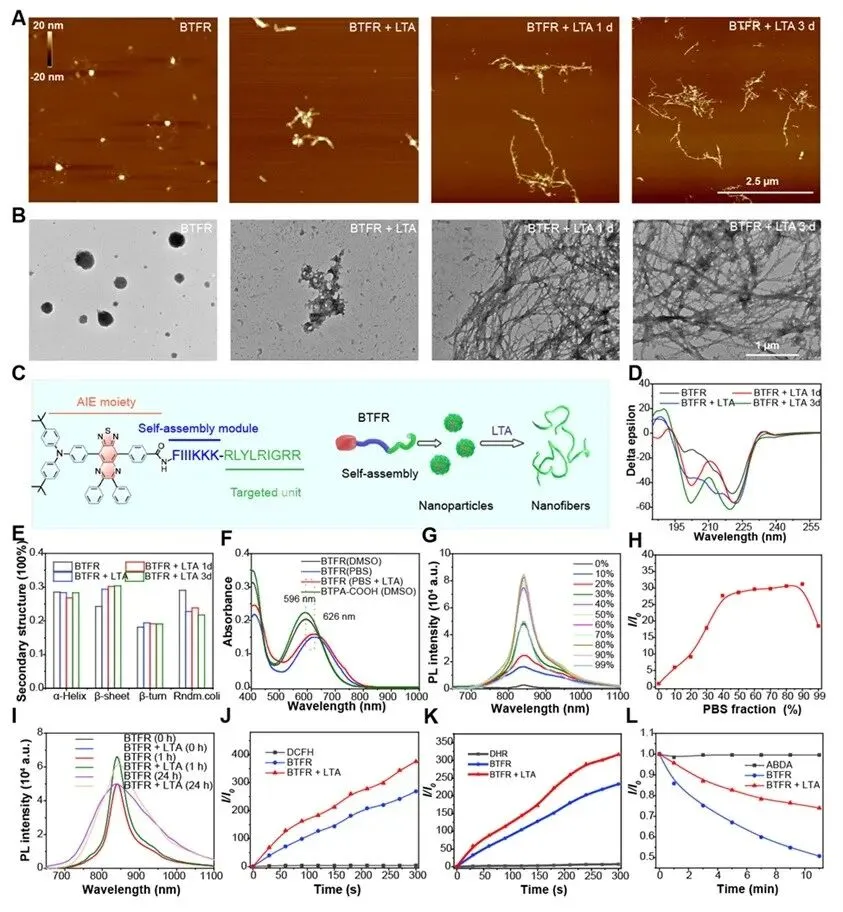
图2. BTFR的光物理特征。
实验表明,BTFR纳米颗粒能特异性识别金黄色葡萄球菌表面的靶点,并在结合后迅速自我组装成一张致密的“纳米纤维网”,将细菌牢牢缠绕、聚集,使其无法自由移动。更关键的是,这种“困住”策略直接瓦解了细菌的侵袭能力。单纯的捕获并非终点。BTFR被设计为“多模态”智能分子,其第二步杀招是“光动力清除”。研究证实,BTFR本身在黑暗条件下不具有直接杀菌活性,一旦对捕获了细菌的BTFR进行特定波长(660 nm)的光照,其内置的光敏模块会被激活,高效产生具有杀伤力的活性氧(ROS),对已聚集的细菌进行“定点清除”。BTFR联合光照,不仅能有效抑制新生物膜的形成,更能强力清除已成熟的生物膜。
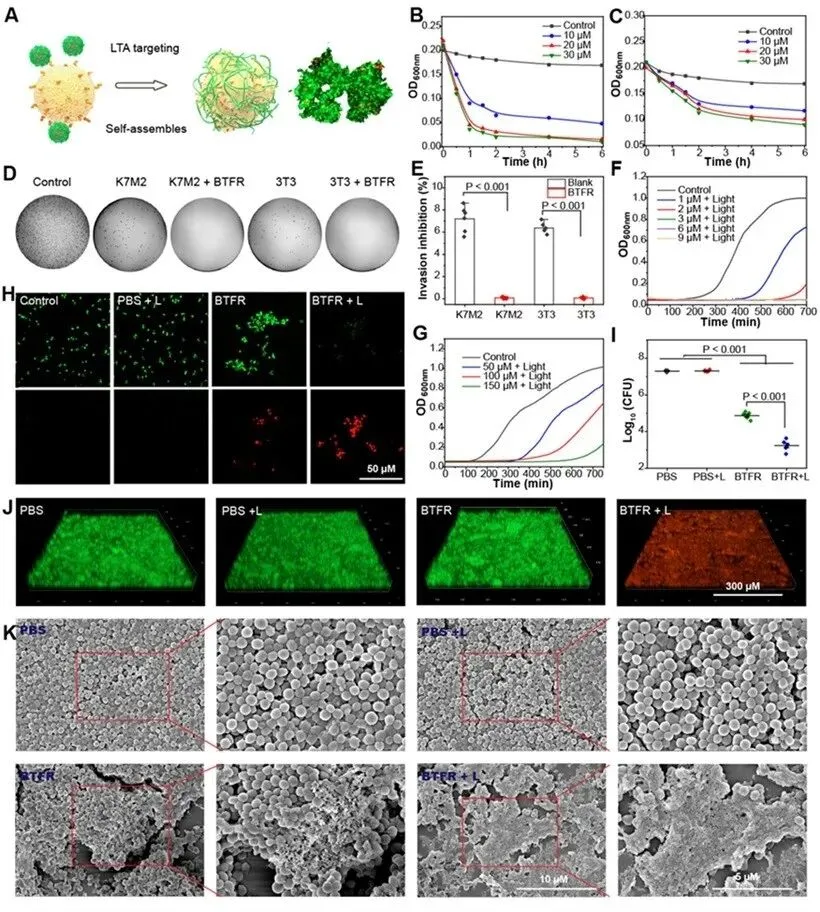
图3. BTFR的体外抗菌功效。
通过对比未处理的细菌,研究绘制了耐药菌在遭遇新型疗法时的全局基因表达变化图谱。分析显示,仅BTFR处理就影响了超过460个基因的表达。而当BTFR结合光照后,另有438个基因的表达发生显著改变。这些发生变化的基因广泛富集于多个关键生命过程,包括细胞间通讯、物质转运、DNA复制修复以及新陈代谢等,表明BTFR处理对细菌的生存状态造成了全方位冲击。该转录组学研究从最根本的基因表达层面,揭示了“物理捕获”与“生化清除”并非独立环节,而是连贯的协同作战。BTFR首先创造一个物理限制的微环境,迫使细菌转入低毒、低侵袭的防御状态;紧随其后的光动力打击,则能高效地对此状态下聚集的细菌造成致命DNA损伤。
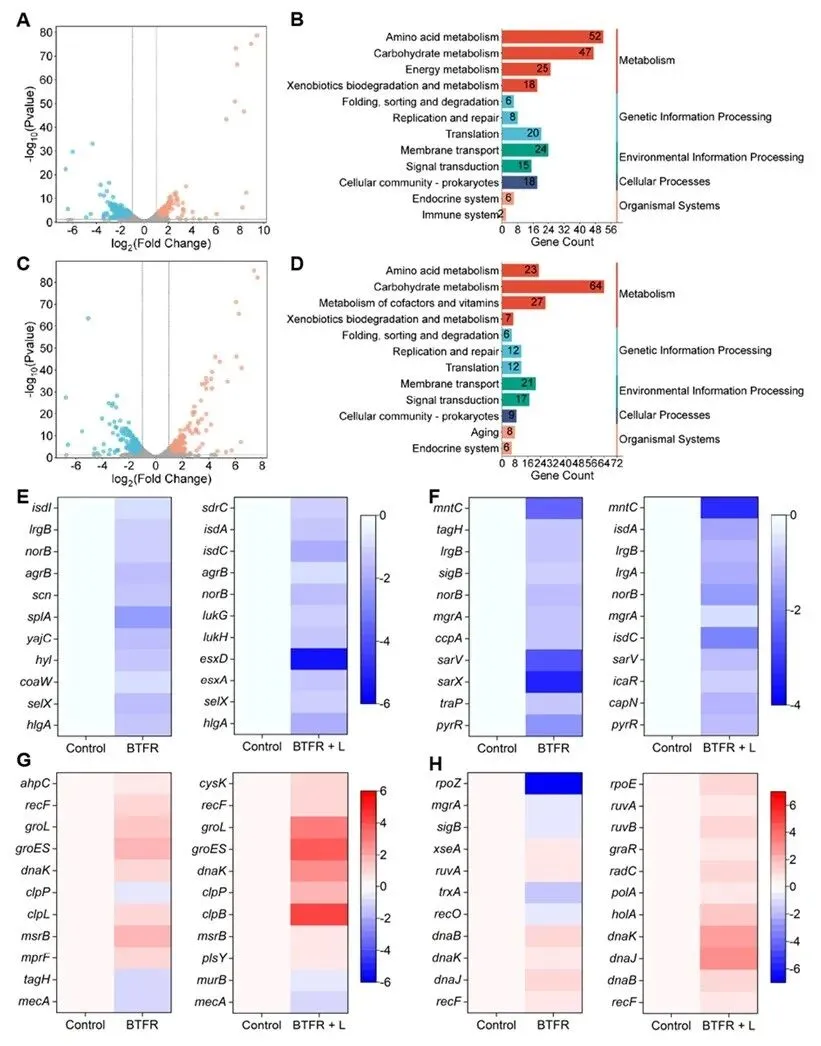
图4. MRSA的转录组分析。
静脉注射后,BTFR迅速在肺部聚集,产生强烈的荧光信号,证实了其高效、选择性的肺部靶向能力。BTFR在肺部的驻留是一个智能的动态过程。其荧光信号在注射初期达到峰值,随后逐渐减弱,并在约15天后基本无法检测。药代动力学分析揭示了背后的精妙机制:BTFR并非被一次性永久截留,而是在肺部毛细血管中经历“捕获-解离-再捕获”的循环。在血流剪切力作用下,部分聚集体可分解并重新进入体循环,而分子本身的肽链会逐渐被蛋白酶降解。最终,降解产物主要通过肝脏被代谢清除,平均终末消除半衰期约为107.7小时。
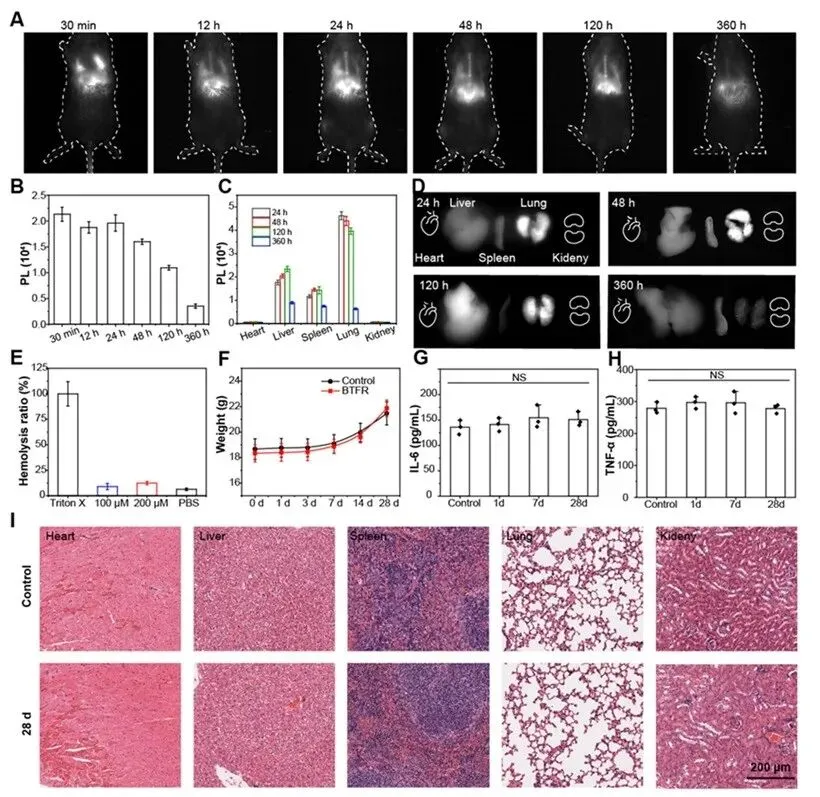
图5. BTFR的体内成像和生物安全。
在致死性MRSA肺炎模型中,所有对照组小鼠均在48小时内死亡。相比之下,仅接受BTFR注射(仅捕获,不照射)的小鼠,14天生存率达到66%。而接受完整“BTFR注射+肺部光照”治疗的小鼠,生存率进一步提升至83%,实现了从无人生存到多数存活的根本性逆转。对肺部组织的分析显示,单独光照无杀菌效果。BTFR组通过捕获作用使肺部细菌载量降低约1.65个数量级。而“BTFR+光照”治疗组清菌效果惊人,细菌载量下降2.9个数量级,几乎将肺部细菌彻底扫清。治疗显著降低了肺部灌洗液和血液中关键促炎因子(TNF-α, IL-6, IL-1β)的水平,说明该疗法有效遏制了感染引发的致命“炎症风暴”,减轻了机体自身免疫反应导致的附带损伤。
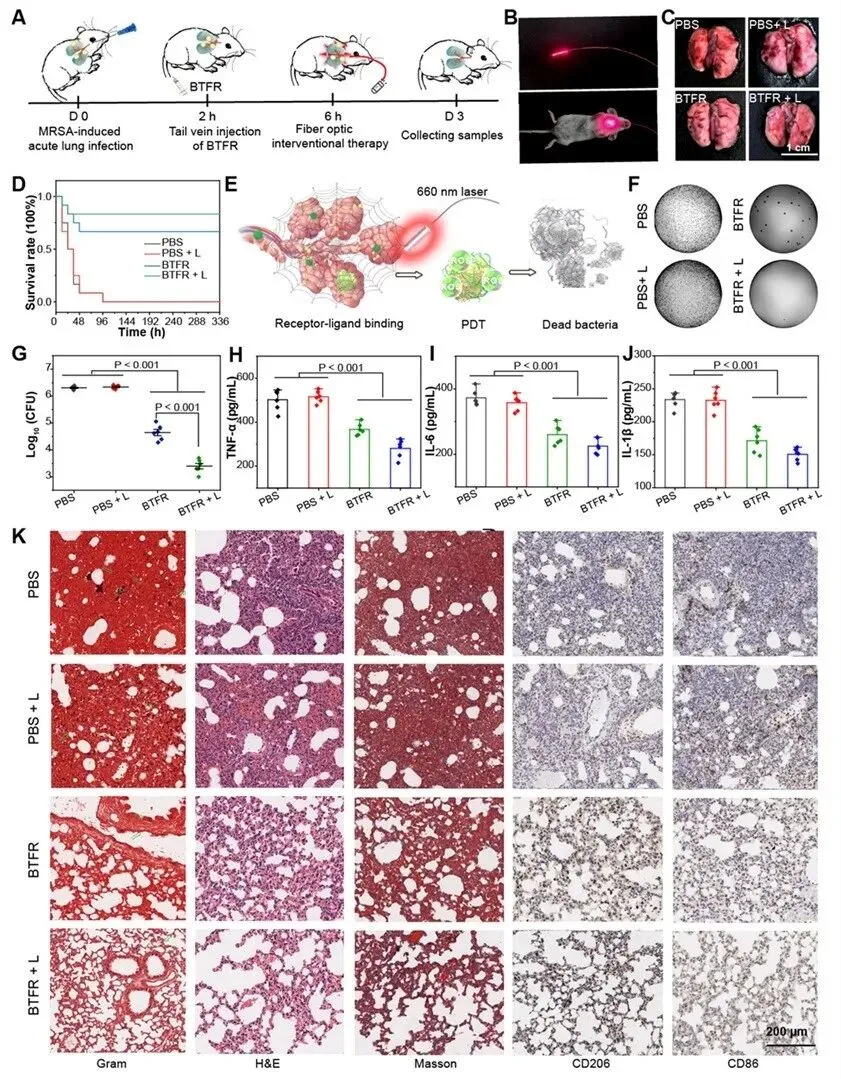
图6. “肺陷阱”策略用于治疗MRSA引起的急性肺炎。
该研究清晰阐明,“肺陷阱”策略治疗败血症的成功依赖于两步协同:首先,BTFR在肺部血管形成“过滤网”,物理拦截并富集循环中的细菌,阻止其向全身器官扩散;随后,通过局部光照激活光动力效应,对已聚集的细菌进行高效清除。所有对照组小鼠在48小时内全部死亡。而仅接受BTFR注射(仅物理捕获)的小鼠,存活率与常用抗生素万古霉素(van)治疗组相当,达到75%。接受完整“BTFR+光照”治疗的小鼠,存活率进一步提升至92%,近乎实现全员存活。感染后48小时检测发现,BTFR治疗使血液、心脏、肝脏、脾脏、肺和肾脏中的细菌负荷均下降超过99.9%。这直接证实“肺陷阱”策略能高效捕获并清除循环于全身的细菌,防止其在各器官定植。治疗显著降低了血液中关键促炎细胞因子(TNF-α, IL-6, IL-1β)的水平,表明该疗法有效遏制了败血症引发的全身过度炎症反应,避免了“细胞因子风暴”对机体的二次打击。
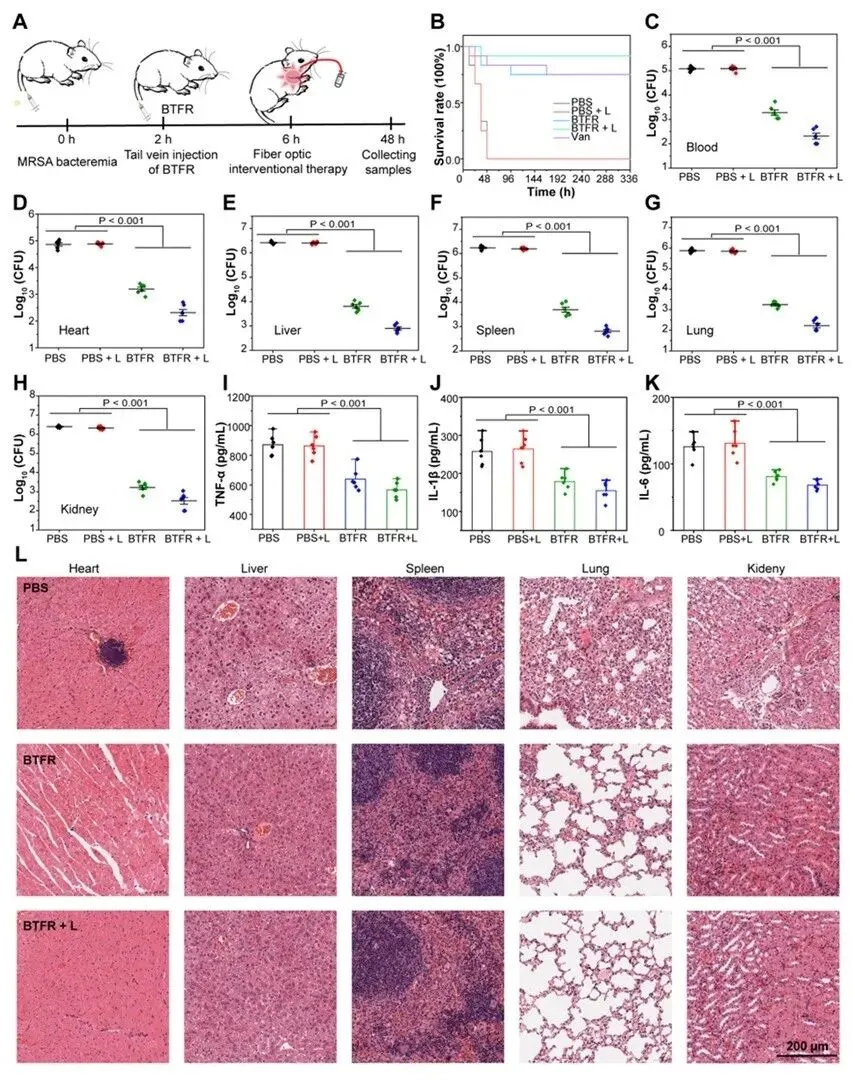
图7. “肺陷阱”策略用于治疗MRSA引起的菌血症。
研究成果发表在J. Am. Chem. Soc.上。深圳大学侯养谦博士、燕鼎元研究员和黄伟庚硕士生为该论文共同第一作者,深圳大学王东教授为本文通讯作者。
原文(扫描或长按二维码,识别后直达原文页面):

A “Lung-Trap” Theranostic Strategy for Precision Management of Drug-Resistant Bacterial Pneumonia and Bacteremia
Yang Qian Hou, Dingyuan Yan, Weigeng Huang, Dengke Chen, Jiachun Chen, Shilin Chen, Yu Tian, Jiayi Chen, Ben Zhong Tang, Dong Wang*
J. Am. Chem. Soc., 2026, DOI: 10.1021/jacs.6c00209
研究团队介绍

王东,教授,博士生导师,现任深圳大学材料学院副院长,深圳大学AIE研究中心执行主任,Luminescence期刊(Wiley)主编。获得国家优青、国家重点研发计划(青年)、广东省杰青基金。在Nat. Nanotechnol.、Nat. Chem.、Nat. Protoc.、Nat. Rev. Bioeng.、J. Am. Chem. Soc.、Angew. Chem. Int. Ed.、Adv. Mater.等期刊上发表论文多篇,28篇论文入选“ESI高被引论文”。论文共被引用20000余次。H指数74。以第一或唯一完成人获得广东省科学技术奖-青年科技创新奖、广东省材料研究会青年科技奖、深圳市自然科学奖二等奖,深圳市科学技术奖青年科技奖,“深圳市优秀教师”荣誉称号。
科研思路分析
Q:这项研究最初是什么目的?或者说想法是怎么产生的?
A:这项研究最初的、最根本的目的是应对全球抗生素耐药性(AMR)危机,并试图彻底改变传统抗菌治疗的范式。想法产生于对现有疗法局限性的深刻反思。传统“全身化学歼灭”模式在与细菌的进化竞赛中疲于奔命,且破坏菌群。我们因此提出范式转换的构想。若能设计一种药物,在静脉注射后选择性滞留在肺部血管中“设伏”,就能将肺部从被动的感染部位转变为主动捕获、清除血液中细菌的“防御屏障”。这一构想最终通过融合靶向肽、刺激响应自组装、以及聚集诱导发光(AIE)光动力技术等多学科前沿而得以实现。
Q:研究过程中遇到哪些挑战?
A:该研究面临多重挑战,核心在于实现创新策略的同时确保其安全性与有效性。既要让药物精准靶向并在肺部有效滞留以形成“陷阱”,又要避免造成肺部栓塞或长期毒性。我们通过设计动态的“捕获-解离-再捕获”循环及可降解的分子结构解决了这一问题。其次,如何让同一个分子无缝衔接“物理捕获”和“光动力清除”两种功能,并通过分子设计使其在捕获细菌后自发增强杀伤效能;同时,如何让光疗有效作用于肺部深处,这需要通过使用长波长光源或图像引导的介入技术来克服组织穿透深度的限制。最后,拓展应用范围也是一个明确挑战,目前平台主要针对革兰氏阳性菌,未来需通过模块化设计适配更广的病原体。
Q:该研究成果可能有哪些重要的应用?
A:该成果最重要的应用在于为治疗致命的耐药细菌感染提供了一种全新的精准治疗范式,尤其适用于传统抗生素无效的MRSA引起的重症肺炎和败血症,其局部拦截、定点清除的模式能极大降低全身毒性和耐药风险。此外,它在处理生物膜相关感染(如慢性伤口、医疗器械感染)和作为诊疗一体化平台(治疗同时可实时成像)方面也潜力巨大。



