《合成生物学》推荐 | 深圳先进院卞光凯/华中农大徐娟/波恩大学Dickschat合作实现细菌二萜合酶的系统挖掘与结构导向功能互换
- 2026-03-31 19:22:52
摘 要
萜类化合物是一类兼具重要经济价值和生物学功能的天然产物,其中二萜类化合物以其复杂的环化反应和显著的生物活性而闻名,植物激素赤霉素、抗癌药物紫杉醇均为其典型代表。过去几十年,研究人员主要从植物和真菌中寻找新颖萜类化合物灵感,而近年来,细菌作为极具潜力却尚未被充分挖掘的萜类生物合成基因宝库,正逐渐进入科学家的视野。然而,如何从数以万计的候选基因中精准筛选出具有活性的萜类合酶,并理解其催化机制,是制约该领域核心瓶颈。
2026年3月16日,中国科学院深圳先进技术研究院定量合成生物学全国重点实验室、合成生物学研究所卞光凯团队联合华中农业大学徐娟课题组和波恩大学Jeroen S. Dickschat课题组,在国际期刊Journal of the American Chemical Society上发表了题为“Systematic Discovery of Bacterial Diterpene Synthases and Structure-Guided Functional Interconversion of ShHS and CbCS”的最新研究成果。该研究通过系统挖掘细菌二萜合酶,显著拓展了细菌二萜天然产物的化学空间,并揭示了活性中心微环境对产物骨架分化的决定作用。

文章上线截图
(点击文末“阅读原文”可直达文章链接)
研究内容
在本研究中,研究团队首先构建了基于大规模基因组挖掘与工程酵母异源表达相结合的高通量筛选体系,对313个候选的细菌I型二萜合酶进行了高通量功能筛选。通过一系列筛选,团队成功鉴定出16个具有二萜活性的萜类合酶(系列单萜、倍半萜和二倍半萜合酶功能验证仍在进行中),并表征了10种新二萜化合物,其中包含5种全新碳骨架(图1 B)。这一发现大幅扩展了细菌二萜类化合物的结构多样性和化学空间。
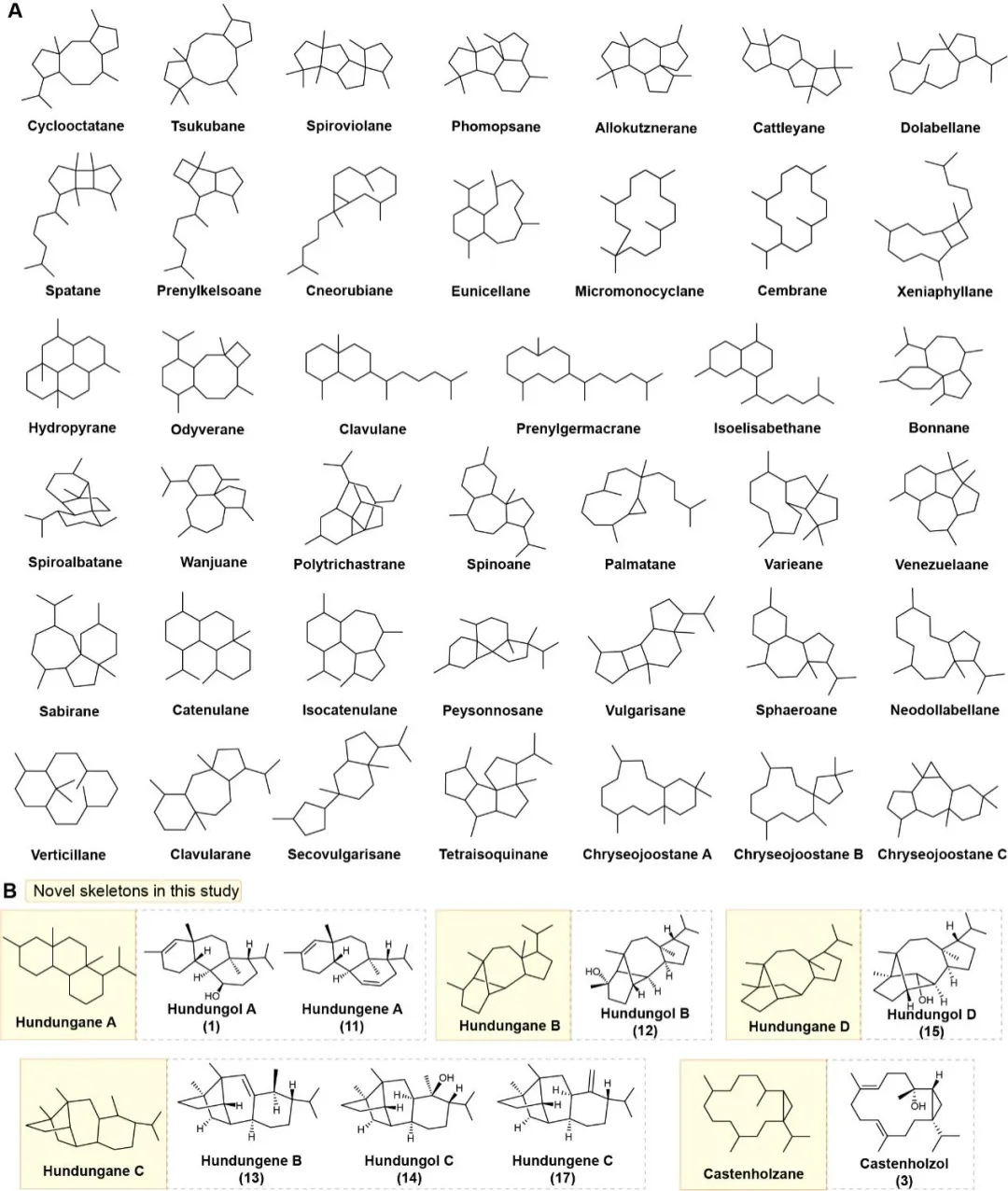
图1 细菌中形成的二萜骨架的多样性
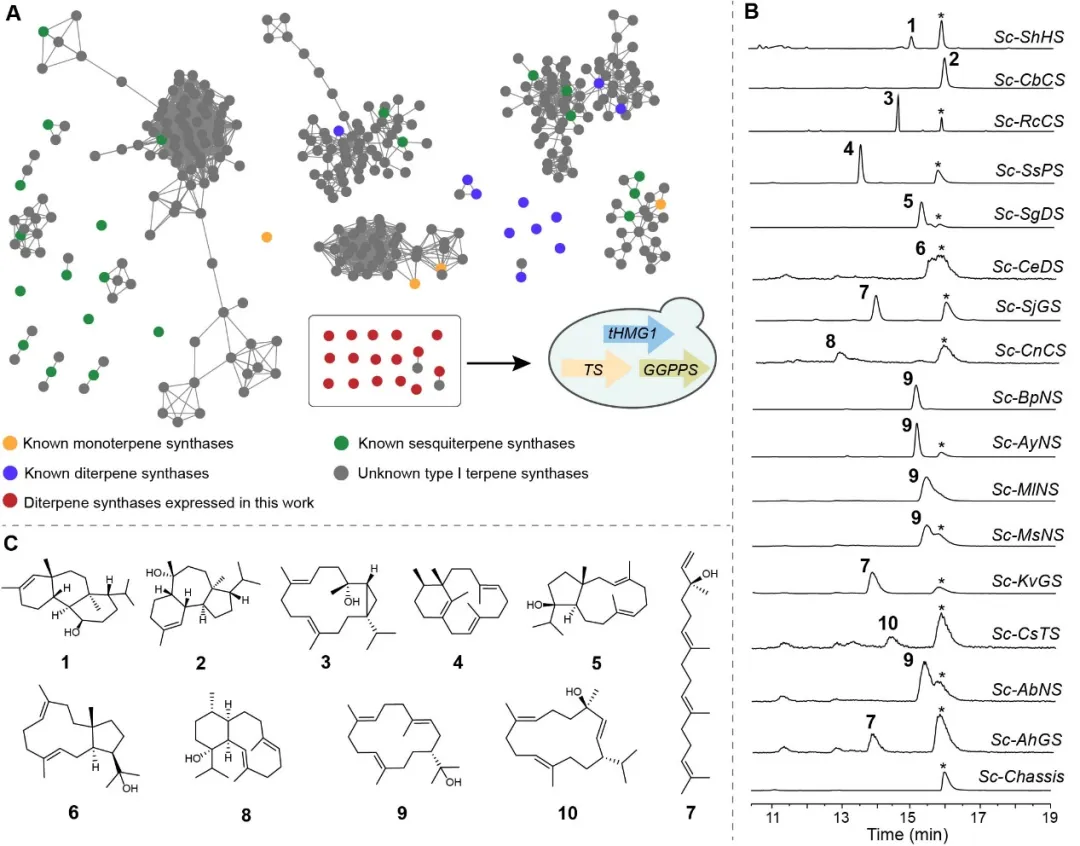
图2 细菌二萜合酶的基因组挖掘和功能表征
在此基础上,研究人员进一步聚焦来源于Streptomyces hundungensis的二萜合酶ShHS。通过密度泛函理论计算与精确同位素标记实验相结合,系统解析了该酶催化GGPP环化生成hundungol A及系列副产物的完整反应机制。研究表明,该反应首先通过GGPP异构化生成GLPP,为后续关键的1,11-环化反应奠定构象基础;随后经连续环化、氢迁移和甲基迁移过程,形成关键碳正离子中间体H。在后续反应阶段,不同的环化路径和骨架重排决定了最终产物的结构分支,其中包括一次罕见的1,5-氢迁移步骤。此外,研究还发现CbCS的产物2虽与上述机制具有相同的早期反应步骤,但在中间体H处直接被水分子淬灭。
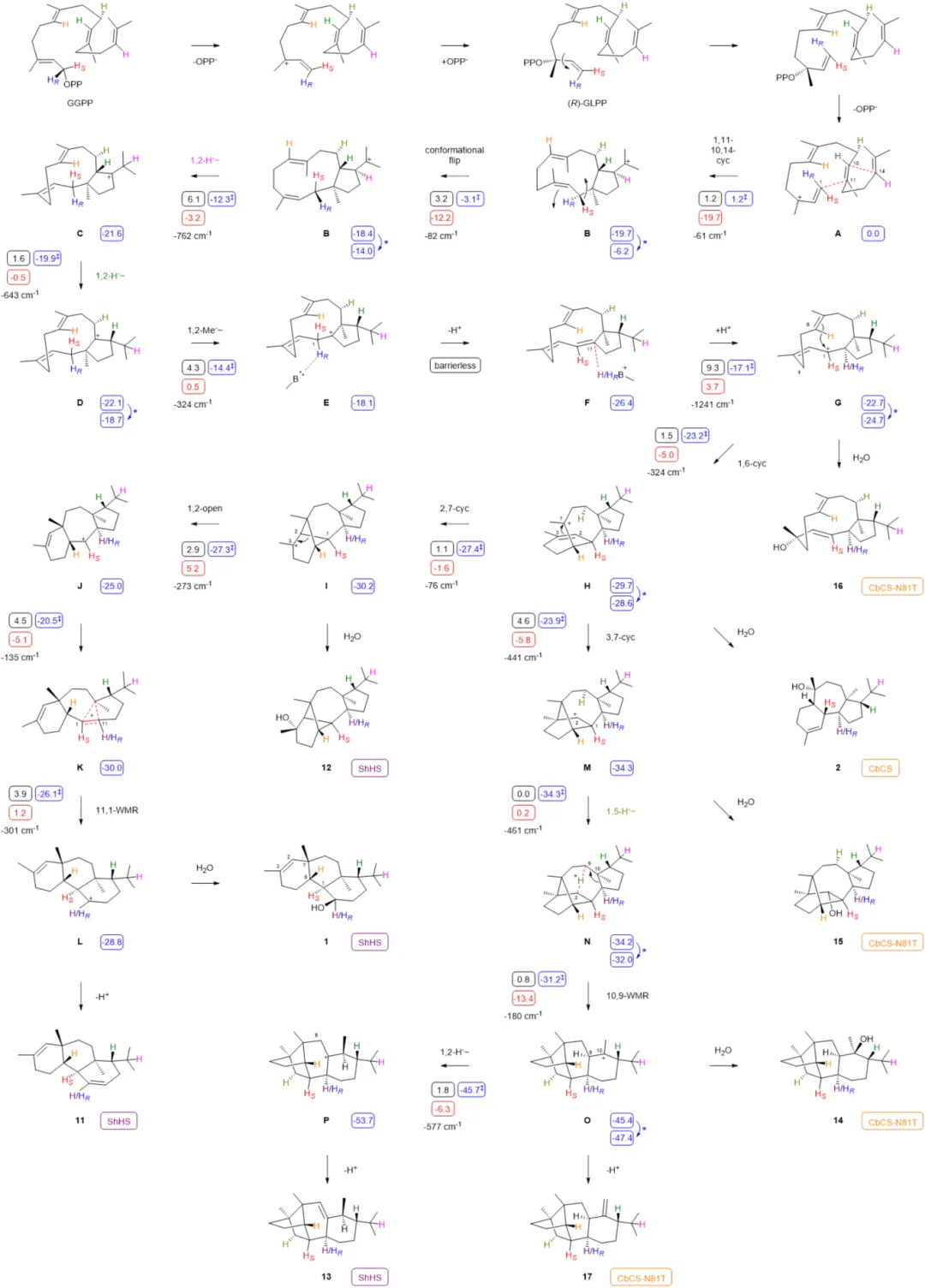
图3 ShHS和CbCS催化GGPP环化生成1、2和11-17的机制
一个关键问题随之出现:是什么决定了CbCS和ShHS两个酶在分支点H之后的反应方向?为了回答这一问题,研究人员成功解析了CbCS的晶体结构,同时借助AlphaFold3完成了ShHS的结构预测,并将关键中间体H分别对接至两个酶的活性中心开展比对分析。结构分析结果显示,中间体H周围共有17个潜在参与催化的氨基酸残基,其中8个在两种酶之间存在差异。通过定点突变实验,研究人员成功实现了二者的功能互换:在ShHS中引入E193T和L196Y突变,可使其生成CbCS的主要产物;而在CbCS中引入相应的反向突变T194E和Y197L,则能产生ShHS的特征产物。此外,位于活性中心附近的关键位点N76/N81对反应路径同样具有重要调控作用。研究团队进一步利用这些突变体,分离鉴定出hundungol C、hundungol D、chloroflexotol B和hundungene C等多种新型二萜化合物,并通过同位素标记实验,验证了这些化合物具有共同的早期环化过程,以及后期的1,5-氢迁移机制。
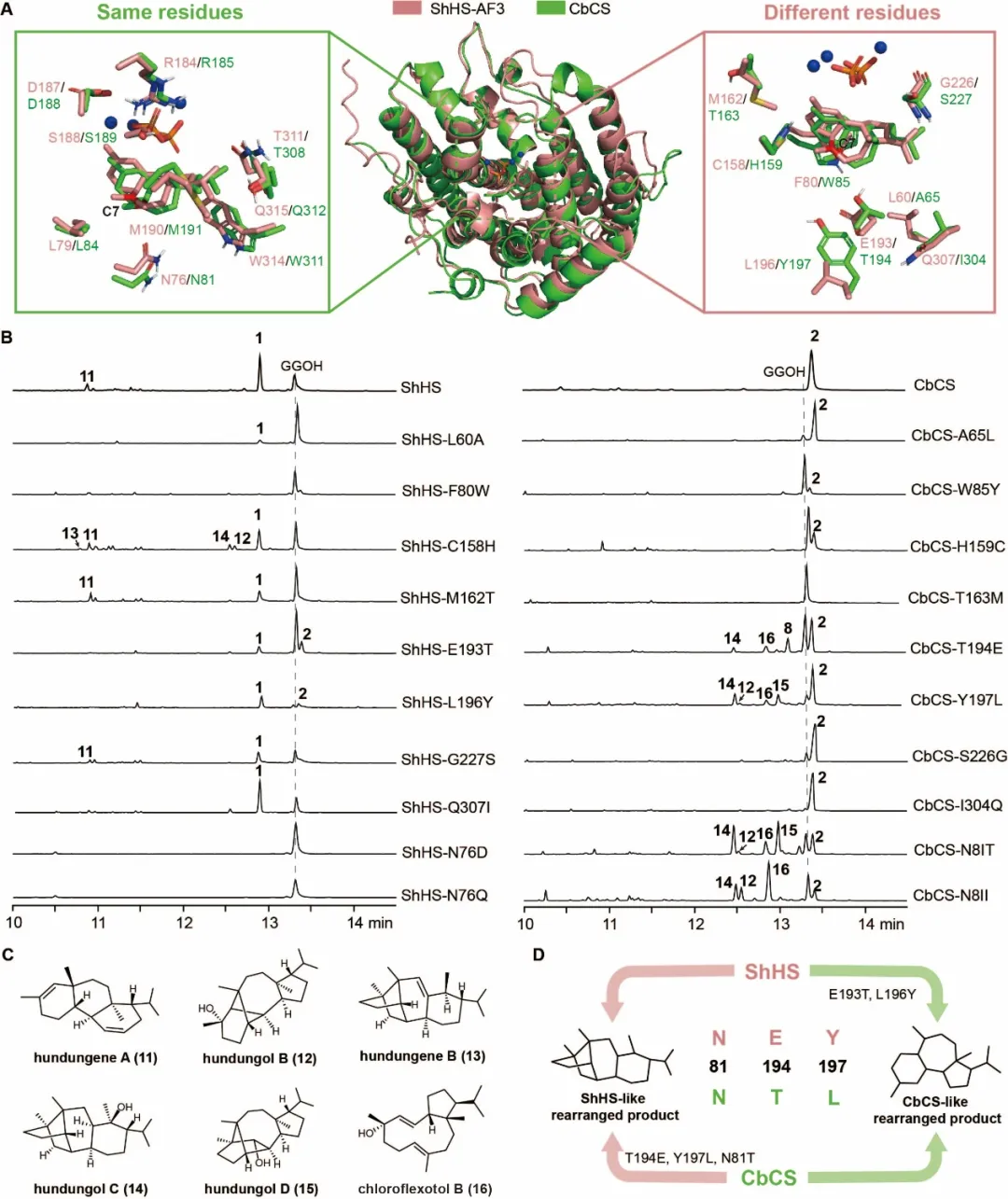
图4 ShHS 和 CbCS 变体的功能相互转化分析
在论文评审过程中,国际同行专家对该研究给予了高度评价。审稿人指出,在当前萜类合酶大规模挖掘研究不断涌现的背景下,该工作不仅是对新酶和新产物的罗列,更重要的是揭示了决定萜类骨架形成的结构与机理。总体而言,该研究通过整合基因组挖掘、合成生物学、结构生物学与计算化学等多学科方法,不仅系统拓展了细菌二萜天然产物的化学空间,还揭示了萜类合酶如何通过活性中心精细调控碳正离子级联重排,并实现不同产物骨架之间的可设计转换,为理解萜类天然产物多样性的分子基础提供了关键线索,也为基于理性设计的天然产物生物合成、新型萜类分子定向创制提供了重要的理论与技术支撑。
中国科学院深圳先进院定量合成生物学全国重点实验室、合成生物学研究所卞光凯研究员、华中农业大学徐娟教授和波恩大学Jeroen S. Dickschat教授为本文共同通讯作者;中国科学院深圳先进技术研究院/华中农业大学联合培养博士生胡哲辉和波恩大学博士后Zhiyong Yin为本文共同第一作者。中国科学院深圳先进技术研究院为第一完成单位。科隆大学Bernd Goldfuss教授、南方医科大学罗奇副教授为研究提供重要支持。感谢深圳合成生物研究重大科技基础设施在自动化萜类合酶挖掘和功能表征方面提供的支持。本研究得到了国家重点研发计划、国家自然科学基金、广东省杰出青年基金、深圳市重点项目以及深圳合成生物学创新研究院等项目的支持。
卞光凯课题组简介
卞光凯,中国科学院深圳先进技术研究院合成生物学研究所研究员,博士生导师。课题组聚焦于天然产物生物合成与高效生物制造,真菌生物材料的理论及应用研究。近5年作为第一/通讯作者在Nature,Nat. Catal.,JACS,Angew. Chem,Adv. Mater.,Nat. Commun.,PNAS等期刊上发表文章十余篇。主持国家自然科学基金面上项目、深圳市自然科学基金基础研究重点项目、科技部重点研发计划等科研项目。
实验室主页:
http://isynbio.siat.ac.cn/BianLab/
本文来源:iSynBio爱星博
责任编辑:焦欣渝 杨蕴力
排版设计:任晓静
总监制:胡晓丹
往期推荐


2026,7(1)

2025,6(6)

2025,6(5)

2025,6(4)

2025,6(3)

2025,6(2)

2025,6(1)

2024,5(6)

2024,5(5)
2024,5(4)

2024,5(3)

2024,5(2)

2024,5(1)

2023,4(6)

2023,4(5)
2023,4(4)

2023,4(3)

2023,4(2)

2023,4(1)

2022,3(6)

2022,3(5)

2022,3(4)

2022,3(3)

2022,3(2)

2022,3(1)

2021,2(6)

2021,2(5)

2021,2(4)

2021,2(3)

2021,2(2)

2021,2(1)

2020,1(6)

2020,1(5)

2020,1(4)
2020,1(3)

2020,1(2)

2020,1(1)
《合成生物学》编辑
识别二维码
与《合成生物学》编辑面对面

添加编辑微信 | 加入科学家社群
验证请写明 姓名+单位哦
点击下方“阅读原文”查看全文




