广州国家实验室 | 新生儿骨髓间质液通过NGF/LTF/HMGB1/IGF1协同增强hBMSC功能
- 2026-06-11 19:20:01

导读
基于骨髓微环境对干细胞功能的关键作用及骨髓间质液研究空白,推测新生儿骨髓间质液(NBIF)含支持干细胞增殖分化的 niche 因子,通过对比 NBIF 与胎牛血清(FBS)、成年牛骨髓间质液(ABIF)对人骨髓间充质干细胞(hBMSCs)的影响,结合转录组、蛋白质组分析筛选活性成分,验证关键因子组合(LINH 鸡尾酒)的作用,最终发现 NBIF 可通过 JAK-STAT3、CXCL12-CXCR4 通路增强 hBMSCs 自我更新、成骨分化及骨髓归巢能力,其活性成分组合可模拟该效应,为干细胞疗法优化及骨再生治疗提供新策略。
注:该文章发表于《Bone Research》,该期刊是由四川大学与Springer Nature合作出版的英文期刊,最新影响因子为15,位列JCR分区Q1区。
聚焦新生儿骨髓间质液(NBIF)这一未被充分探索的骨髓微环境成分,首次系统揭示其与成年牛骨髓间质液(ABIF)、胎牛血清(FBS)的组成差异及对 hBMSCs 的独特调控作用。通过多组学结合功能验证,筛选出 NGF、LTF、HMGB1 及 IGF1 组成的 LINH 鸡尾酒组合,可模拟 NBIF 增强 hBMSCs 成骨分化和骨髓归巢的核心功能,明确其通过 JAK-STAT3、CXCL12-CXCR4 通路发挥作用,为干细胞体外培养优化和骨再生临床治疗提供了全新的活性因子组合及作用机制参考。
骨髓间质液分离:从新生牛(1-7 天)和成年牛(3 岁)长骨中分离 NBIF、ABIF,提取新生牛血清(NBS),标准化蛋白浓度至 0.25 mg/mL。
干细胞培养与处理:hBMSCs 分别在含 NBIF、ABIF、FBS 的培养基中培养,进行长期传代(至 P17),检测细胞增殖、表型及衰老情况。
分化与归巢实验:通过茜素红、油红 O、阿尔新蓝染色检测成骨、成脂、成软骨分化能力;Transwell 实验检测细胞迁移能力,小鼠体内移植实验评估骨髓归巢效率;颅骨缺损模型验证骨再生效果。
分子机制研究:采用转录组测序(RNA-seq)分析基因表达变化,蛋白质组学(质谱)鉴定 NBIF 差异蛋白,结合 GSEA、GO 分析通路富集;通过抑制剂、siRNA 干扰验证 JAK-STAT3 通路的作用。
活性因子筛选与验证:利用 HPLC 分馏 NBIF,结合功能实验筛选活性组分,通过重组蛋白单独及组合处理,验证关键因子(NGF、LTF、HMGB1、IGF1)的协同作用。
NBIF 支持 hBMSCs 扩增并维持表型:NBIF 培养的 hBMSCs 可长期增殖,保持 CD73、CD90、CD105 阳性,CD34、CD45 阴性的间充质干细胞表型,基因组稳定,但不抑制复制性衰老。
增强成骨分化并调控基因表达:NBIF 组 hBMSCs 茜素红染色钙沉积更多,成骨标志物 RUNX2、COL1A1 表达上调,成脂分化减弱;转录组分析显示 1614 个差异基因,上调基因富集于骨形成、组织修复通路,下调基因与细胞增殖、免疫原性相关。
维持自我更新与骨髓归巢能力:NBIF 培养的 hBMSCs 成骨祖细胞标志物 LEPR 表达升高,CFU-F 集落形成能力增强;CXCR4 表达上调,Transwell 迁移实验中对 CXCL12 的响应性增强,体内移植后骨髓归巢率显著高于 FBS 组。
蛋白质组差异与活性因子鉴定:NBIF 富含 NGF、LTF、HMGB1 等组织修复相关因子,抗氧化酶(CAT、SOD1 等)富集;NGF、LTF、HMGB1 与 IGF1 组成的 LINH 鸡尾酒可显著上调 LEPR、RUNX2、CXCR4 表达,增强成骨分化,模拟 NBIF 效应。
促进骨再生:颅骨缺损模型中,NBIF 预处理的 hBMSCs 移植组骨体积分数和骨密度显著高于 FBS 组,骨缺损修复率达 34%。
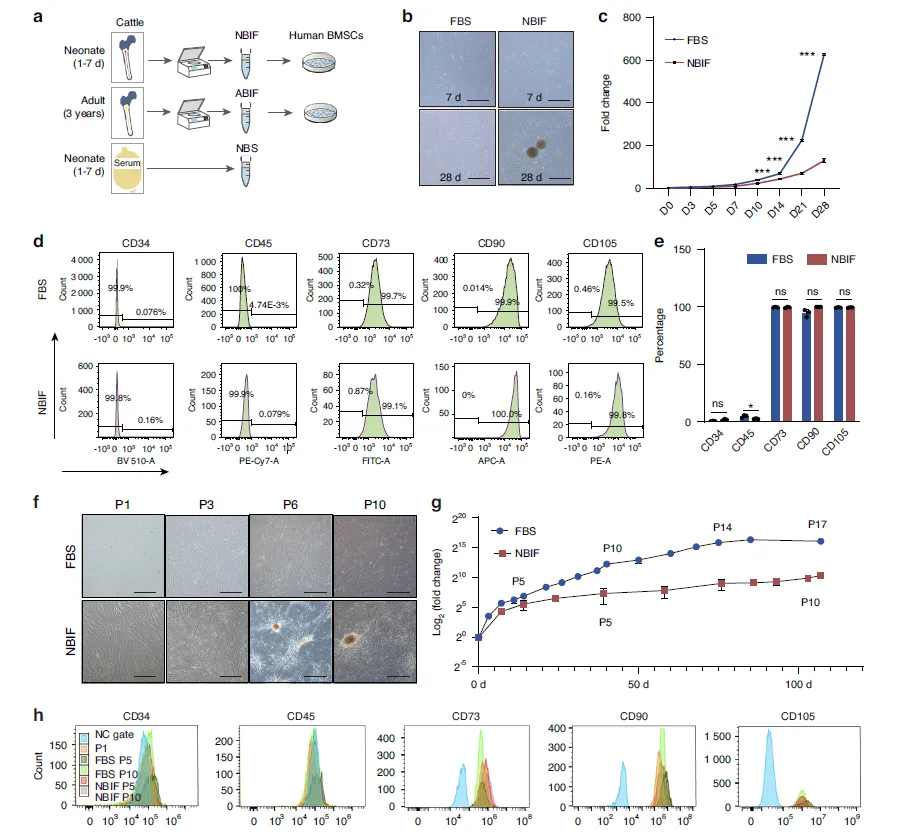
Figure 1:NBIF 对 hBMSCs 体外扩增及表型稳定性的影响
该图通过实验设计、细胞形态观察、生长曲线绘制及流式细胞术分析,阐明了新生儿骨髓间质液(NBIF)、成年牛骨髓间质液(ABIF)和胎牛血清(FBS)对人骨髓间充质干细胞(hBMSCs)体外培养的不同作用。结果显示,ABIF 显著抑制 hBMSCs 增殖并诱导其早期衰老,而 NBIF 虽增殖促进能力略低于 FBS,但能在 4 周培养期内支持 hBMSCs 扩增,且经 100 天 10 代传代后,仍能维持 hBMSCs 的 CD73、CD90、CD105 等特异性表面标志物表达,同时不表达造血细胞标志物 CD34 和 CD45,基因组也保持稳定。此外,NBIF 培养的 hBMSCs 在 3-4 周后会形成类球体结构,表明其具备维持 hBMSC 特性和自我更新的生物活性,且效果与 FBS 相当,但无法避免复制性衰老带来的细胞周期抑制剂上调及衰老相关 β- 半乳糖苷酶阳性细胞增多。
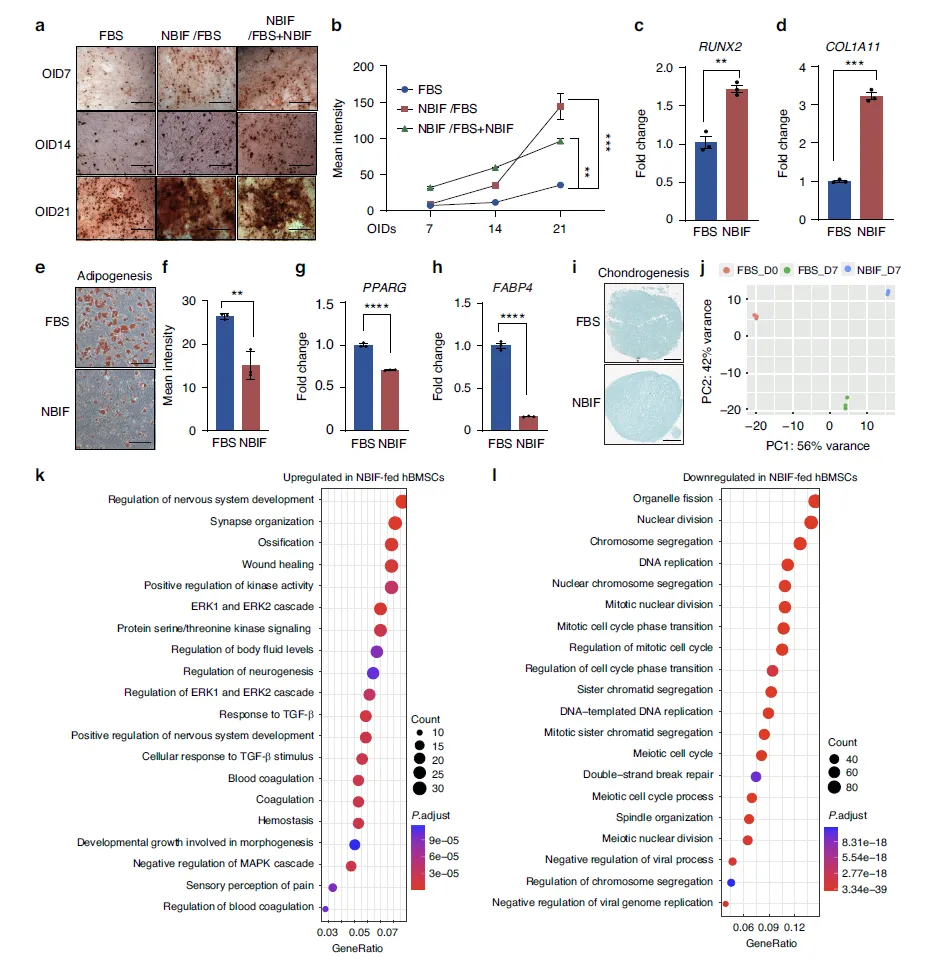
Figure 2:NBIF 对 hBMSCs 分化能力的调控及分子机制
此图聚焦 NBIF 对 hBMSCs 多向分化潜能的影响及转录组层面的分子变化。成骨诱导实验中,茜素红染色和 RT-PCR 结果显示,NBIF 培养的 hBMSCs 钙沉积量显著增加,成骨标志物 RUNX2 和 COL1A1 表达上调,成骨分化能力明显优于 FBS 组;而成脂分化相关的油红染色信号及 PPARG、FABP4 基因表达则显著降低,软骨分化能力未受明显影响,表明 NBIF 可特异性增强 hBMSCs 成骨分化潜能并抑制成脂分化。转录组分析显示,NBIF 组与 FBS 组 hBMSCs 存在 1614 个差异表达基因,上调基因富集于神经发育、骨形成等组织修复相关通路,下调基因则与 DNA 复制、细胞增殖及炎症信号通路相关,且主要 MHCⅠ 类和 Ⅱ 类基因表达降低,提示 NBIF 可能降低 hBMSCs 免疫原性。进一步的 Luminex 分析发现,NBIF 培养的 hBMSCs 分泌的组织修复相关因子(如 FGF2、HGF、CXCL12)显著增加,而 VEGF 分泌减少,表明培养环境可调控 hBMSCs 的分泌因子谱。
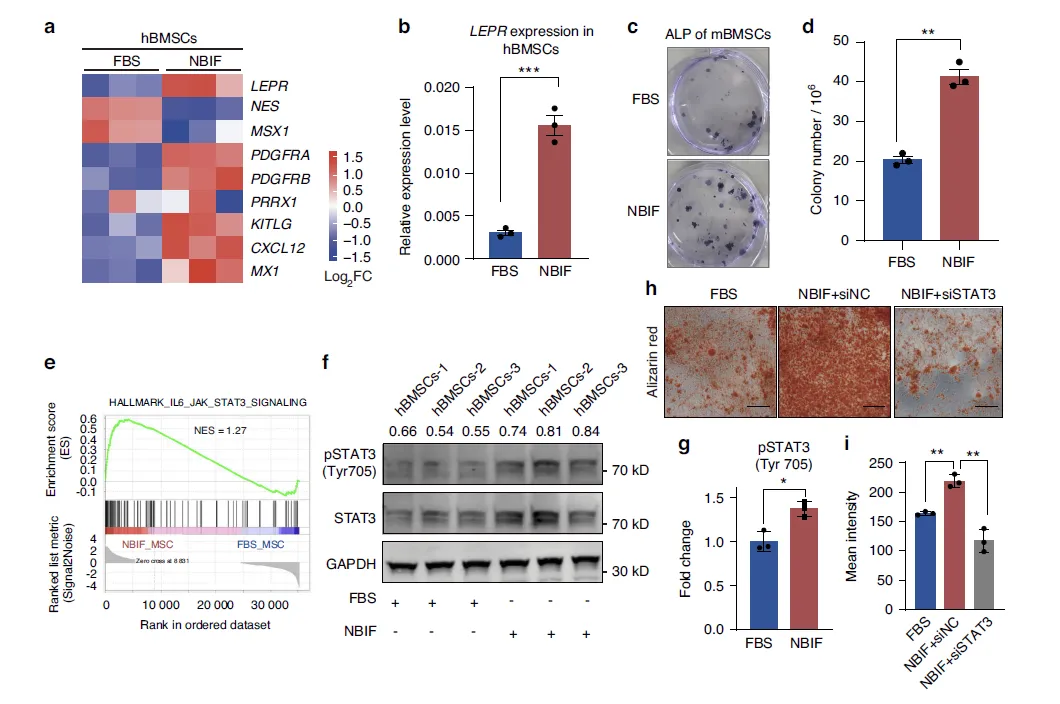
Figure 3:NBIF 维持 hBMSCs 自我更新能力的分子通路
该图通过基因表达分析、功能实验及通路验证,揭示了 NBIF 支持 hBMSCs 自我更新的机制。转录组数据显示,NBIF 培养的 hBMSCs 中,成骨祖细胞相关基因(如 LEPR、PDGFR、PRRX1 等)表达显著上调,其中 LEPR 作为骨髓成骨祖细胞特异性标志物,其高表达经 qRT-PCR 验证;小鼠 BMSCs 的 CFU-F 实验也显示,NBIF 组碱性磷酸酶阳性集落数显著多于 FBS 组,证明 NBIF 能增强 BMSCs 自我更新能力。GO 和 GSEA 分析发现,NBIF 组 hBMSCs 的 ERK/MAPK、JAK-STAT3 等多条信号通路被激活,其中 JAK-STAT3 通路关键,抑制剂 AG490 和 siRNA 介导的 STAT3 敲低均能显著降低 NBIF 诱导的 LEPR、RUNX2 表达,且抑制成骨矿化,Western blot 结果也显示 NBIF 组 hBMSCs 中磷酸化 STAT3(Tyr705)水平升高,表明 NBIF 可能通过激活 JAK-STAT3 通路促进 BMSCs 增殖和成骨潜能。
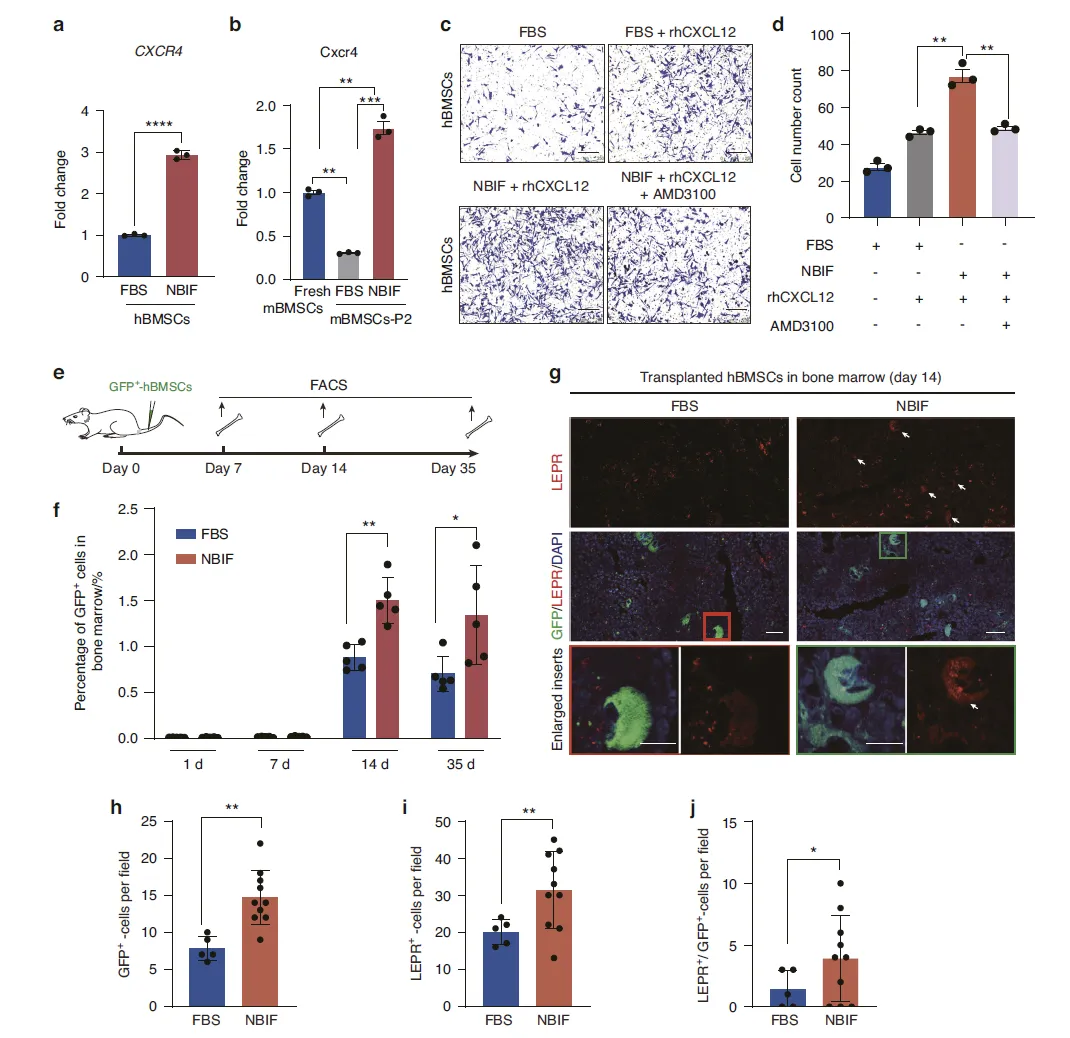
Figure 4:NBIF 增强 hBMSCs 骨髓归巢能力的机制
此图围绕 NBIF 对 hBMSCs 归巢能力的调控展开,核心聚焦 CXCL12-CXCR4 信号轴。qRT-PCR 结果显示,NBIF 培养的 hBMSCs 和原代小鼠 BMSCs 中 CXCR4 表达显著升高,而 FBS 培养 2 代后 mBMSCs 的 Cxcr4 表达则明显下调;Transwell 迁移实验表明,NBIF 组 hBMSCs 迁移能力显著增强,且对重组人 CXCL12 的响应性更高,而 CXCR4 拮抗剂 AMD3100 可消除这一增强效应,证实 CXCR4 表达上调是 NBIF 提升 hBMSCs 迁移能力的关键。体内实验中,GFP 标记的 NBIF 组 hBMSCs 经静脉注射后,在免疫缺陷小鼠骨髓中 14 天和 35 天的定植比例显著高于 FBS 组,免疫荧光染色也显示更多 GFP + 细胞及 GFP+/LEPR + 细胞驻留于骨髓,表明 NBIF 通过上调 CXCR4 表达,增强了 hBMSCs 向骨髓的归巢能力。
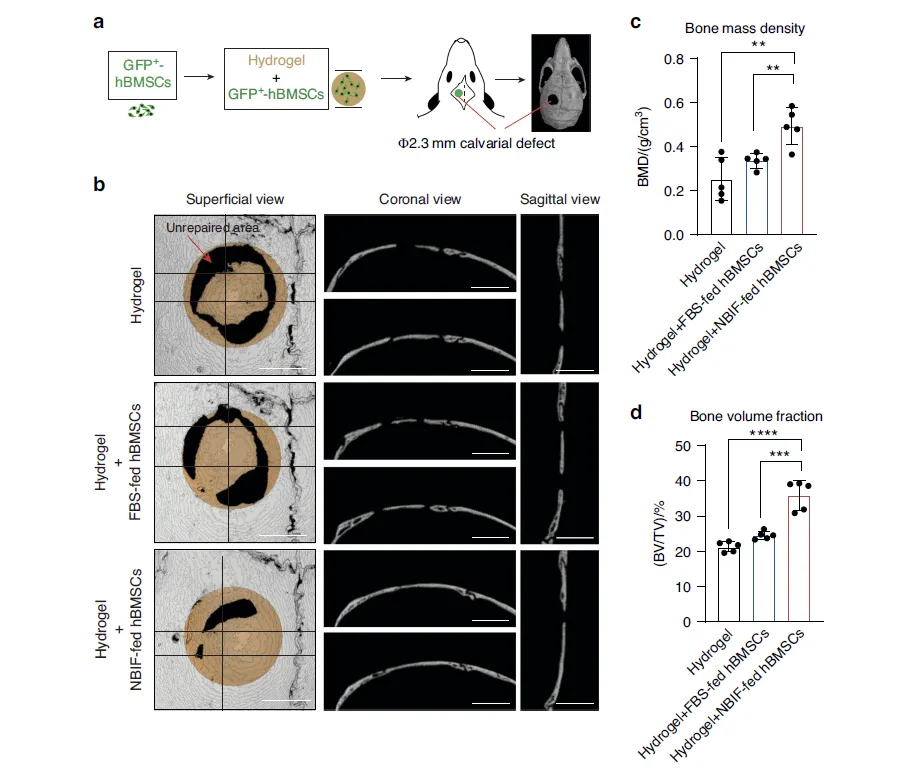
Figure 5:NBIF 预处理 hBMSCs 在体内的骨再生效果
该图通过小鼠颅骨缺损模型,验证了 NBIF 预处理 hBMSCs 的体内骨再生潜力。实验将负载 NBIF 培养 hBMSCs、FBS 培养 hBMSCs 的水凝胶支架及空白水凝胶分别植入小鼠 2.3mm 颅骨缺损处,7 周后 Micro-CT 扫描显示,NBIF 组骨缺损修复率达 34%,显著高于 FBS 组的 20% 和空白水凝胶组。定量分析表明,NBIF 组的骨矿物质密度(BMD)和骨体积分数(BV/TV)均显著高于其他两组,说明 NBIF 预处理的 hBMSCs 能更有效地促进颅骨缺损区域的骨组织结构修复和功能再生,为骨缺损治疗提供了更优的干细胞来源。
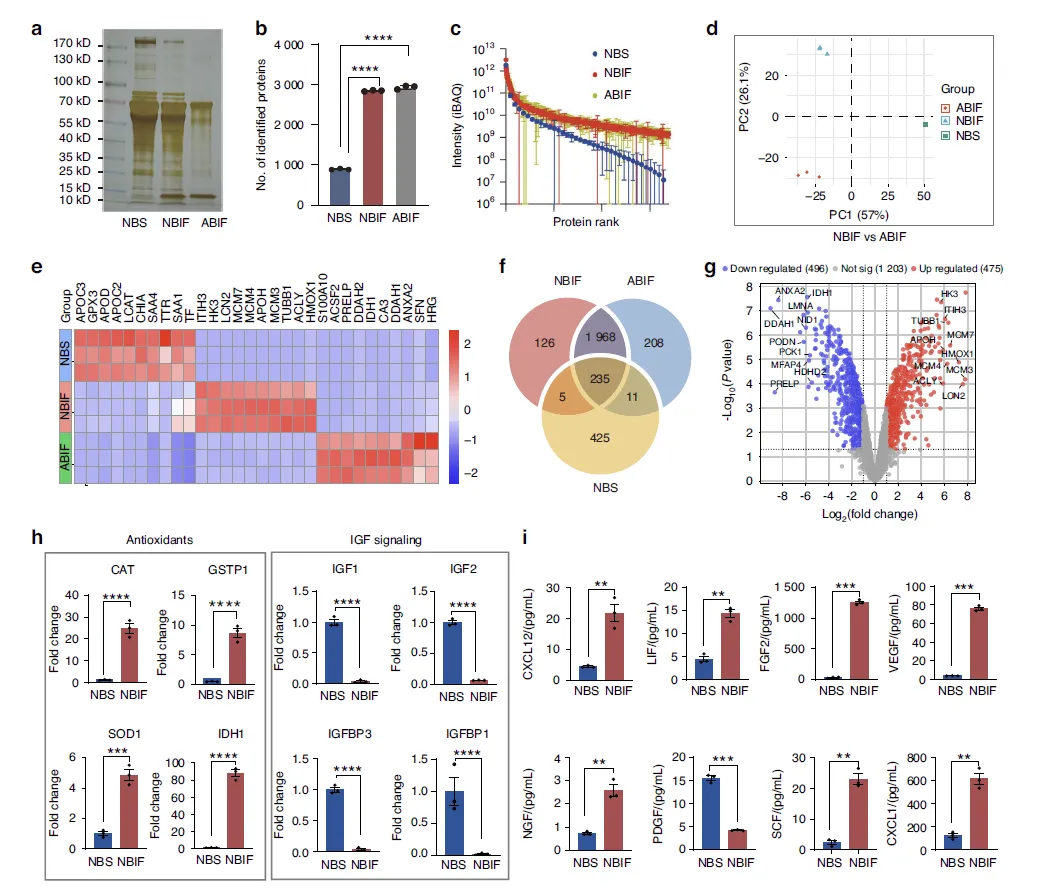
Figure 6:NBIF、NBS 及 ABIF 的蛋白质组学差异分析
此图通过蛋白质组学技术,对比了 NBIF、新生牛血清(NBS)和 ABIF 的蛋白质组成差异。质谱分析鉴定出 NBIF 含 2847 种蛋白质,ABIF 含 2934 种,NBS 仅含 891 种,三者蛋白质丰度分布和 PCA 分析均显示明显的分组差异,表明其生物学功能存在本质区别。NBIF 与 ABIF 共有 2203 种蛋白质,其中 475 种在 NBIF 中上调,496 种下调;NBIF 与 NBS 仅共有 240 种蛋白质,NBIF 独有的 2094 种蛋白质主要参与谷胱甘肽代谢(增强抗氧化能力)、核糖核苷一磷酸代谢(调控细胞增殖分化)等通路。此外,NBIF 中抗氧化酶(CAT、GSTP1 等)富集,胰岛素信号相关蛋白(IGF1、IGFBP1 等)下调,且 Luminex 分析显示 NBIF 中 NGF、bFGF、HGF 等细胞因子和生长因子水平显著高于 NBS,这些成分差异可能是 NBIF 调控 hBMSCs 功能的物质基础。
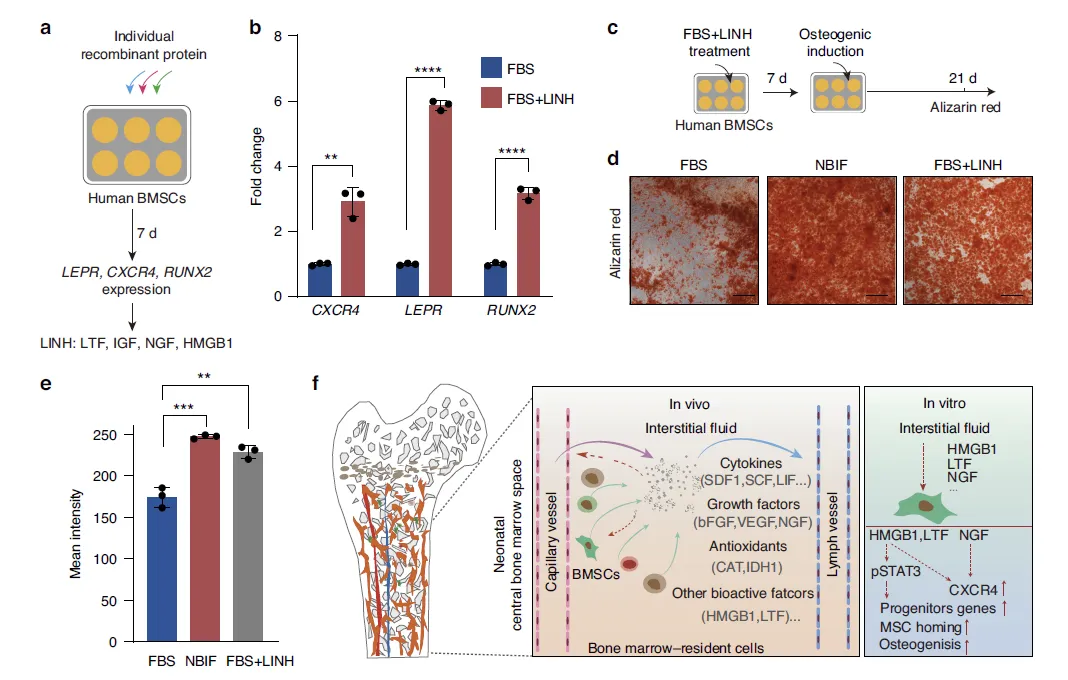
Figure 7:NBIF 中关键活性因子的筛选及功能验证
该图旨在筛选 NBIF 中调控 hBMSCs 功能的关键活性因子并验证其效果。通过 HPLC 对 NBIF 进行分子量分级,发现 25-100kD 的 BM3 组分能模拟 NBIF 的成骨促进效应,该分子量范围包含 HMGB1、LTF、NGF 等 56 种 NBIF 富集配体。单独重组蛋白实验显示,LTF、NGF、HGF 可上调 CXCR4 表达,HMGB1、NGF 能增加 LEPR 表达,NGF、IGF1 可轻度提升 RUNX2 表达;进一步优化浓度后,HMGB1(1000ng/mL)、IGF1(50ng/mL)、LTF(1000ng/mL)和 NGF(500ng/mL)组成的 “LINH 鸡尾酒”,能显著上调 hBMSCs 中 LEPR、RUNX2、CXCR4 的表达,且成骨诱导后的茜素红染色定量结果显示,其成骨分化促进效果与 NBIF 相当,证实该因子组合可部分模拟 NBIF 对 hBMSCs 成骨分化和骨髓归巢能力的调控作用。图中总结模型也明确,NBIF 中的细胞因子、生长因子、抗氧化蛋白等通过促进 LEPR 和 CXCR4 表达,经 JAK-STAT3 等通路增强 BMSCs 成骨能力和归巢能力。
本研究证实新生儿骨髓间质液(NBIF)是维持 hBMSCs 功能的关键微环境成分,其通过富含的 NGF、LTF、HMGB1 等活性因子,激活 JAK-STAT3 通路增强干细胞自我更新和成骨分化能力,通过上调 CXCR4 表达强化 CXCL12-CXCR4 介导的骨髓归巢。NBIF 可替代 FBS 用于 hBMSCs 体外培养,且其关键活性因子组合(LINH 鸡尾酒)能模拟其核心功能。该发现揭示了骨髓间质液的年龄相关功能差异,为优化干细胞体外培养体系、提升骨再生治疗效果提供了新的生物活性试剂和分子靶点,具有重要的临床转化价值。
局限性:主要聚焦 NBIF 的蛋白质成分,未探究代谢物等其他组分的作用;LINH 鸡尾酒的体内长期效果及临床适用性尚未充分验证。展望:后续需深入分析 NBIF 中代谢物、外泌体等其他成分的功能;扩大 LINH 鸡尾酒的体内实验规模,优化剂量和给药方式;探索其在其他组织再生中的应用,推动该策略向临床转化。
文章来源:Zhang J, Ma T, Ke L, et al. Neonatal bone marrow interstitial fluid supports expansion and osteogenic ability of human bone marrow mesenchymal stromal cells. Bone Res. 2025;13(1):102. Published 2025 Dec 15. doi:10.1038/s41413-025-00496-z
#新生儿骨髓间质液#hBMSCs#成骨分化#骨髓归巢#LINH鸡尾酒#骨再生#干细胞疗法#JAKSTAT3通路

国家杰青一对一答疑视频
医学省自然申请答疑,立项的关键条件是哪一些?从哪些方向可以杀出重围
临床型博士如何准备国青标书?没有预实验怎么办?专家一对一解答规划
中医药科研研究