深圳理工大学 | 从激素到骨骼:FSHβ 转录调控,解锁骨质疏松治疗新路径
- 2026-04-07 23:08:02

导读
本研究围绕绝经后骨质疏松发病机制展开,以卵巢切除(OVX)小鼠模拟绝经状态,首先证实C/EBPβ是垂体FSHβ的转录因子并直接结合其启动子,调控 FSHβ 表达;进一步发现AEP可正向调控 C/EBPβ,进而促进 FSHβ 合成,而 FSH 升高会激活破骨细胞、加速骨吸收引发骨质疏松;随后使用 AEP 特异性抑制剂 #11a 干预,证实其可抑制 C/EBPβ、降低 FSH 水平,同时促进成骨分化、抑制破骨生成,且疗效与 FDA 获批药物特立帕肽相当;此外,TrkB 激动剂 CF3CN 虽能改善骨质疏松,但因垂体缺乏 TrkB 受体无法降低 FSH,仅作用于骨骼局部。最终明确 C/EBPβ/AEP 通路是绝经后 FSHβ 转录的关键调控轴,靶向 AEP 可有效缓解骨质疏松。
注:该文章发表于《Bone Research》,该期刊是由四川大学与Springer Nature合作出版的英文期刊,最新影响因子为15,位列JCR分区Q1区。
首次证实C/EBPβ 直接调控垂体 FSHβ 转录,揭示 AEP 对该通路的正向反馈作用;明确 AEP 抑制剂 #11a 可同时抑制 FSH 合成与骨吸收、促进骨形成,疗效媲美特立帕肽;阐明 TrkB 激动剂与 AEP 抑制剂的差异化作用机制,为绝经后骨质疏松提供全新靶点。
动物层面选用 C57BL6/J 野生型、C/EBPβ±、AEP⁻/⁻、BDNF± 雌性小鼠,构建OVX 绝经模型与假手术组,分别给予 AEP 抑制剂 #11a、TrkB 激动剂 CF3CN/R13、特立帕肽干预,检测子宫重量、血清 FSH/LH、骨密度、骨微结构(μCT)、骨组织形态学(H&E、TRAP、钙黄绿素双标);细胞实验采用大鼠原代垂体细胞、MC3T3-E1 成骨细胞、RAW264.7 破骨细胞,通过慢病毒过表达 / 敲降 C/EBPβ,结合 GnRH、E2 处理,检测 FSHβ 等基因与蛋白表达;分子机制采用ChIP、EMSA、荧光素酶报告基因验证 C/EBPβ 与 FSHβ 启动子结合,同时检测 AEP 酶活性、信号通路蛋白(Akt、ERK、CREB)磷酸化水平,统计学采用 t 检验与单 / 双因素 ANOVA 分析。
C/EBPβ 可直接结合 FSHβ 启动子并调控其转录,敲除 / 敲降 C/EBPβ 显著降低垂体 FSHβ 水平,且不影响 LH;AEP 敲除或抑制剂 #11a 可抑制 C/EBPβ 活性,进而降低 OVX 小鼠血清与垂体 FSHβ,TrkB 激动剂因垂体无 TrkB 受体无法降低 FSH;#11a 与 CF3CN 均能改善 OVX 小鼠骨微结构、提升骨密度,减少骨髓脂肪增生,#11a 疗效与特立帕肽相当;细胞水平证实 #11a 与 CF3CN 可促进成骨分化、抑制破骨生成,上调 OPG、Runx2、Osterix,下调 RANKL 与 AEP 活性;OVX 激活骨与脑内 C/EBPβ/AEP/FSHR 轴,#11a 可同时阻断该通路在骨骼与中枢的激活。
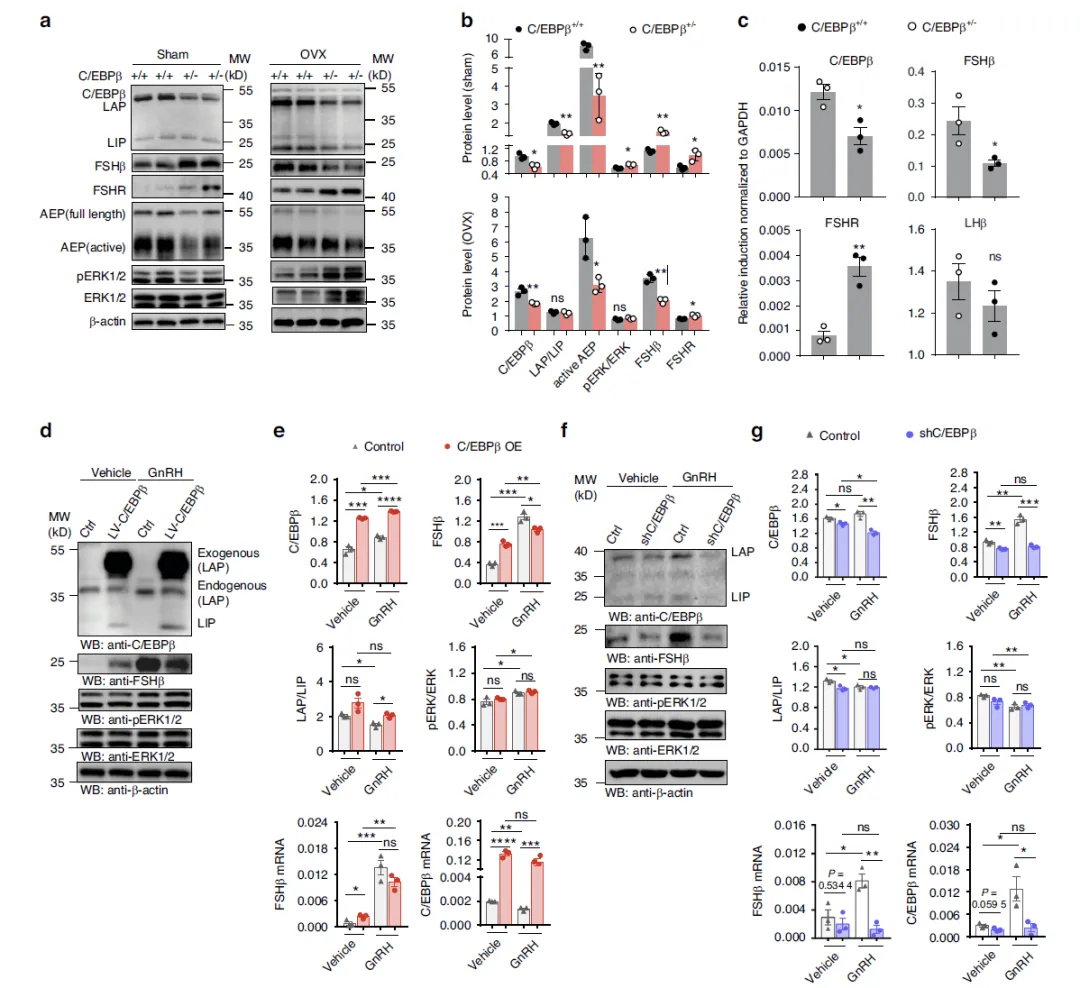
Figure 1:C/EBPβ 在体内外调控垂体 FSHβ 的表达
这张图通过动物体内实验与垂体原代细胞体外实验,系统证明 C/EBPβ 是垂体 FSHβ 表达的关键调控因子。在卵巢切除(OVX)与假手术小鼠中,C/EBPβ 杂合缺失会显著降低垂体 FSHβ 蛋白与 mRNA 水平,而不影响 LHβ,同时伴随 AEP 下降、ERK 通路激活以及 GnRHR 表达上升,提示 C/EBPβ 对 FSHβ 具有正向转录调控作用,并对 GnRHR 存在负反馈抑制。在大鼠原代垂体细胞中,过表达 C/EBPβ 可直接提高基础状态下 FSHβ 的表达,而在 GnRH 刺激下则呈现一定的负向调节;敲低 C/EBPβ 则明显削弱 GnRH 诱导的 FSHβ 上升。整体结果说明,C/EBPβ 作为 GnRH 下游的核心转录因子,直接决定垂体 FSHβ 的转录水平,同时参与信号反馈调节。
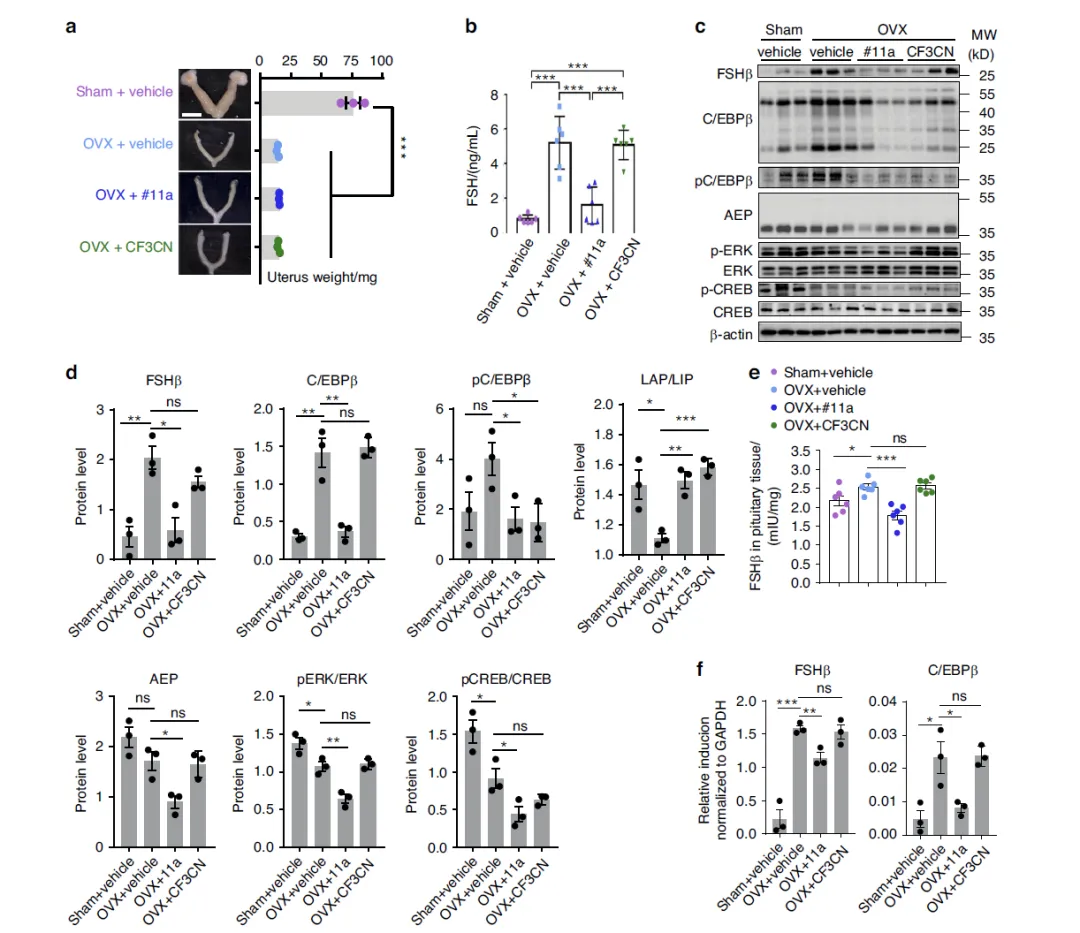
Figure 2:AEP 抑制剂 #11a 特异性抑制 OVX 诱导的 FSH 升高,TrkB 激动剂 CF3CN 无此作用
这张图重点阐明 AEP 抑制剂 #11a 与 TrkB 激动剂 CF3CN 在调控 FSH 方面的差异。结果显示,OVX 手术成功造成小鼠子宫萎缩,并显著升高血清与垂体 FSH 水平;口服 #11a 可明显降低 OVX 引起的 FSHβ、C/EBPβ、磷酸化 C/EBPβ 以及成熟 AEP 的表达,同时抑制垂体 FSH 合成与分泌,而 CF3CN 对这些指标几乎无影响。进一步检测发现,垂体组织几乎不表达 TrkB 受体,因此 TrkB 激动剂无法作用于垂体调控 FSH。这些结果证明,#11a 通过直接抑制 AEP–C/EBPβ 通路,在垂体层面选择性阻断 FSHβ 的合成,而 CF3CN 不具备中枢抑制 FSH 的能力。
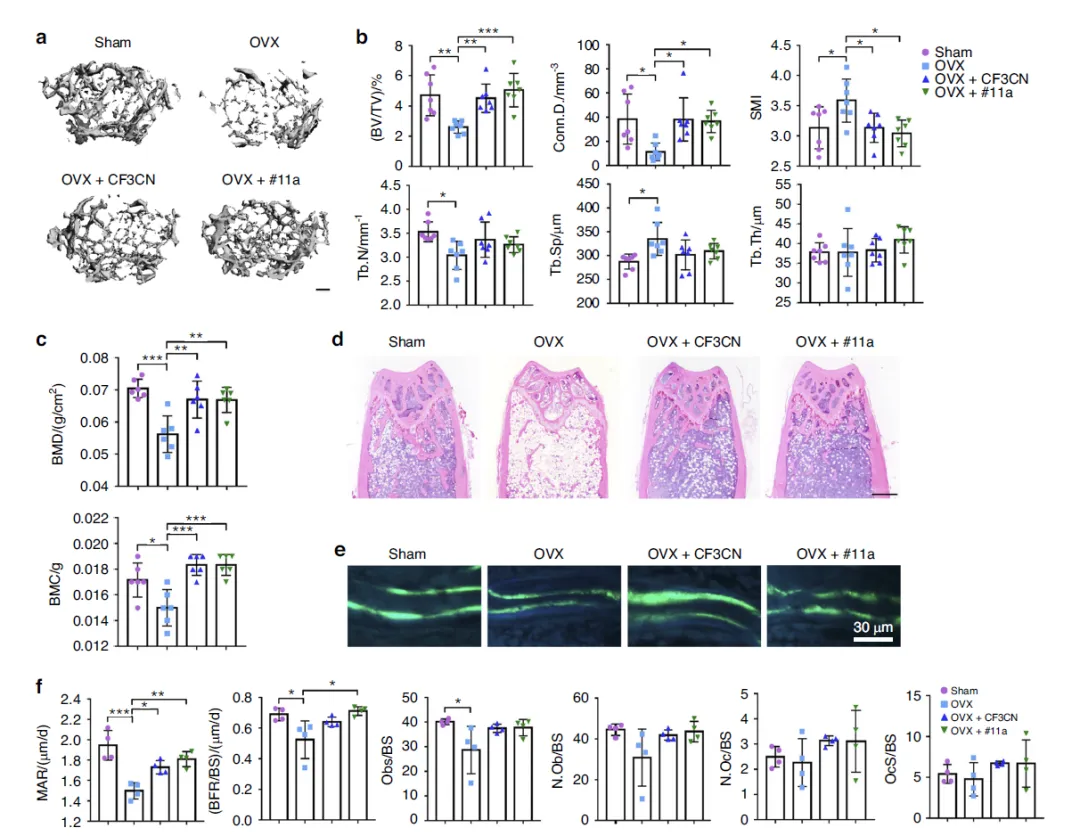
Figure 3:#11a 与 CF3CN 均可改善 OVX 诱导的小鼠骨质疏松,抑制骨转换
这张图从骨骼结构、密度、组织形态与动态骨形成等层面,证实 #11a 和 CF3CN 对绝经后骨质疏松的治疗效果。μCT 结果显示,OVX 显著降低骨体积分数、连接密度与骨小梁数量,增加骨小梁分离度,而 #11a 与 CF3CN 均可逆转上述指标,提升骨微结构质量;DXA 检测表明两种药物均能恢复 OVX 降低的骨密度与骨矿含量。H&E 染色显示药物可减少 OVX 引起的骨髓脂肪化,钙黄绿素双标结果提示药物能恢复骨形成率与矿化沉积率,局部区域分析还显示两者均可降低破骨细胞数量与表面占比。整体说明,#11a 与 CF3CN 通过抑制骨吸收、促进骨形成,有效缓解 OVX 诱导的骨质疏松。
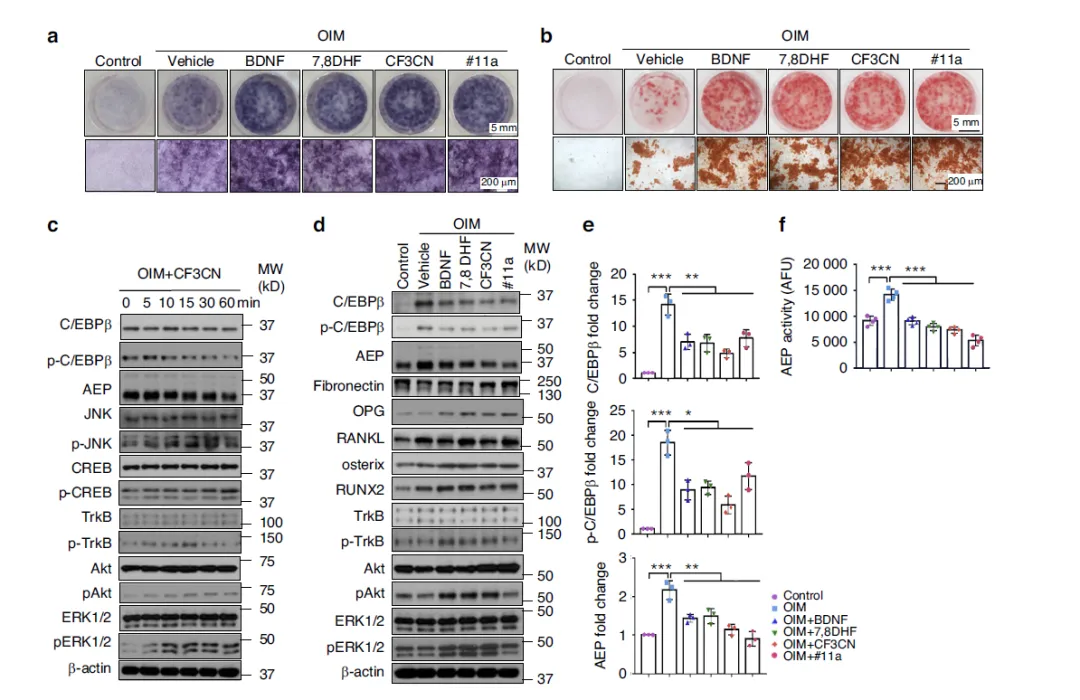
Figure 4:#11a 与 CF3CN 促进成骨细胞分化与矿化,抑制 C/EBPβ/AEP 通路
这张图在细胞水平揭示两种药物促进骨形成的机制。在成骨诱导液刺激的 MC3T3-E1 细胞中,#11a、CF3CN、BDNF 及其激动剂 7,8-DHF 均可增强碱性磷酸酶活性与钙结节沉积,促进成骨分化。机制上,CF3CN 快速激活 TrkB–Akt–ERK–CREB 通路,进而抑制 C/EBPβ 与 AEP;#11a 则直接抑制 AEP 酶活,下调 C/EBPβ/AEP 信号。两种药物均能上调成骨关键因子 Runx2、Osterix 以及骨保护素 OPG,对 RANKL 无明显影响。结果表明,#11a 与 CF3CN 通过不同上游通路汇聚于抑制 C/EBPβ/AEP,实现促进成骨分化、提升骨形成能力的效果。
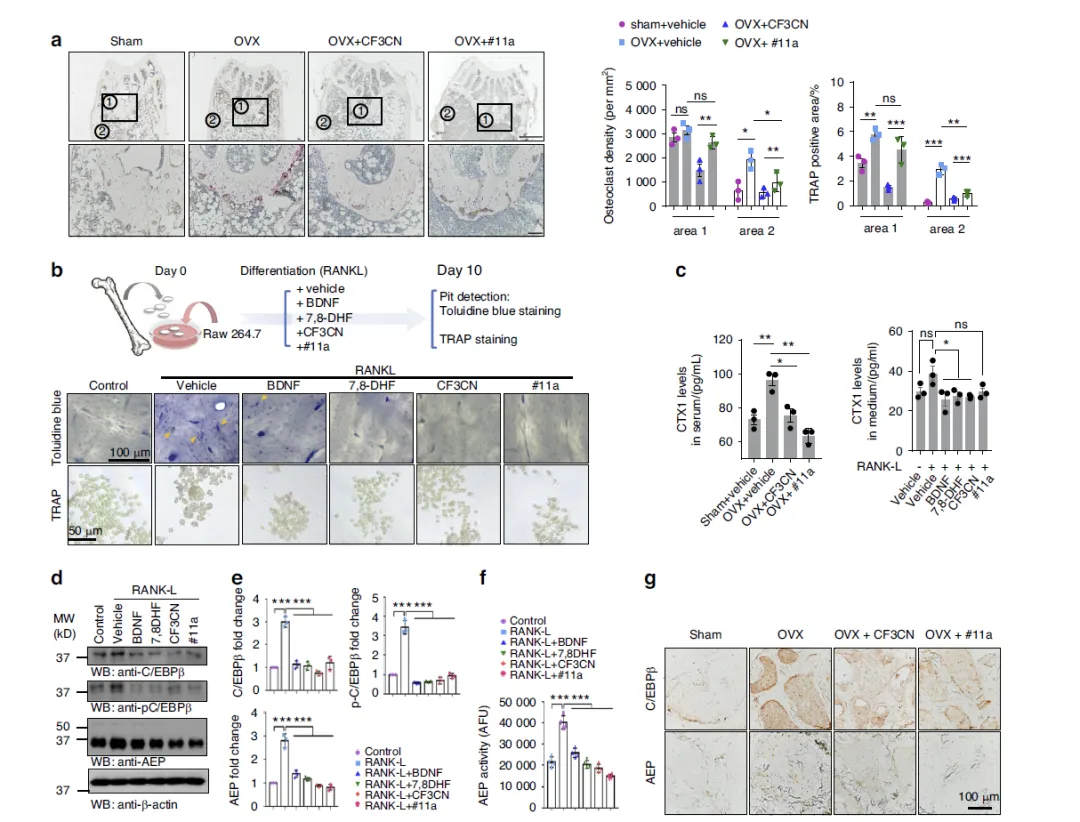
Figure 5:#11a 与 CF3CN 抑制破骨细胞生成与骨吸收功能
这张图聚焦破骨细胞,证明 #11a 与 CF3CN 可阻断 RANKL 诱导的破骨发生。动物实验中,OVX 显著增加股骨破骨细胞数量与密度,#11a 与 CF3CN 均可使其下降;细胞实验显示,在 RANKL 诱导的 RAW264.7 细胞中,两种药物能减少破骨细胞形成、降低骨吸收陷窝面积,并下调骨吸收标志物 CTX-1。机制上,RANKL 可激活 C/EBPβ/AEP 通路,而 #11a、CF3CN、BDNF、7,8-DHF 均能抑制 C/EBPβ 磷酸化、AEP 表达与酶活。免疫组化也证实,药物可降低 OVX 小鼠骨组织中 C/EBPβ 与 AEP 的信号。整体说明,两种药物通过抑制 C/EBPβ/AEP 通路,直接阻断破骨分化与骨吸收,发挥骨保护作用。
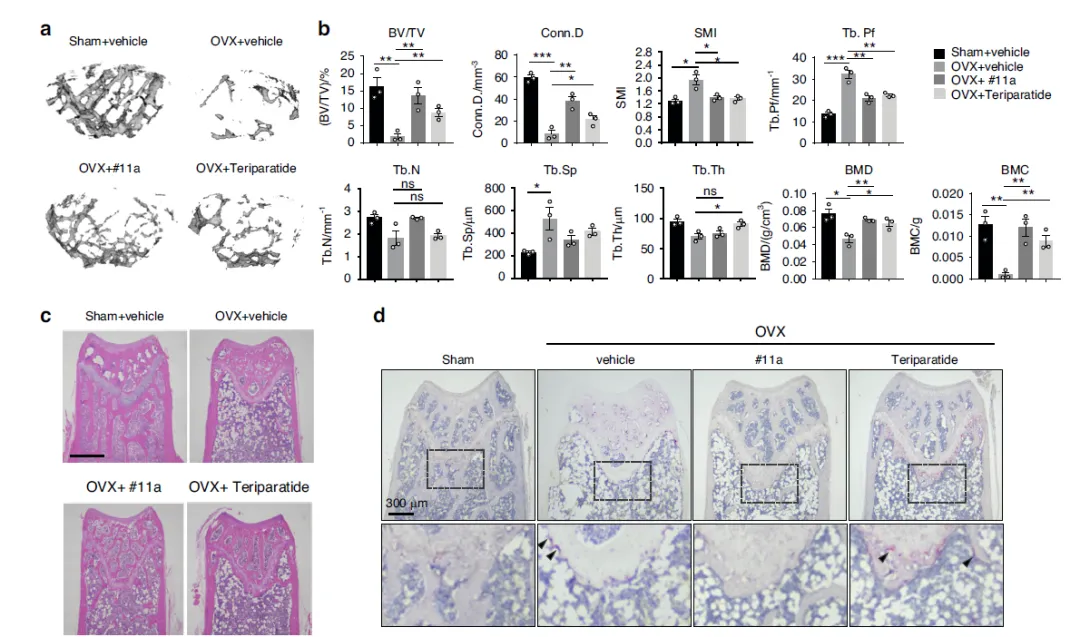
Figure 6:AEP 抑制剂 #11a 抗骨质疏松效果与 FDA 获批药特立帕肽相当
这张图通过头对头比较,确立 #11a 作为骨质疏松候选药物的疗效价值。在 OVX 小鼠中,#11a 与特立帕肽干预后,μCT 检测的骨体积分数、连接密度、骨小梁数量等结构指标均显著回升,骨分离度下降;DXA 结果显示两者均可恢复骨密度与骨矿含量;H&E 染色可见骨髓脂肪化减少,骨小梁更密集;TRAP 染色显示破骨细胞数量明显下降。各项指标均证明,#11a 在改善骨微结构、提升骨密度、抑制骨吸收方面,与已上市的成骨性药物特立帕肽效果相当,具备成为新型抗骨质疏松药物的潜力。
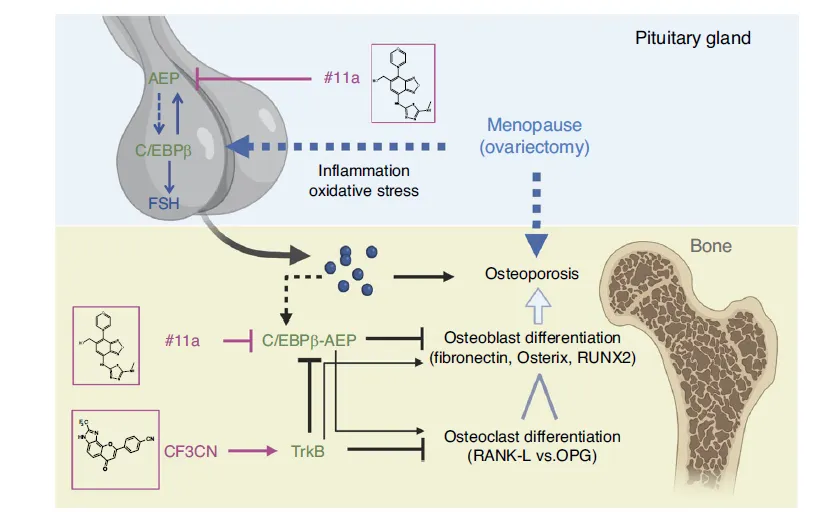
Figure 7:AEP 抑制剂与 TrkB 激动剂抗骨质疏松的差异化机制模式图
这张模式图整合全文机制,清晰展示绝经后骨质疏松的调控通路与药物作用位点。绝经 / OVX 引发炎症与氧化应激,激活垂体 C/EBPβ,进而直接转录上调 FSHβ,使 FSH 升高并作用于骨骼,激活 C/EBPβ/AEP 通路,促进破骨、抑制成骨,最终导致骨质疏松。AEP 抑制剂 #11a 可同时在垂体抑制 C/EBPβ–FSH 轴,并在骨骼阻断 AEP、保护纤连蛋白、提升 OPG,实现 “中枢降 FSH + 外周护骨” 双重作用;而 TrkB 激动剂 CF3CN 因垂体无 TrkB,无法降低 FSH,仅在骨骼局部激活 TrkB–Akt 通路抑制 C/EBPβ/AEP,促进骨形成、抑制骨吸收。该图直观揭示两种药物的作用差异与关键通路靶点。
本研究证实C/EBPβ 是垂体 FSHβ 转录的关键转录因子,AEP 通过正向调控 C/EBPβ 促进 FSHβ 合成,形成 C/EBPβ/AEP/FSH 调控轴,介导绝经后骨质疏松发生;AEP 特异性抑制剂 #11a 可阻断该通路,降低 FSH 水平,同时促进成骨、抑制破骨,发挥显著抗骨质疏松作用,疗效与特立帕肽相当;TrkB 激动剂仅作用于骨骼局部改善骨代谢,无法调控垂体 FSH;该研究明确绝经后骨质疏松的全新分子机制,为 AEP 作为治疗靶点提供坚实实验依据。
局限:仅在小鼠模型验证,未开展临床试验;未探索 #11a 长期用药安全性。展望:推进 #11a 临床前研究,评估人体疗效与安全性;探索 C/EBPβ/AEP 通路与雌激素的协同调控机制,开发更精准的骨质疏松靶向药物。
文章来源: Xie Z, Liao J, Xiong J, Zhao Z, Ye K. C/EBPβ dictates postmenopausal FSHβ transcription and blockade of AEP/C/EBPβ pathway alleviates osteoporosis. Bone Res. 2026 Mar 17;14(1):31. doi: 10.1038/s41413-026-00510-y. PMID: 41844581; PMCID: PMC12996317.

国家杰青一对一答疑视频
医学省自然申请答疑,立项的关键条件是哪一些?从哪些方向可以杀出重围
临床型博士如何准备国青标书?没有预实验怎么办?专家一对一解答规划
中医药科研研究
