Nat Chem|深圳湾实验室李刚团队揭示精氨酸的“另一面”:人类蛋白质组中的反应性与配体性地图
- 2026-05-09 15:19:22
点击蓝字
关注我们

尽管精氨酸在蛋白质结构稳定、酶催化、信号转导及液-液相分离等多种生物学过程中发挥着关键作用,其在人类蛋白质组层面的反应性(reactivity)与配体性(ligandability)仍长期缺乏系统性研究。这一认知空白显著限制了精氨酸作为潜在共价药物靶点的开发与利用。
2026年1月2日,深圳湾实验室李刚团队在 Nature Chemistry(IF = 20.7)在线发表题为 “Global profiling of arginine reactivity and ligandability in the human proteome”的研究论文,首次绘制了人类蛋白质组中精氨酸反应性与配体性的全局图谱。
在该研究中,研究人员结合基于活性的蛋白质组学(activity-based protein profiling, ABPP)与苯基乙二醛(phenylglyoxal)衍生化学探针,系统性构建了精氨酸反应性分析策略。通过对多种苯基乙二醛衍生物进行筛选,团队发现了一种覆盖范围更广、选择性更高的优化探针,能够在多种人类细胞系中对 4,606 个精氨酸位点进行定量分析。其中,一部分高反应性精氨酸残基被证实参与调控蛋白质的液-液相分离行为。
研究进一步结合珠上还原二甲基化蛋白质组学(on-bead reductive dimethylation proteomics)方法,对精氨酸反应性进行了独立验证,揭示了一类具有显著功能意义的高反应性精氨酸位点子集。
此外,研究团队采用数据独立采集的 ABPP(DIA-ABPP)策略开展竞争性片段筛选,系统评估了 60 种二羰基化合物与精氨酸残基的配位关系,构建了精氨酸配体性图谱。
该大规模数据集揭示了一批可被小分子共价修饰、并参与调控蛋白质活性,尤其是蛋白质-蛋白质相互作用(PPI)的精氨酸残基,明确了其作为潜在共价药物靶点的价值。
总之,该研究首次在蛋白质组层面系统描绘了精氨酸的反应性与配体性景观,深化了对精氨酸功能多样性的理解,并显著拓展了共价药物发现的靶点范围,将精氨酸纳入可药靶氨基酸的核心序列。
Abstract
01
摘要

Results
02 主要研究结果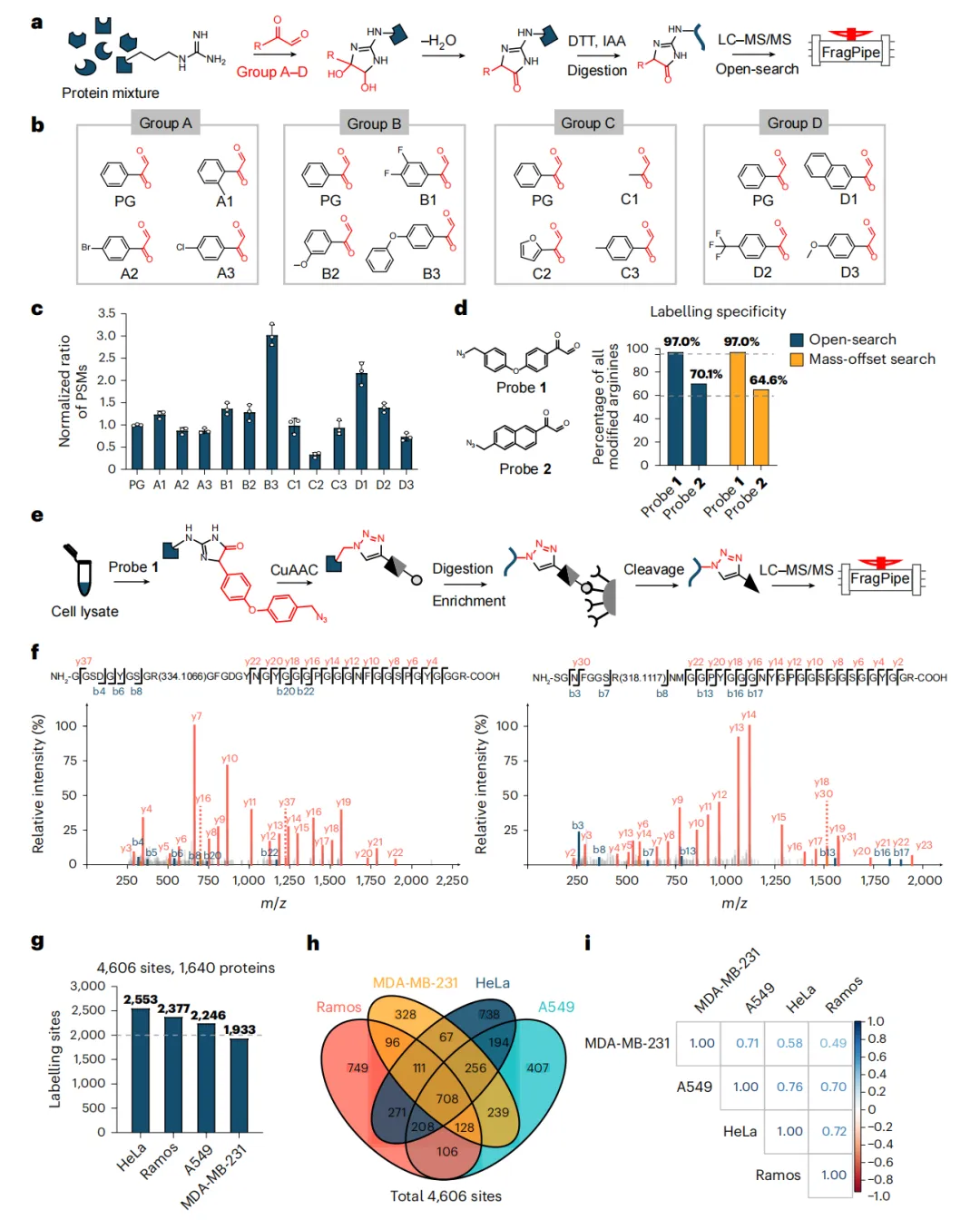
图1 | 人源蛋白质组中精氨酸修饰肽段的PG衍生物筛选。a、LC-MS/MS工作流程示意图及探针优化的开放式搜索分析。b、初始筛选中使用的13种PG衍生物结构与分组策略。c、以PG为内标时精氨酸修饰肽段的PSMs标准化数值。数据以三次生物学重复的平均值±标准差表示。d、通过开放式搜索和质量偏移搜索评估探针1和2的选择性,突出精氨酸特异性。水平虚线标记95%和60%特异性水平。e、优化后的化学蛋白质组学工作流程示意图,其中探针1富集前进行胰蛋白酶消化。f、探针1标记的精氨酸位点代表性MS/MS谱图,显示+334 Da或+318 Da质量偏移的共价修饰。g、探针1在多种人源细胞系中鉴定的精氨酸位点总数。h、不同细胞系间鉴定精氨酸位点的重叠情况。i、基于细胞系间精氨酸位点定量的Pearson相关系数热图。
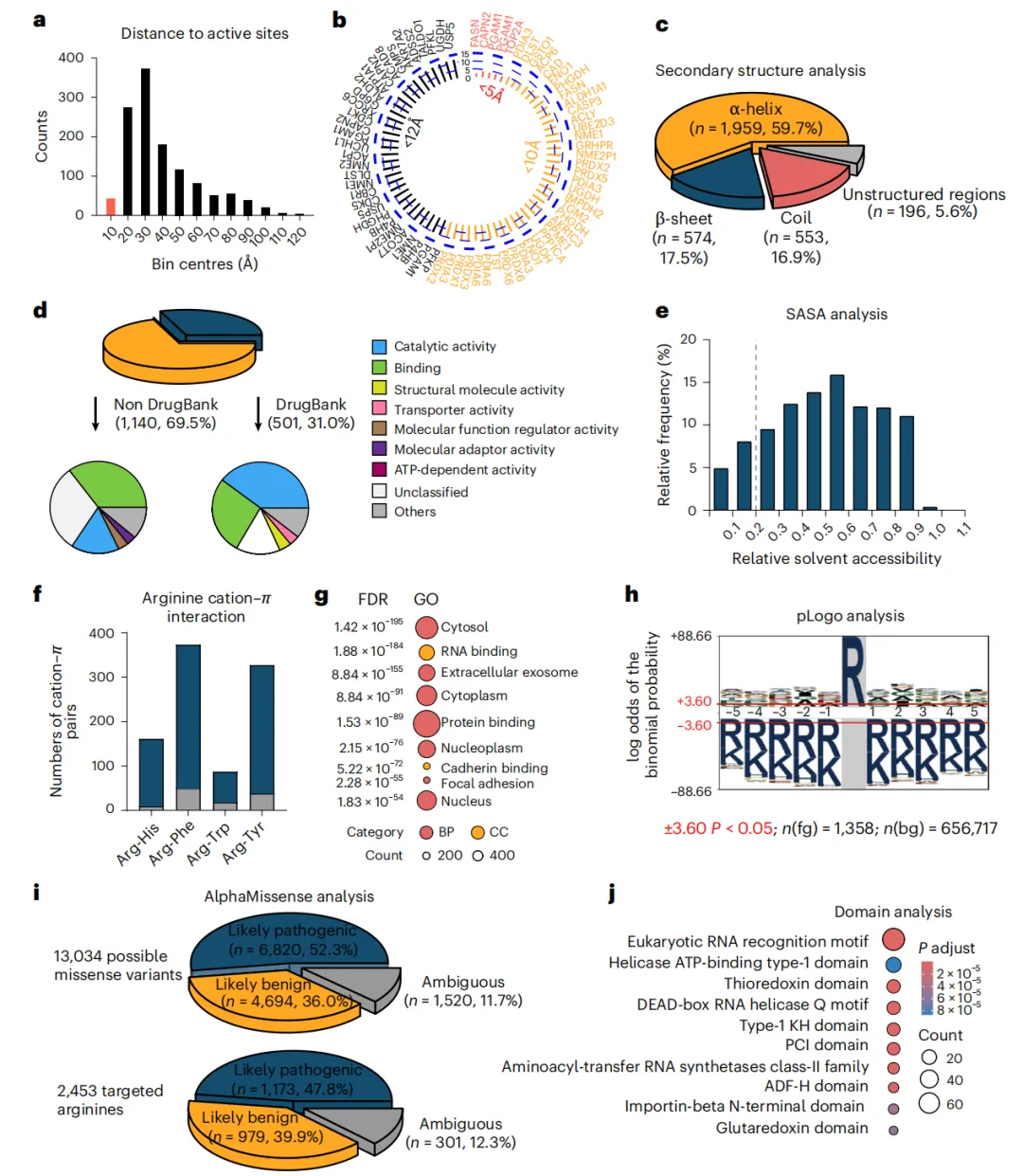
图2 | 标记精氨酸功能的生物信息学分析。a、直方图显示标记精氨酸与活性位点残基之间的距离分布。b、圆形柱状图分类显示位于活性位点5 A、10 A和12 A范围内的精氨酸数量。c、预测二级结构中标记精氨酸的比例:螺旋(包括三转角、四转角和五转角螺旋)、 β 片层(包括 β 链和 β 桥)、卷曲(包括 β 转角、弯曲和卷曲)以及非结构区域。d、DrugBank与非DrugBank条目中含标记精氨酸的蛋白质比例,各组按Panther数据库分类显示功能类别分布。e、标记精氨酸的相对溶剂可及表面积(RSA),溶剂暴露以20% RSA阈值定义,垂直虚线标示该阈值。f、基于AlphaFold结构模型预测的阳离子- π 相互作用分布。深蓝色条形表示距离阈值<6埃的相互作用,灰色条形表示同时满足二面角约束(<20°)的高置信度子集。g,GO分析显示含标记精氨酸的蛋白质主要功能。h,pLogo分析展示标记精氨酸周围的局部序列环境。n(fg),前景集大小;n(bg),背景/参考集大小。i,AlphaMissense预测评估2,453个比对精氨酸中13,034个可能错义变异的致病潜力。j,通过将标记精氨酸映射至prosite注释鉴定的富集蛋白质结构域。显著性通过双侧二项检验(经Benjamini-Hochberg校正,Q < 0.01)确定。
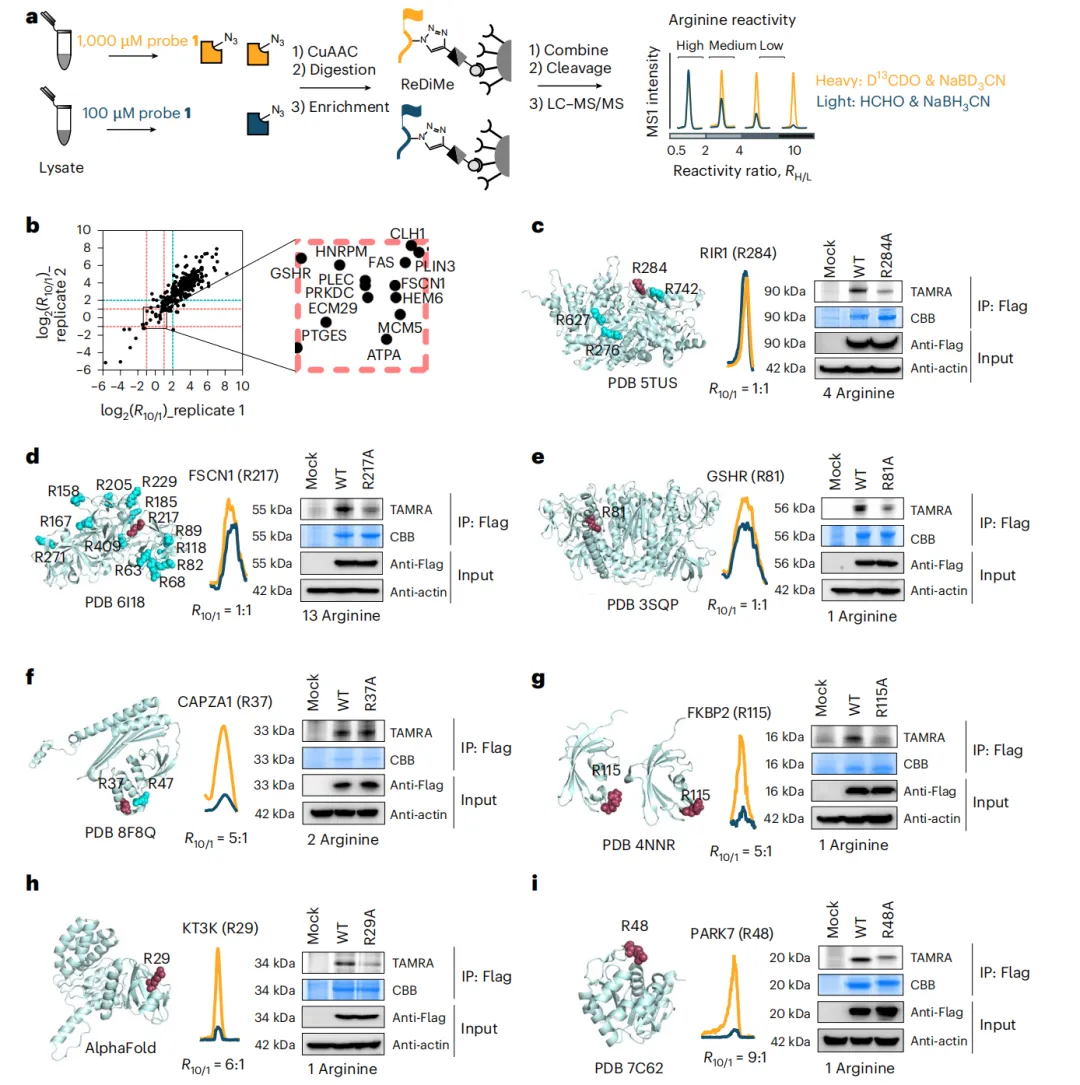
图3 | 人类蛋白质组中精氨酸反应性的定量分析。a,精氨酸反应性分析工作流程示意图。HeLa细胞蛋白质组经100 μM 或1 mM探针1处理后,采用ReDiMe定量蛋白质组学方法进行定量分析。b,显示两个生物学重复中log2(R10:1)值的相关性图。精氨酸位点根据其反应性分类:高反应性(−1 < log2(R10:1)< 1)、中等反应性(1 < log2(R10:1)< 2)和低反应性(log2(R10:1)> 2)。c–i,通过凝胶内荧光验证探针1在特定精氨酸位点的标记。在HEK293T蛋白质组中过表达重组野生型蛋白及其相应的精氨酸-丙氨酸突变体,并用探针1处理。在c–i中,分析的蛋白包括核糖核苷二磷酸还原酶大亚基(RIR1),含有高反应性R284(c);fascin(FSCN1),含有高反应性R217(d);谷胱甘肽还原酶(GSHR),含有高反应性R81(e);封端蛋白肌动蛋白丝Z线亚基α1(CAPZA1),含有低反应性R37(f);肽基脯氨酰顺反异构酶(FKBP2),含有单个低反应性精氨酸R115(g);酮胺-3-激酶(KT3K),含有单个低反应性R29(h);帕金森病蛋白7(PARK7),含有单个低反应性R48(i)。

图4 | 阿尔吉宁- π 相互作用介导的相分离。a,c,荧光成像比较野生型与突变型细胞,证实R269在UBQL2相分离中的功能作用(a)及R313在 NONO 相分离中的功能作用(c),采用抗Flag 488荧光标记。比例尺:5 μm 。n = 3个生物学独立重复实验。NS,无统计学意义。b,d,亚砷酸盐处理后野生型与R269K UBQL2细胞(b)及相同条件下野生型与R313K NONO 细胞(d)中斑点数量与大小的定量分析。中心线表示中位数,箱线限表示第25和第75百分位数。采用非配对双尾Student t检验进行统计分析,P值已标注。e,f,AlphaFold2预测结构显示:UBQL2中的R269与Y265形成阳离子- π 相互作用(e); NONO 中的R313在预测的异源二聚体模型 SFPQ 中与H90形成推定的阳离子- π 相互作用(f)。g,精氨酸介导的阳离子- π 相互作用调控 LLPS 的示意图。精氨酸突变破坏这些相互作用并损害相分离。
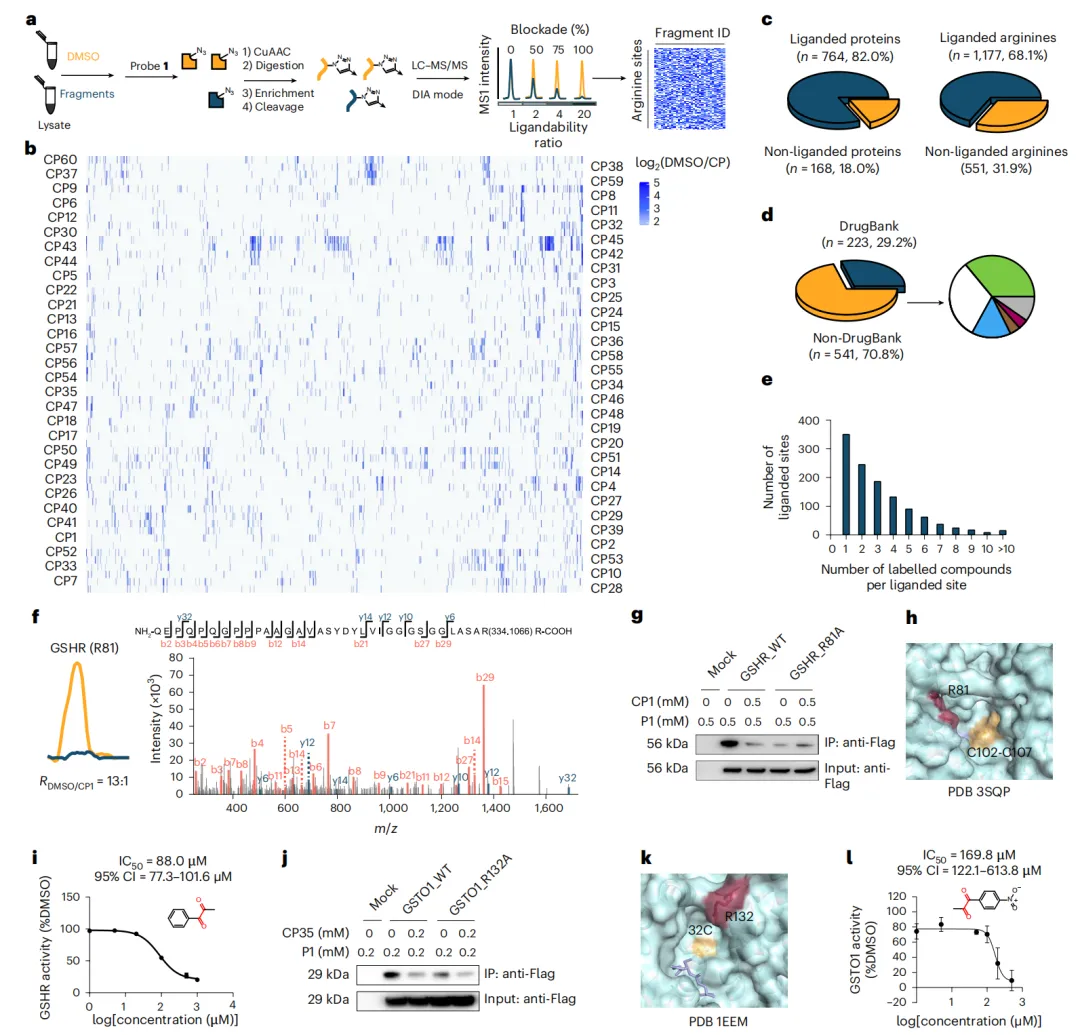
图5 | 人精氨酸位点中乙二醛化合物反应性的全局分布图。f,对应肽段的MS/MS谱图与蛋白质组对照。a,竞争性DIA- ABPP 提取离子色谱图(XICs)工作流程示意图。蓝色轨迹对应用于识别被乙二醛化合物配位的精氨酸。b,热图显示探针1标记的肽段在 GSHR 中与CP1竞争的 GSHR ,黄色轨迹表示未受CP1竞争的配位精氨酸位点的 RDMSO /CP值(DMSO与化合物的比值)。色谱图下方标注了乙二醛化合物库中(RDMSO /CP≥4)的层级聚类平均 RDMSO /CP1值。g,j,对行和列进行验证。细胞裂解液中配位精氨酸的欧氏距离用于分析。Western blot分析证实了选择性聚集的可配体精氨酸位点(柱状图)和乙二醛化合物(行)对HEK293T细胞裂解液中探针1标记的抑制作用,这些细胞表达野生型或根据(1 - Pearson相关系数)聚集以捕获 GSHR (g)和GSTO1(j)的精氨酸-丙氨酸突变体版本。h,k,反应性谱相似性的结构。c,配体化蛋白质的比例(左)展示了 GSHR(PDB 3SQP;h)和GSTO1(PDB 1EEM;k),配体化和精氨酸(右)相对于定量蛋白质的总数,红色高亮显示活性位点,黄色显示酶底物或精氨酸。d,配体化蛋白质的分布分类为DrugBank和配体(紫色)。i,l,半抑制浓度曲线显示CP非DrugBank条目对酶活性的抑制。 GSHR (i)的功能类别分布由Panther 1分类,GSTO1(l)由CP 35分类。
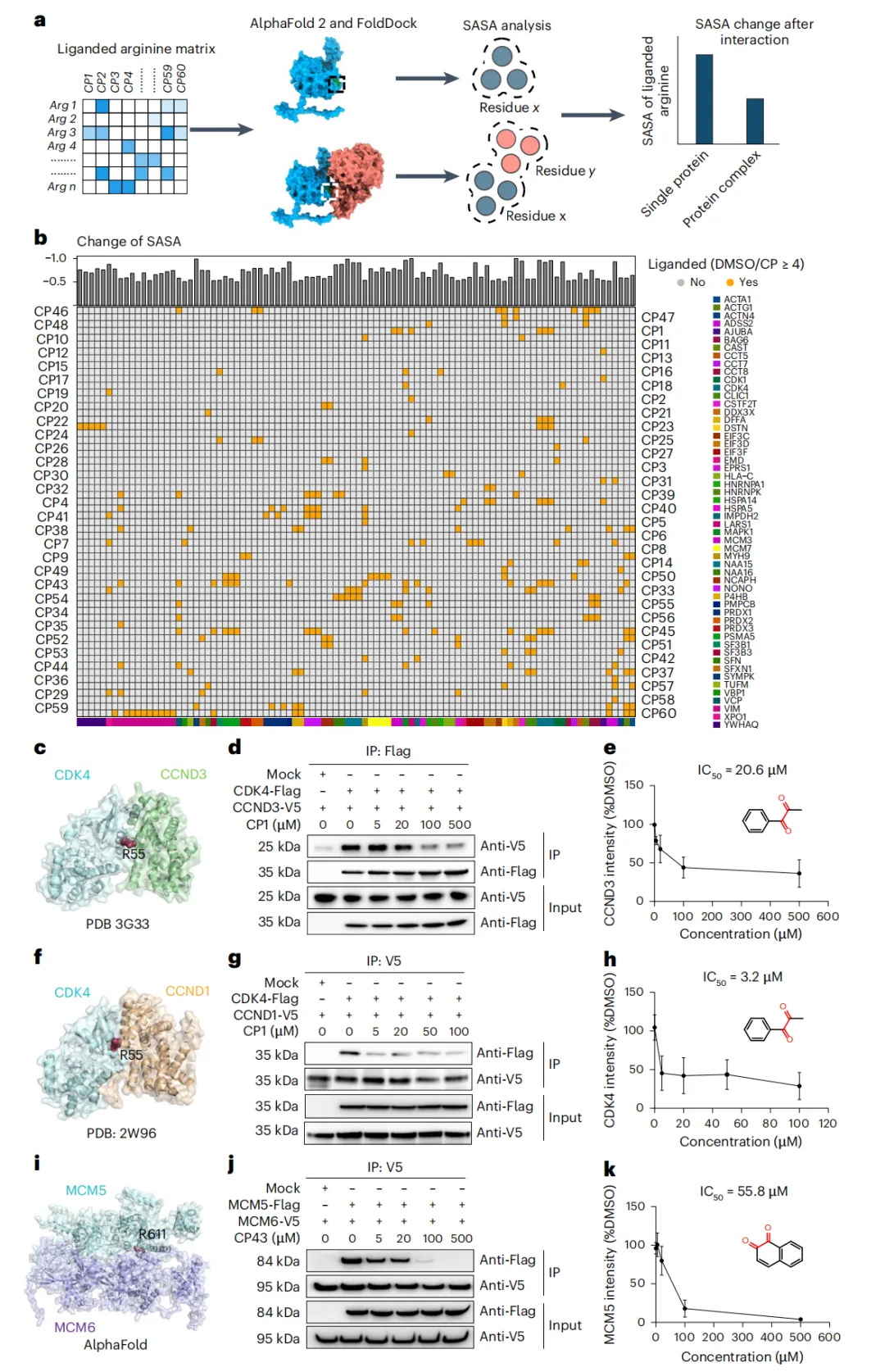
图6 | 酪氨酸靶向配体对蛋白质相互作用的干扰作用。a、示意图展示配体可结合的精氨酸在蛋白质复合物形成时表面积(SASA)的变化。b、潜在介导蛋白质相互作用的配体可结合精氨酸热图。这些精氨酸在二元复合物形成时SASA降低≥50%。c,f,i、选定蛋白质复合物中位于蛋白质相互作用界面的配体可结合精氨酸结构验证:CDK4–CCND3复合物(PDB 3G33)(c)、CDK4–CCND1复合物(PDB 2W96)(f)和MCM5–MCM6复合物(AlphaFold)(i)。d,g,j、不同浓度共价配体对蛋白质相互作用的破坏:CP1对CDK4–CCND3复合物的共免疫沉淀分析(d)、CP1对CDK4–CCND1复合物的共免疫沉淀分析(g)以及CP43对MCM5–MCM6复合物的共免疫沉淀分析(j)。代表性共免疫沉淀实验显示共价配体对选定蛋白质相互作用的剂量依赖性破坏。
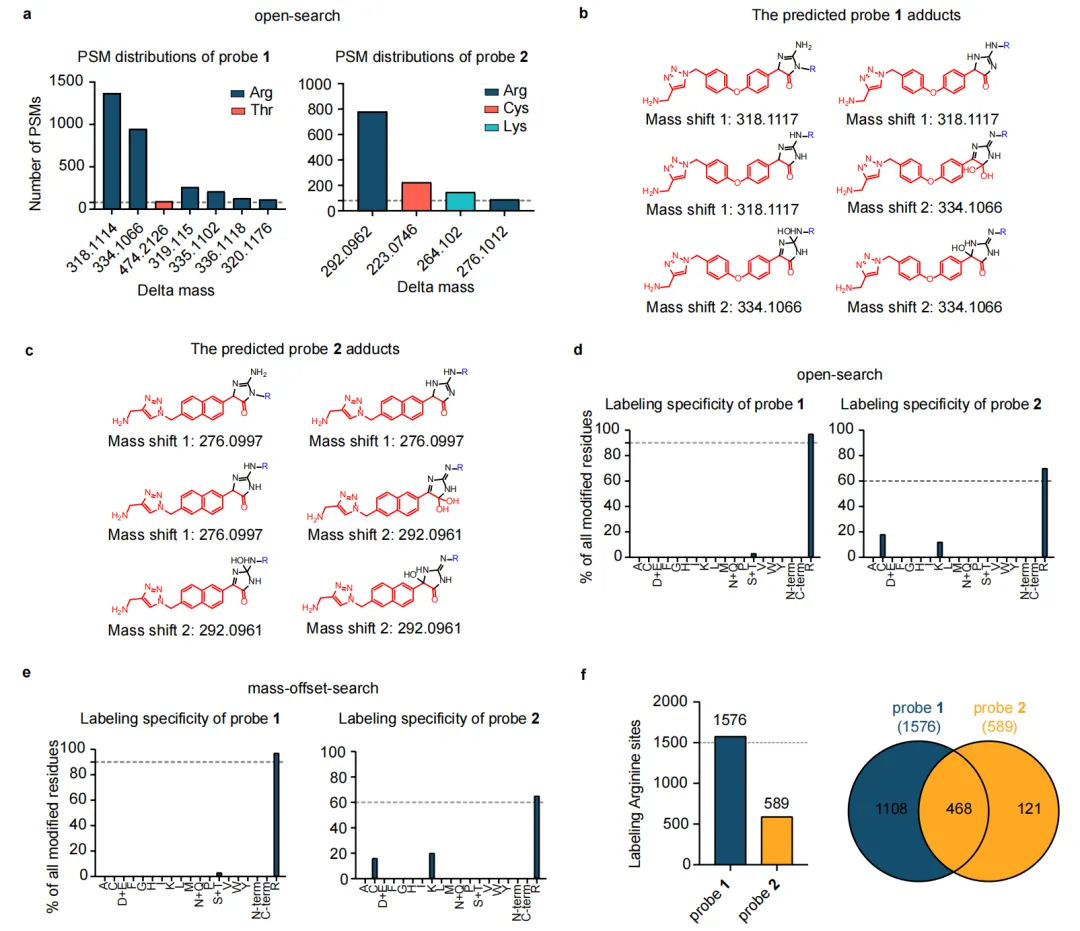
补充数据图1 | 探针1与2的特异性分析。a) 探针1和2的肽段修饰分布,考虑局部肽谱匹配(PSMs)超过80的情况。b) 探针1衍生加合物的拟议结构,对应质荷比变化值+318.1117 Da及其氧化形式(+334.1066 Da)。c) 探针2衍生加合物的拟议结构,对应质荷比变化值+276.0997 Da及其氧化产物(+292.0961 Da)。d) 采用开放搜索法进行探针选择性分析。e) 通过质荷比偏移搜索(基于(a)中质荷比变化值)确定探针1和2的选择性。f) 通过闭式搜索,利用各探针预期的差异质量识别修饰位点数量。
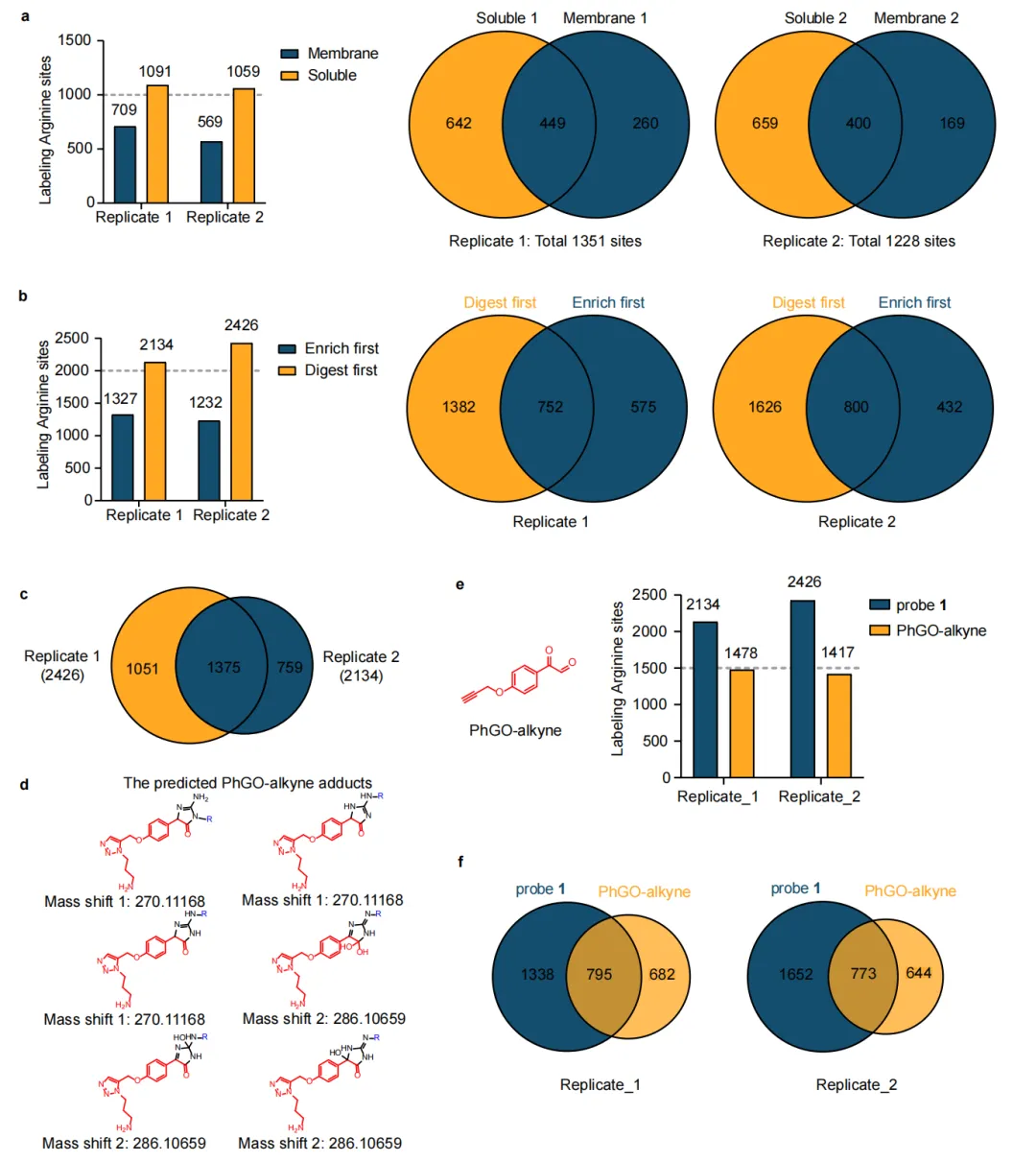
补充数据图2 | 增强精氨酸标记位点的策略。a) 使用探针1在膜组分和可溶性组分中鉴定精氨酸标记位点,包含两个生物学重复。b) 比较采用胰蛋白酶消化先于富集的替代流程与传统富集先于消化的方法,两种生物学重复均已完成。c) 人类蛋白质组中两个生物学重复标记的精氨酸位点重叠情况。d) PhGO-炔烃衍生加合物的拟议化学结构。e) HeLa细胞裂解液中通过探针1和PhGO-炔烃鉴定的精氨酸修饰位点比较。f) 探针1和PhGO-炔烃在人类蛋白质组中标记的精氨酸位点重叠情况。
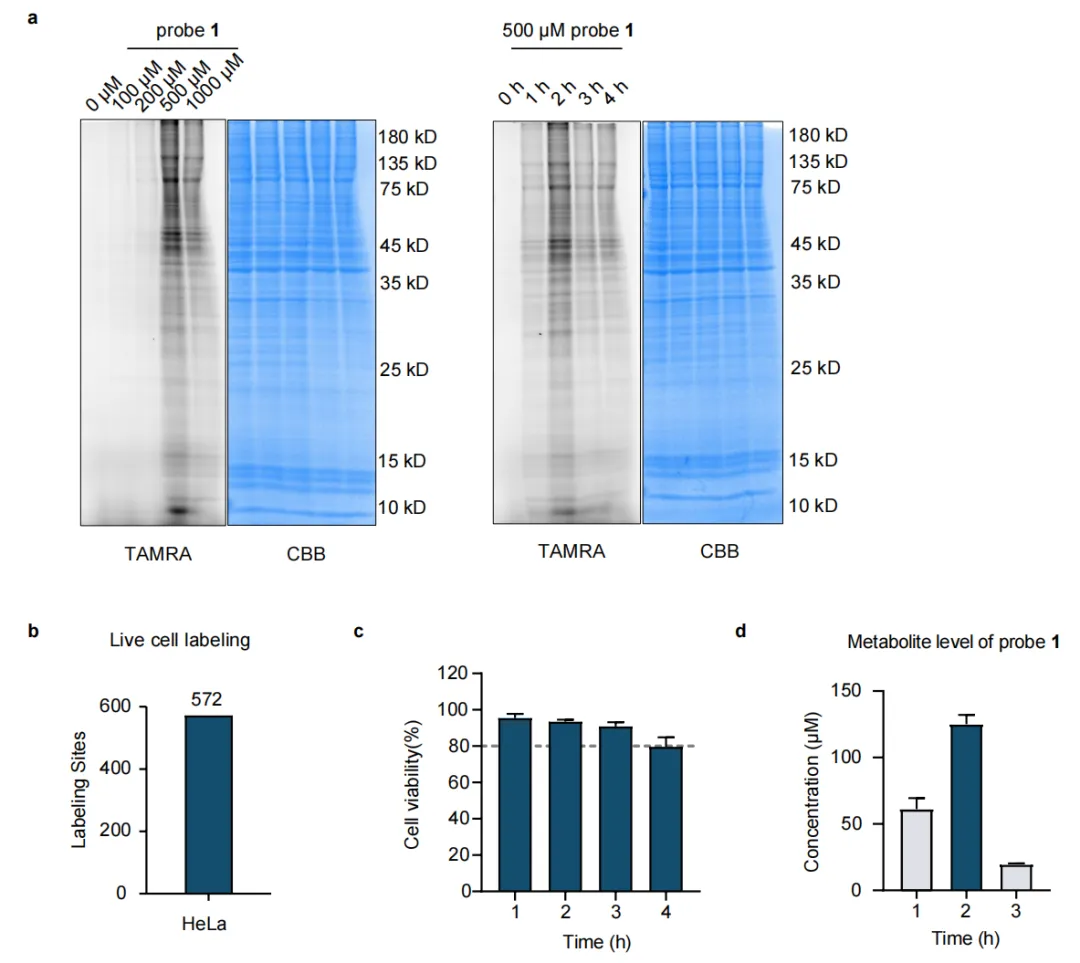
补充数据图3 | 探针1对活细胞精氨酸的标记。a) 探针1浓度与孵育时间对活细胞标记的优化。b) 通过探针1预期质量偏移的闭式搜索在活细胞中鉴定的精氨酸修饰位点数量。c) 通过CellTiter-Glo检测法测量的探针1在HeLa细胞中的细胞毒性。d) 通过靶向LC–MS/MS测定的探针1在HeLa细胞中的细胞内浓度。

补充数据图4 | 人类蛋白质组中精氨酸反应性的定量分析。a) 两个生物学重复样本的log2(R10:1)值瀑布图,代表用于量化蛋白质组中精氨酸反应性的探针修饰精氨酸位点。b-d) 对含高反应性精氨酸残基(GSHR R81、RIR1 R284及FSCN1 R217)的蛋白质进行标记验证。重组野生型(WT)蛋白及其对应的精氨酸-苏氨酸(R-to-K)突变体在HEK293T细胞中表达,使用探针1标记并通过凝胶内荧光分析。e) 采用蛋白质印迹法验证 LLPS 检测的蛋白表达。
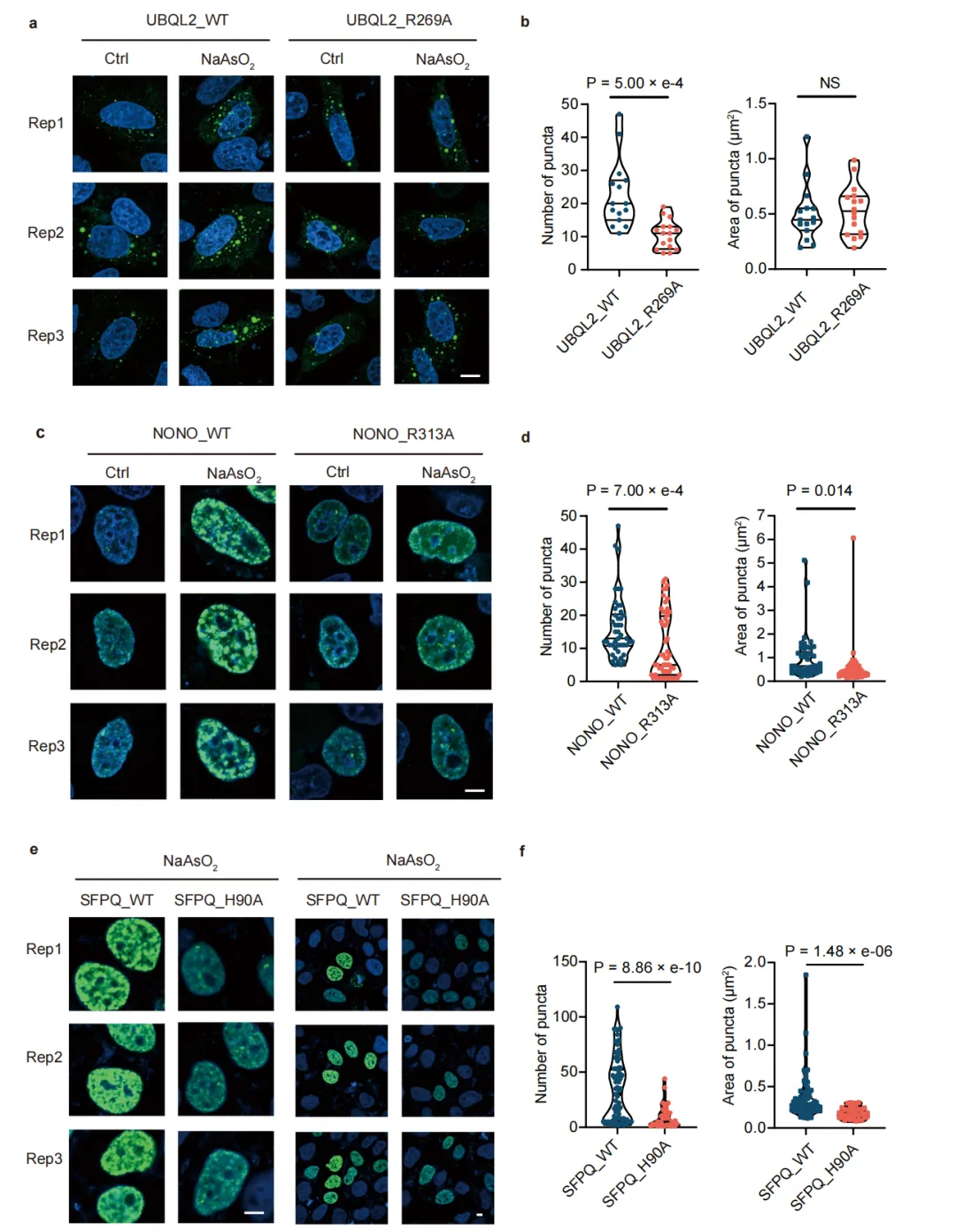
补充数据图5 | 阿尔吉宁- π 相互作用介导的相分离。a、c、e)荧光成像比较野生型与突变型细胞,证实R269在UBQL2(a)、R313在 NONO (c)及H90在 SFPQ (e)中促进相分离的功能作用。比例尺:5 μm 。n = 3个生物学独立重复样本。b、d、f)亚砷酸盐处理后野生型与突变型细胞(b中UBQL2 R269A突变体、d中 NONO R313A突变体、f中 SFPQ H90A突变体)斑点数量与大小的定量分析。
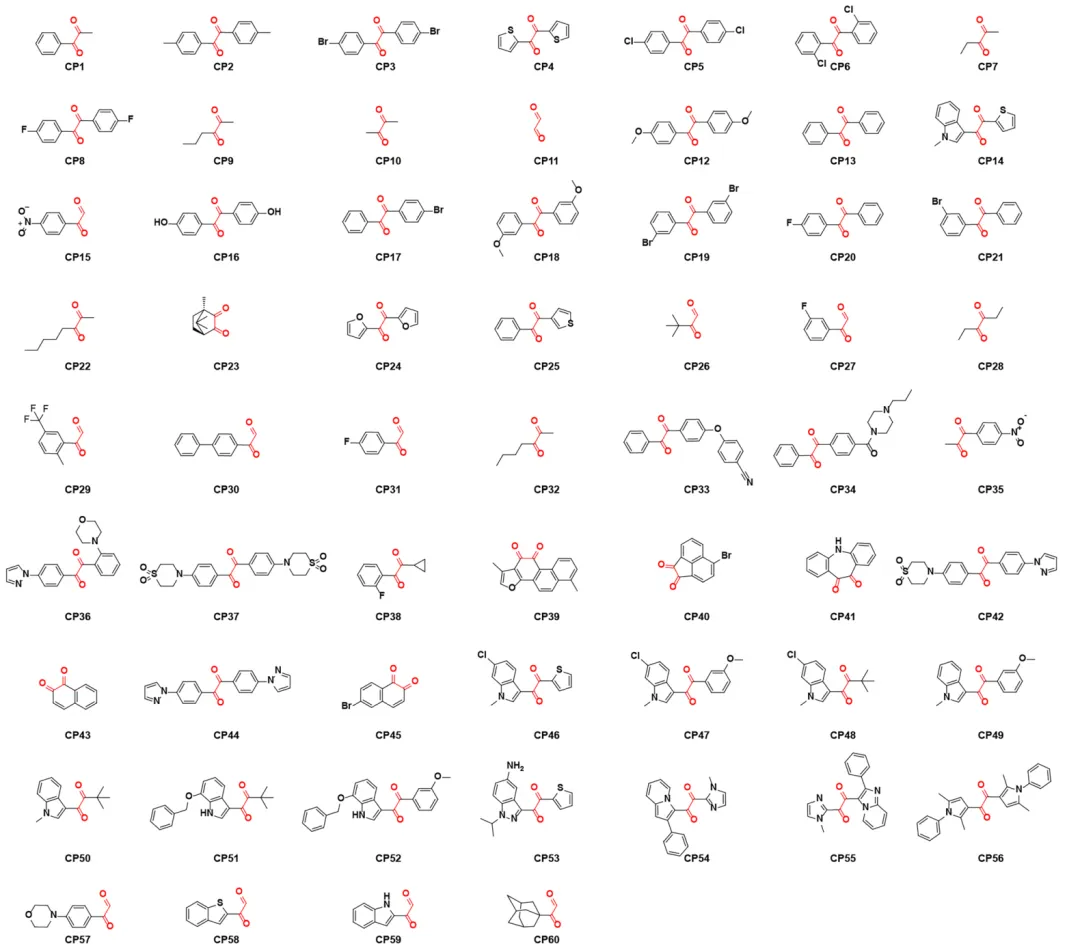
补充数据图6 | 本研究中使用的乙二醛化合物的化学结构。乙二醛化合物可分为三种结构类型:芳基二取代乙二醛(类型1)、烷基二取代乙二醛(类型2)和单取代乙二醛(类型3)。
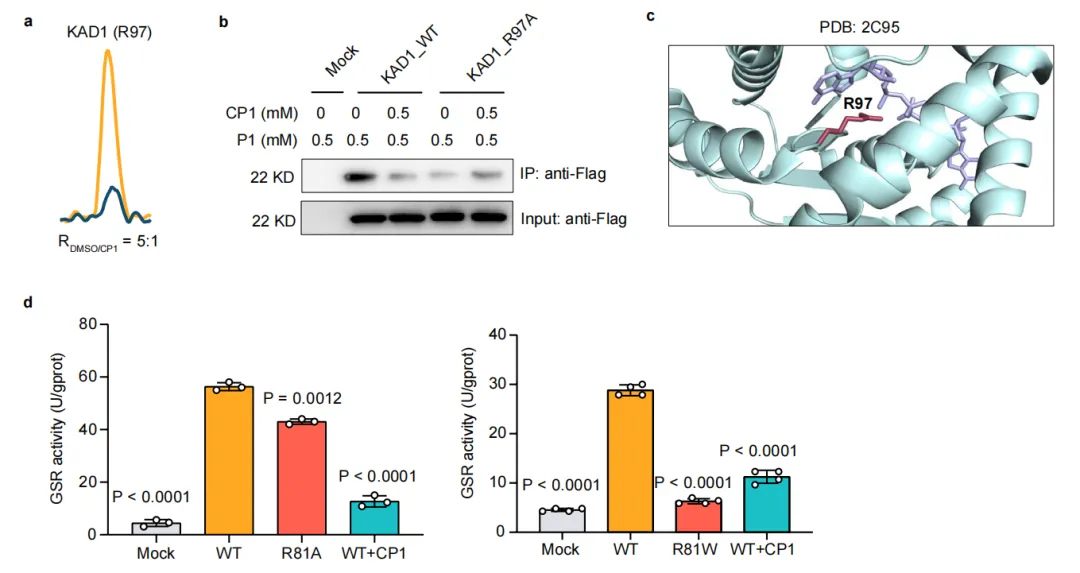
补充数据图7 | 细胞裂解液中配体结合精氨酸的验证。a) MS1提取离子色谱图(XIC)显示,当CP1与KAD1竞争时,探针1标记的肽段信号减弱。 XIC 下方标注了基于生物学重复计算的平均 RDMSO /CP值。b) 西部印迹验证显示,在表达野生型或精氨酸→丙氨酸突变体KAD1的HEK293T细胞裂解液中,CP1可选择性阻断探针1标记。c) KAD1结构模型(PDB: 2C95)突出显示配体结合的精氨酸残基。d) 条形图展示CP1、R81A和R81W突变对 GSHR 氧化还原依赖性酶活性的影响。
文献学习脑图总结:

以上内容均来自期刊官网、Pubmed平台,本公众号仅做整理分享。
推荐阅读:
Gut|复旦大学附属中山医院周俭院士和杨欣荣教授团队发表CD177+中性粒细胞能够驱动肝再生最新研究结果

专业医药科研服务商
文献PDF请识别下方二维码直接下载
Global profiling of arginine reactivity and ligandability in the human proteome.pdf

