中国科学院深圳先进技术研究院王怀雨《Advanced Materials》:声敏纳米苍耳实现NO介导的H2O2滞留抗菌疗法
- 2026-05-09 15:22:03
文章信息
生物膜感染因对传统治疗的固有抗性,已成为临床一大难题。近日,香港城市大学、中科院深圳先进技术研究院等团队在《Advanced Materials》发表重磅研究,提出“弃车保帅”的创新策略 —— 通过声敏纳米苍耳(G-B@NXs)释放牺牲性一氧化氮(NO),抑制H2O2清除系统并补充H2O2生成,最终高效清除生物膜,为植入物相关感染、皮肤软组织感染等治疗提供新方向!

要点分析
一、研究背景:生物膜感染的“顽固”根源
细菌生物膜是80% 细菌感染的元凶,可定植于组织、伤口及植入器械表面,形成由胞外聚合物(EPS)包裹的三维结构。传统消毒剂如H₂O₂虽能产生活性极强的羟基自由基(∙OH)杀灭浮游细菌,但面对生物膜时却“束手无策”:
1. 生物膜内细菌会分泌过氧化氢酶(CAT)和谷胱甘肽(GSH),快速降解H₂O₂,阻止∙OH 生成;
2.EPS 屏障阻碍H₂O₂渗透,内部细菌可启动适应性防御;
3.过量H₂O₂可能损伤正常组织,限制其临床应用。
因此,如何抑制H₂O₂清除系统、延长其滞留时间并精准发挥作用,成为突破生物膜感染的关键。
二、核心设计:多功能声敏纳米苍耳G-B@NXs
研究团队开发了一种仿生多功能纳米颗粒G-B@NXs,其设计巧思堪称 “精准打击”:
载体结构:以中空介孔二氧化硅制备纳米苍耳(NXs),仿生苍耳的棘刺结构可牢牢锚定在生物膜 EPS 网络上,提高局部富集度;
核心功能分子:
1.空腔内负载 NO 供体 BNN6,需超声(US)触发才释放 NO,实现 “按需激活”;
2.表面嫁接葡萄糖氧化酶(GOD),可催化葡萄糖生成H₂O₂,持续补充“弹药”。
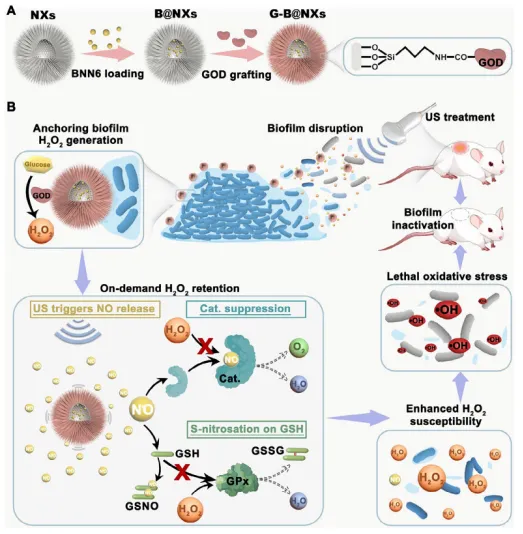
图1.建立按需保留H2O2的抗生物膜策略。(A)在空腔中含有NO供体,表面含有H2O2产生体的G-B@NXs的制备。(B)使用G-B@NXs处理生物膜示意图。G-B@NXs锚定在生物膜上并产生H2O2。在US照射下,G-B@NXs释放NO与周围的过氧化氢酶和谷胱甘肽反应,从而通过抑制清除剂引起H2O2积累。同时,US处理破坏了EPS网络,增加了生物膜对H2O2的敏感性,最终导致生物膜被有效清除。
三、关键机制:NO“牺牲”换H₂O₂滞留,三重协同杀菌
这一策略的核心在于牺牲性NO的巧妙运用,其作用机制已通过实验与理论计算双重验证:
1.NO优先占据CAT活性中心:DFT 计算显示,NO与CAT中血红素Fe³⁺的结合自由能远低于H₂O₂,可通过亚硝基化抑制CAT活性,阻止H₂O₂降解;
2.NO灭活GSH:NO与GSH发生S-亚硝基化反应生成GSNO,阻断谷胱甘肽过氧化物酶(GPx)介导的H₂O₂还原通路;
3.超声的双重作用:既触发NO精准释放,又机械破坏EPS屏障,暴露内部细菌,提升其对∙OH的敏感性。
三者协同实现“H₂O₂滞留-∙OH爆发-生物膜瓦解”的闭环,最终对细菌形成致命氧化应激。
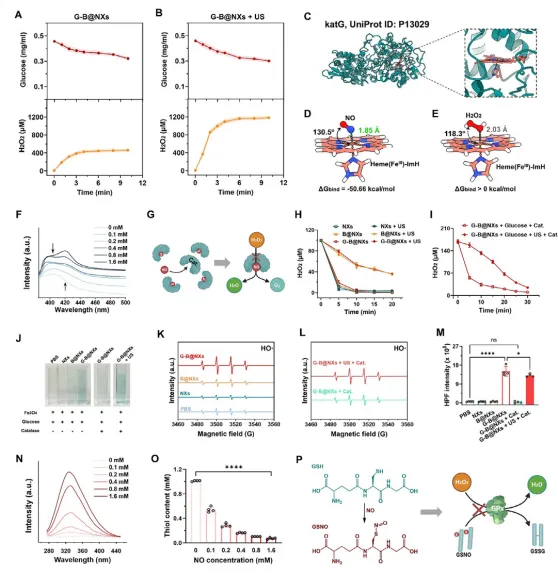
图3.NO对H2O2清除剂的抑制作用。
四、实验验证:体内外均展现高效抗菌活性
1. 材料表征与功能验证(图2)
G-B@NXs尺寸约264nm,具有良好的分散性和介孔结构;
1mgNXs可负载0.4 mg BNN6,GOD嫁接率达 26% 以上;
超声触发下NO释放浓度达15µM,且具有良好的组织穿透性(6-12 mm 猪组织屏障下仍有效);
GOD 可持续催化葡萄糖生成H₂O₂,10 min 达峰后稳定滞留。
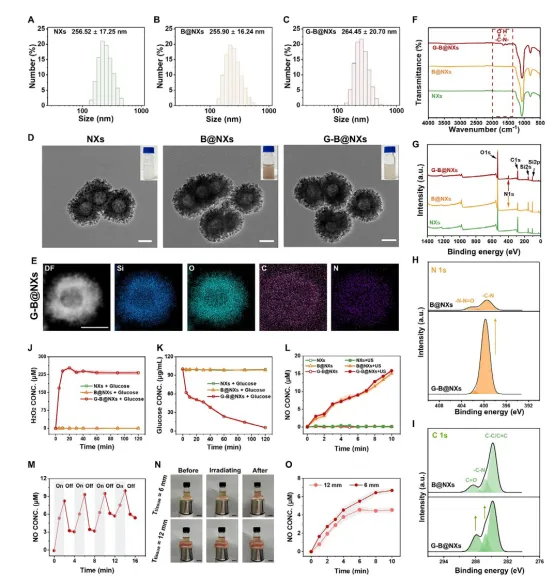
图2.NXs, B@NXs和G-B@NXs的表征
2. 体外抗菌:97.2%生物膜灭菌率
对大肠杆菌(E. coli)和金黄色葡萄球菌(S. aureus)生物膜的体外实验显示(图 4):
G-B@NXs+US组实现高效杀菌,对 E. coli 生物膜灭菌率达97.2%,S. aureus 达95.9%;
结晶紫染色与荧光成像证实,生物膜结构被彻底破坏,残留细菌多为死菌;
流式细胞术显示,两组生物膜的PI阳性率均达主导水平,证实杀菌效果。
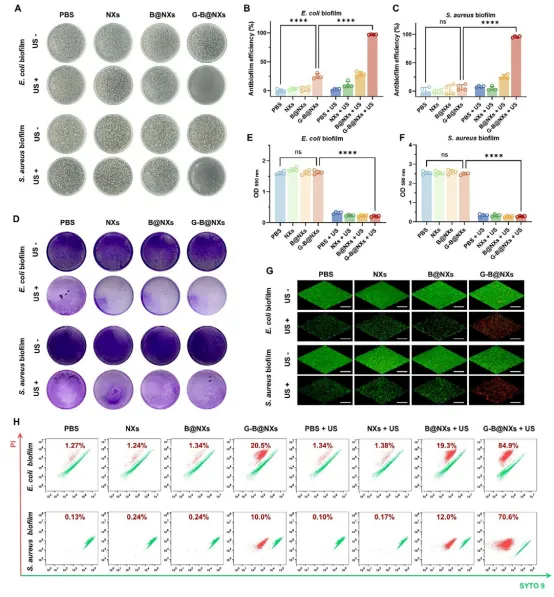
图4.超声辐照对不同纳米粒体外抗生物膜性能的影响
3. 体内实验:有效治疗植入性感染与皮肤软组织感染
(1)大鼠植入性感染模型(图 7)
G-B@NXs+US组植入部位炎症显著减轻,中性粒细胞浸润面积大幅下降;
炎症因子TNF-α、IL-6 水平显著降低,血液中白细胞、中性粒细胞计数恢复正常;
生物膜灭菌率达95.71%,且主要器官无明显损伤,生物安全性良好。
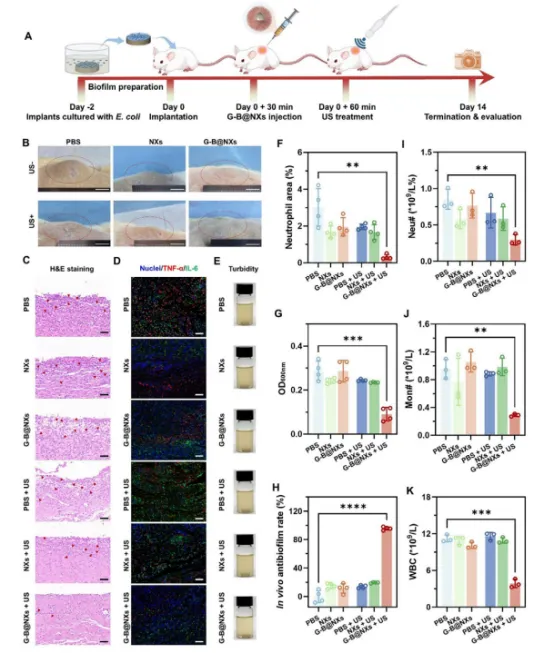
图7.使用大鼠模型进行植入物相关感染的体内抗菌膜活性评估
(2)小鼠皮肤软组织感染(SSTI)模型(图8)
治疗后12天,G-B@NXs+US组皮肤溃疡完全愈合,新生表皮完整;
Giemsa染色显示感染部位细菌几乎被清除,炎症细胞浸润消失;
抗炎巨噬细胞标志物CD206占主导,促进组织修复。
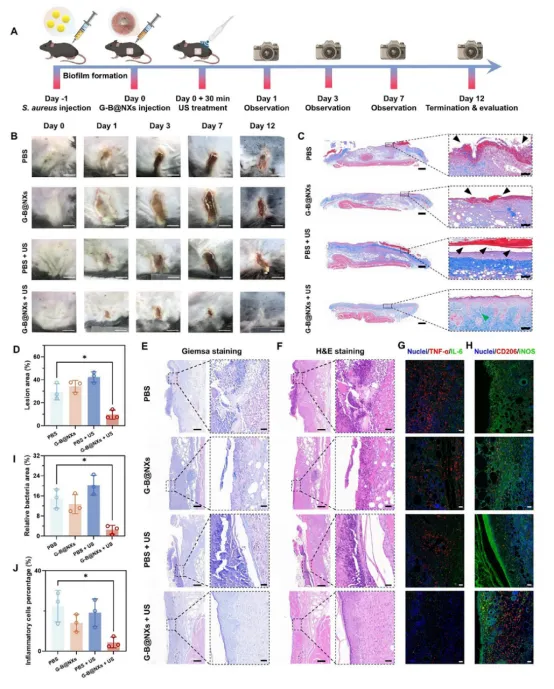
图8.使用SSTI小鼠模型进行体内抗生素膜性能评估。
五、研究意义与展望
该研究提出的“牺牲性NO介导H₂O₂滞留”策略,为生物膜感染治疗提供了全新思路:
1.首次将NO 用于抑制H₂O₂清除系统,实现“1+1>2”的协同杀菌效果;
2.G-B@NXs 的仿生锚定设计、超声按需激活特性,解决了药物富集与精准释放的难题;
3.体内外实验证实对植入性相关感染、皮肤软组织感染均有效,未来有望拓展至糖尿病相关感染等场景。
未来研究可进一步优化H₂O₂生成、滞留及∙OH转化效率,探索CO、H₂S等其他气体分子的协同作用,或结合蓝光触发等方式,进一步提升治疗效果。
论文链接DOI: 10.1002/adma.202521809往期推荐:最新分享
联系小编可免费投稿推送,本公众号另建有纳米医学实名学术交流群,请备注姓名+单位+研究方向添加下方微信号。
点击“阅读原文”,通往论文原文
「ENDING」


投稿微信|nanomedicine1
投稿邮箱|xianwenwang@126.com
关注纳米医学进展
了解纳米医学前沿
长按二维码私信投稿
申明:本微信号转发内容仅做学术交流使用,不作为商业用途,也不代表支持或赞同其观点,如涉及知识产权保护问题或其他方面的问题请及时联系小编,我们会尽快协调处理。本微信号原创文章版权归本微信号所有,欢迎分享。
